Clear Sky Science · de
Fütterungsfreie ex vivo‑Vermehrung von aus Nabelschnurblut gewonnenen natürlichen Killerzellen zur gesteigerten Proliferation und funktionellen Reifung
Warum das Wachstum natürlicher Killerzellen wichtig ist
Wissenschaftler arbeiten mit Hochdruck daran, körpereigene Immunzellen in vorrätige Krebsbehandlungen zu verwandeln. Zu den vielversprechendsten Kandidaten gehören natürliche Killerzellen (NK‑Zellen), die Krebszellen zerstören können, ohne für jeden Patienten individuell abgeglichen werden zu müssen. Diese Studie untersucht, wie man zuverlässig große Mengen NK‑Zellen aus Nabelschnurblut im Labor vermehren kann, ohne auf unterstützende „Feeder“‑Zellen zurückzugreifen, und wie dies so erfolgt, dass die Methode sowohl leistungsfähig als auch kostengünstig genug für Anwendungen in der Praxis ist.
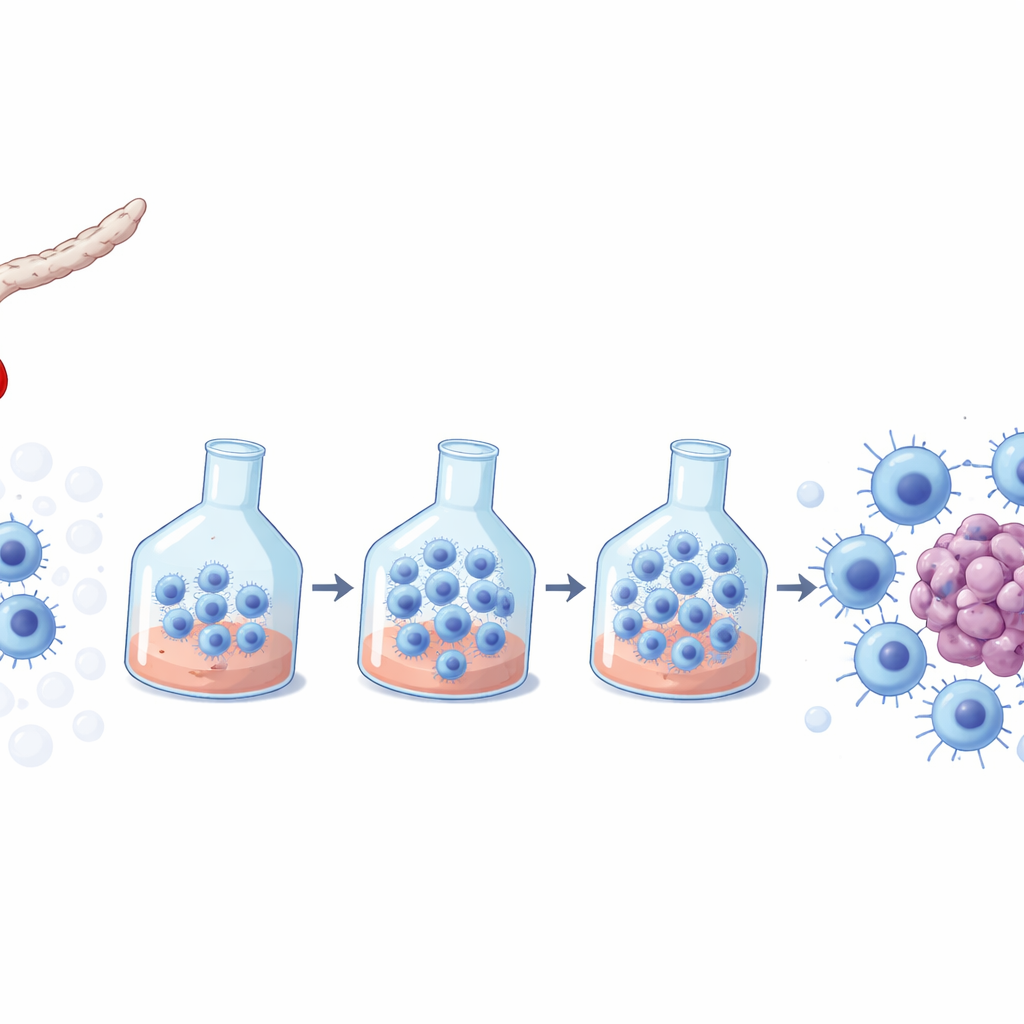
Eine krebsbekämpfende Zelle aus dem Blut Neugeborener
NK‑Zellen sind immunologische Wächter, die virusinfizierte oder krebsartige Zellen sofort erkennen und eliminieren können. Nabelschnurblut, das nach der Geburt aus der Nabelschnur entnommen wird, ist eine attraktive Quelle für NK‑Zellen: Es lässt sich leicht gewinnen, wird vielfach gelagert und birgt ein geringeres Risiko, beim Empfänger gefährliche Immunreaktionen auszulösen. Allerdings enthält jede Einheit Nabelschnurblut zu wenige NK‑Zellen, um einen Patienten direkt zu behandeln; daher müssen die Zellen ex vivo – außerhalb des Körpers – vermehrt werden, wobei ihre Potenz und Sicherheit erhalten bleiben müssen. Viele kommerzielle Rezepte zur NK‑Zell‑Vermehrung wurden für Erwachsenenblut entwickelt, sodass offen bleibt, welche am besten für aus Nabelschnurblut stammende NK‑Zellen geeignet sind.
Vergleich verschiedener Wachstumsrezepte
Die Forscher begannen damit, NK‑reiche CD56‑positive Zellen aus gefrorenen Nabelschnurblutproben mit magnetischen Beads zu isolieren. Dieser Schritt erhöhte den Anteil der NK‑Zellen deutlich, führte aber zur Wiedergewinnung von weniger als einem Drittel der Zellen und verursachte einige frühe Zellstress‑Anzeichen – ein Hinweis darauf, warum robuste Expansionsprotokolle notwendig sind. Das Team verglich anschließend sechs kommerziell erhältliche Kulturmedien, alle ergänzt mit dem Immunsignal Interleukin‑2, um zu ermitteln, welches Medium das fütterungsfreie NK‑Zellwachstum am besten unterstützt. Aus diesem Screening wählten sie drei Bedingungen für eine vertiefte Analyse aus: NK‑Xpander (NKX) und zwei Versionen von NK MACS (NKM1 mit niedrigerem Supplementlevel und NKM2 mit höherem).
Die Zellen vervielfachen und aktivieren
Bei etwa vierwöchiger Kultur durchliefen NK‑Zellen in NKX, NKM1 und NKM2 alle eine ruhige „Lag“‑Phase, bevor sie in eine robuste Wachstumsphase eintraten, in der sie Cluster bildeten und sich vermehrten. Im Mittel stieg die Gesamtzellzahl etwa um das 15–19‑Fache, was rund 200 Millionen Zellen pro Nabelschnurbluteinheit ergab, bei einer hohen Vitalität von über 90 %. Gleichzeitig verbesserten sich ihre krebsbekämpfenden Fähigkeiten deutlich. Frisch isolierte Zellen zeigten zunächst nur eine moderate Fähigkeit, eine Standard‑Leukämie‑Zelllinie zu töten, und geringe Anzeichen von Degranulation – dem Freisetzen toxischer Granula. Nach der Expansion zeigten NK‑Zellen aus allen drei Medien deutlich stärkere Zielzellabtötung und höhere Degranulationswerte, was darauf hindeutet, dass der ex vivo‑Prozess nicht nur die Zellzahlen erhöhte, sondern die Zellen auch funktionell aktivierte.
Verschiedene Ausprägungen von Killerzellen und die Kostenfrage
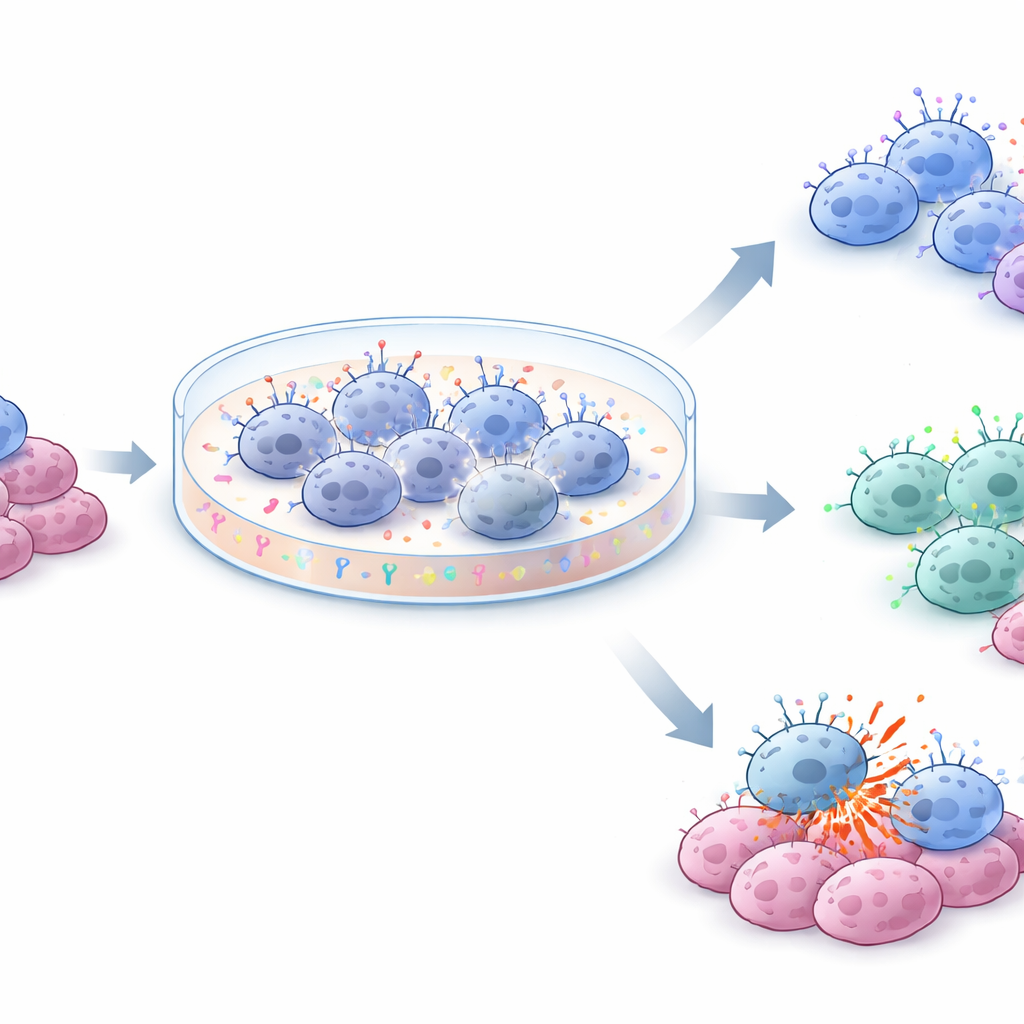
Obwohl die drei Medien eine ähnliche Gesamtvermehrung erzeugten, prägten sie die NK‑Zellen auf unterschiedliche Weise. Unter allen Bedingungen stieg ein aktivierender Oberflächenmarker, der mit Angriffbereitschaft assoziiert ist, deutlich an, während ein hemmender Marker relativ stabil blieb. In NKX blieb die Expression eines wichtigen Rezeptors, der mit antibodygesteuerter Zellabtötung verbunden ist, höher erhalten, wodurch eine Population aggressiverer, zytotoxischer Zellen erhalten blieb. Dagegen verschoben sich Zellen, die in NKM1 und NKM2 kultiviert wurden, allmählich zu einem CD56‑bright, CD16‑low Profil, das oft mit eher regulatorischem, signalproduzierendem Verhalten statt direkter Tötung assoziiert wird. Das Team führte zudem eine detaillierte Kostenanalyse durch. NKX und NKM1 erzeugten Zellen zu vergleichbaren Kosten pro Million, während NKM2, das doppelt so viel Supplement verwendete, die Herstellkosten annähernd verdoppelte, ohne klar überlegene Leistung zu liefern.
Was das für zukünftige Therapien bedeutet
Für nichtfachliche Leser lautet die Kernbotschaft: Es ist nun möglich, große Chargen von aus Nabelschnurblut gewonnenen NK‑Zellen im Labor ohne komplexe Feeder‑Systeme zu züchten und sie dabei lebendig, aktiv und relativ kostengünstig zu halten. NK‑Xpander bot die verlässlichste Expansion über verschiedene Spender hinweg und bewahrte besser NK‑Zellen, die gut mit therapeutischen Antikörpern zusammenarbeiten können, wodurch es sich besonders für krebsbekämpfende Anwendungen eignet. NK MACS, insbesondere bei niedrigerem Supplementlevel, vermehrte die Zellen ebenfalls effektiv, tendierte jedoch dazu, ein stärker regulatorisch geprägtes NK‑Profil zu erzeugen, das für andere klinische Ziele passend sein könnte. Insgesamt liefert diese Arbeit eine praxisnahe Roadmap, um gespendetes Nabelschnurblut in standardisierte, skalierbare NK‑Zellprodukte zu verwandeln, die als gebrauchsfertige Immuntherapien gelagert und verschickt werden könnten.
Zitation: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
Schlüsselwörter: Nabelschnurblut, natürliche Killerzellen, Krebsimmuntherapie, Zellvermehrung, vorrätige Therapien