Clear Sky Science · zh
关于M2型巨噬细胞对PYCR1促进的肝细胞癌细胞生物学行为影响及机制的研究
为何这项肝癌研究重要
原发性肝癌,以肝细胞癌为主,是全球最致命的癌症之一,部分原因在于它常常早期转移并耐受治疗。该研究聚焦于一种鲜为人知的代谢酶PYCR1以及一类称为巨噬细胞的免疫细胞,旨在弄清肝肿瘤如何生长、扩散并逃避细胞死亡。通过揭示这些参与者在肿瘤“邻里”中的协作方式,工作指向了一个新的薄弱环节,未来药物或可针对该环节来减缓或阻止肝癌进展。
肿瘤周围的“邻里”
癌症并非孤立生长;它存在于由血管、基质细胞和免疫细胞构成的复杂“邻里”中,称为肿瘤微环境。在肝癌中,肿瘤相关巨噬细胞是最丰富的免疫细胞类型之一。这些细胞可展现不同“性格”:有的攻击肿瘤,而另一些被称为M2型巨噬细胞,则抑制炎症并最终可能助长癌症。大量研究表明,当M2型细胞占优势时,肿瘤往往生长更快、易于转移且对治疗反应差。这提出了一个重要问题:这些“助攻型”巨噬细胞究竟如何推动肝癌细胞朝更具恶性的行为发展?
助长危险生长的酶
研究人员将注意力集中在PYCR1上,这是一种帮助细胞合成氨基酸脯氨酸的酶,脯氨酸是胶原等结构蛋白的重要组成部分,也是快速分裂细胞的重要“燃料”。通过分析患者数据,他们发现PYCR1在肝肿瘤中的表达高于正常肝组织,且肿瘤中PYCR1表达较高并伴有更多M2型巨噬细胞浸润的患者预后更差。这提示PYCR1可能是肿瘤细胞代谢改变与其有害免疫微环境之间的关键联系。
巨噬细胞如何促使肿瘤细胞扩散
为检验该假说,团队将肝癌细胞系在含有M2型巨噬细胞分泌物的培养基中培养。处于这些条件下的癌细胞变得更具侵袭性:它们在人工“伤口”上移动更快,更容易穿透隔膜,并表现出提示从稳定的上皮样状态向更为灵活、易迁移的间质样状态转变的蛋白学改变。这一被称为上皮—间质转化的开关是转移的关键步骤。当科学家使用遗传学手段降低癌细胞中的PYCR1水平时,这些由M2驱动的效应在很大程度上被逆转,细胞的迁移和侵袭能力下降,表明PYCR1对于巨噬细胞信号完全赋能肿瘤细胞是必需的。
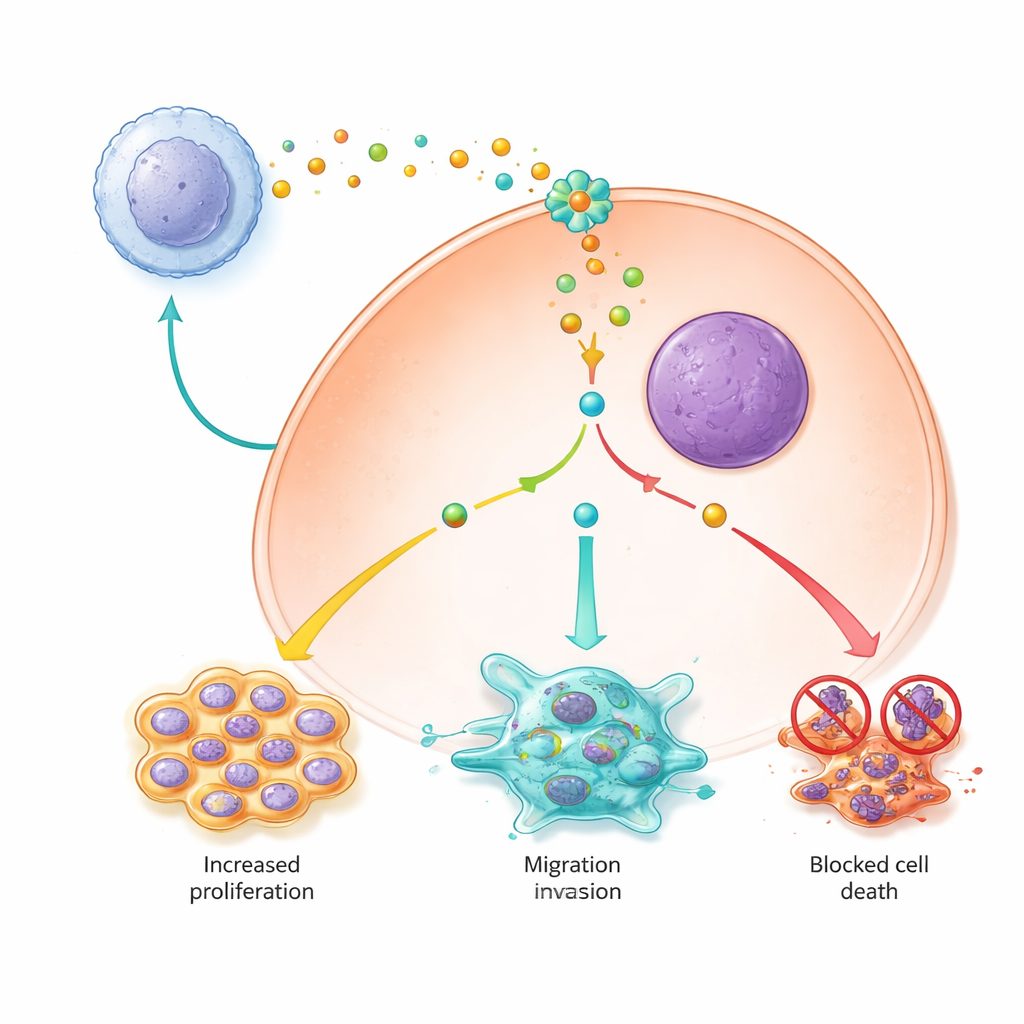
维持癌细胞存活与增殖
研究还显示,M2型巨噬细胞的信号通过改变关键生存通路,帮助肝癌细胞存活并增殖。暴露于M2条件培养上清的癌细胞分裂更快,更不易发生程序性细胞死亡,并且对一种新型的依赖铁的细胞死亡形式——铁死亡(ferroptosis)更为抵抗。细胞内部,PYCR1成为一个核心开关:当它活跃时,一条名为JAK2/STAT3的主要信号通路被更强地激活,促生存蛋白增加,阻止铁死亡的蛋白升高,同时有害的游离铁和反应性分子保持在较低水平。敲低PYCR1或使用小分子抑制剂阻断JAK信号会削弱这一级联反应,减慢增殖,并恢复细胞凋亡和铁死亡。
对未来治疗的意义
总体而言,研究结果将PYCR1描绘为一种“主帮手”,使肝癌细胞能够充分利用M2型巨噬细胞的支持:它促进生长,支持形态转变与扩散,并保护细胞免受两种细胞死亡形式的侵害。对患者而言,这提示针对PYCR1的药物,尤其是与重编程或耗竭肿瘤支持性巨噬细胞的疗法联合使用,可能从多方面同时打击肝癌。尽管这些实验在细胞培养体系中进行,仍需在动物模型和临床研究中进一步验证,但它们突出表明PYCR1及肿瘤微环境是寻求更有效肝癌治疗的有前景靶点。
引用: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
关键词: 肝细胞癌, 肿瘤微环境, 巨噬细胞, PYCR1, JAK2 STAT3