Clear Sky Science · fr
Étude sur les effets et les mécanismes des macrophages M2 sur le comportement biologique des cellules du carcinome hépatocellulaire promu par PYCR1
Pourquoi cette étude sur le cancer du foie est importante
Le cancer primaire du foie, principalement le carcinome hépatocellulaire, fait partie des cancers les plus meurtriers dans le monde, en partie parce qu’il se propage souvent tôt et résiste aux traitements. Cette étude examine une enzyme métabolique peu connue, PYCR1, ainsi qu’un groupe de cellules immunitaires appelées macrophages afin de comprendre comment les tumeurs hépatiques croissent, se disséminent et échappent à la mort cellulaire. En révélant comment ces acteurs coopèrent au sein du « voisinage » tumoral, le travail met en lumière une nouvelle faiblesse potentielle que de futurs médicaments pourraient cibler pour ralentir ou arrêter le cancer du foie.
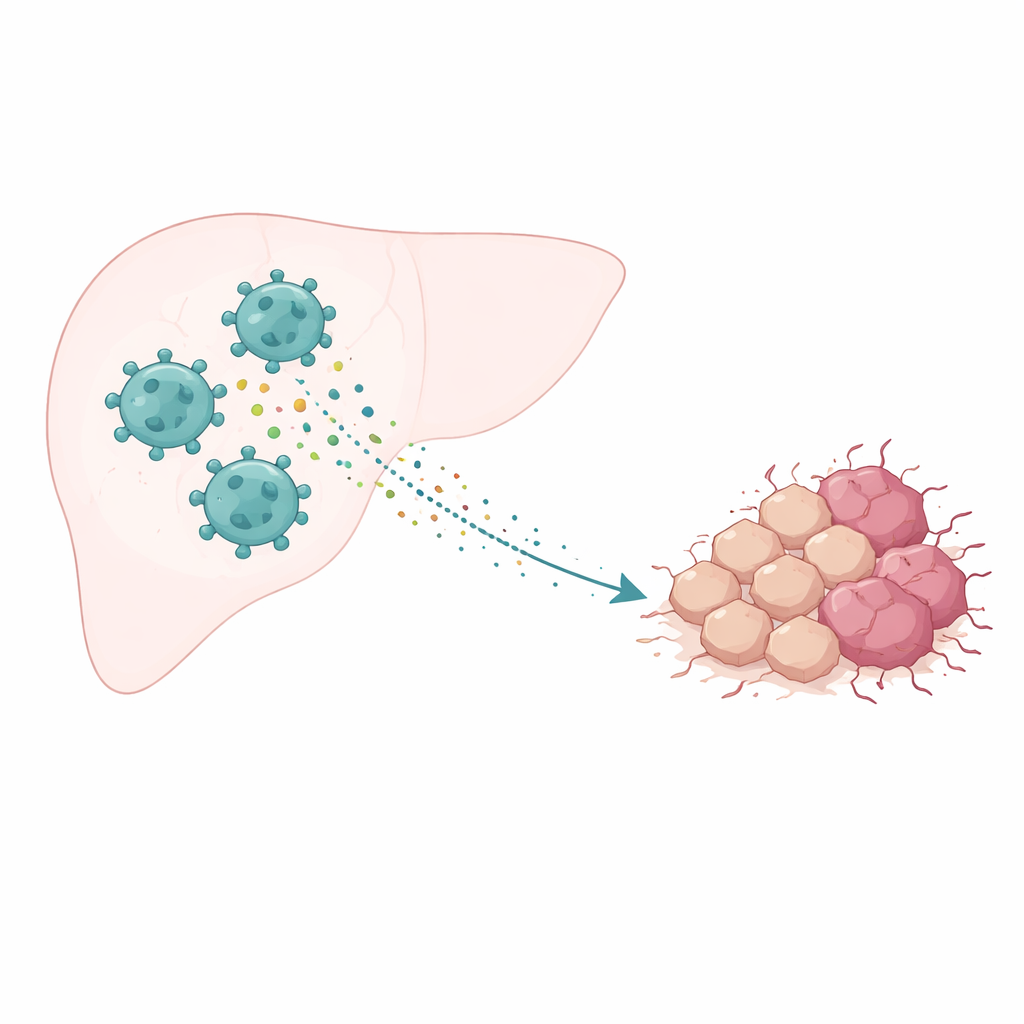
Le voisinage autour d’une tumeur
Le cancer ne se développe pas en isolation ; il vit dans un « voisinage » complexe de vaisseaux sanguins, de cellules de soutien et de cellules immunitaires appelé microenvironnement tumoral. Dans le cancer du foie, l’un des types de cellules immunitaires les plus abondants est le macrophage associé à la tumeur. Ces cellules peuvent adopter des personnalités différentes : certaines attaquent les tumeurs, tandis que d’autres, dites de type M2, apaisent l’inflammation et peuvent finir par aider le cancer. De nombreuses études ont montré que lorsque les cellules de type M2 dominent, les tumeurs ont tendance à croître plus rapidement, à se propager plus facilement et à répondre moins bien au traitement. Cela a soulevé une question importante : comment ces macrophages de type aide‑poste poussent‑ils exactement les cellules du cancer du foie vers un comportement plus malin ?
Une enzyme qui alimente une croissance dangereuse
Les chercheurs se sont concentrés sur PYCR1, une enzyme qui aide les cellules à synthétiser l’acide aminé proline, composant clé des protéines structurales comme le collagène et carburant important pour les cellules qui se divisent rapidement. En analysant des données de patients, ils ont constaté que les niveaux de PYCR1 sont plus élevés dans les tumeurs du foie que dans le tissu hépatique normal, et que les patients dont les tumeurs montrent davantage de PYCR1 et une infiltration plus importante de macrophages de type M2 ont tendance à avoir une survie moins bonne. Cela suggère que PYCR1 pourrait être un lien crucial entre le métabolisme altéré des cellules tumorales et l’influence néfaste de leur environnement immunitaire.
Comment les macrophages poussent les cellules tumorales à se disséminer
Pour tester cette idée, l’équipe a fait croître des lignées de cellules du cancer du foie dans des boîtes avec le milieu recueilli auprès de macrophages de type M2. Dans ces conditions, les cellules cancéreuses sont devenues plus agressives : elles ont migré plus vite à travers des « plaies » artificielles, envahi des membranes plus facilement et montré des modifications protéiques indiquant une transition d’un état épithélial stable et pavimenteux vers un état mésenchymateux plus flexible et prêt au voyage. Ce basculement, connu sous le nom de transition épithélio‑mésenchymateuse, est une étape clé de la métastase. Lorsque les scientifiques ont utilisé des outils génétiques pour diminuer les niveaux de PYCR1 dans les cellules tumorales, ces effets induits par les M2 ont été en grande partie inversés : les cellules sont devenues moins mobiles et moins invasives, indiquant que PYCR1 est nécessaire pour que les signaux des macrophages renforcent pleinement les cellules tumorales.
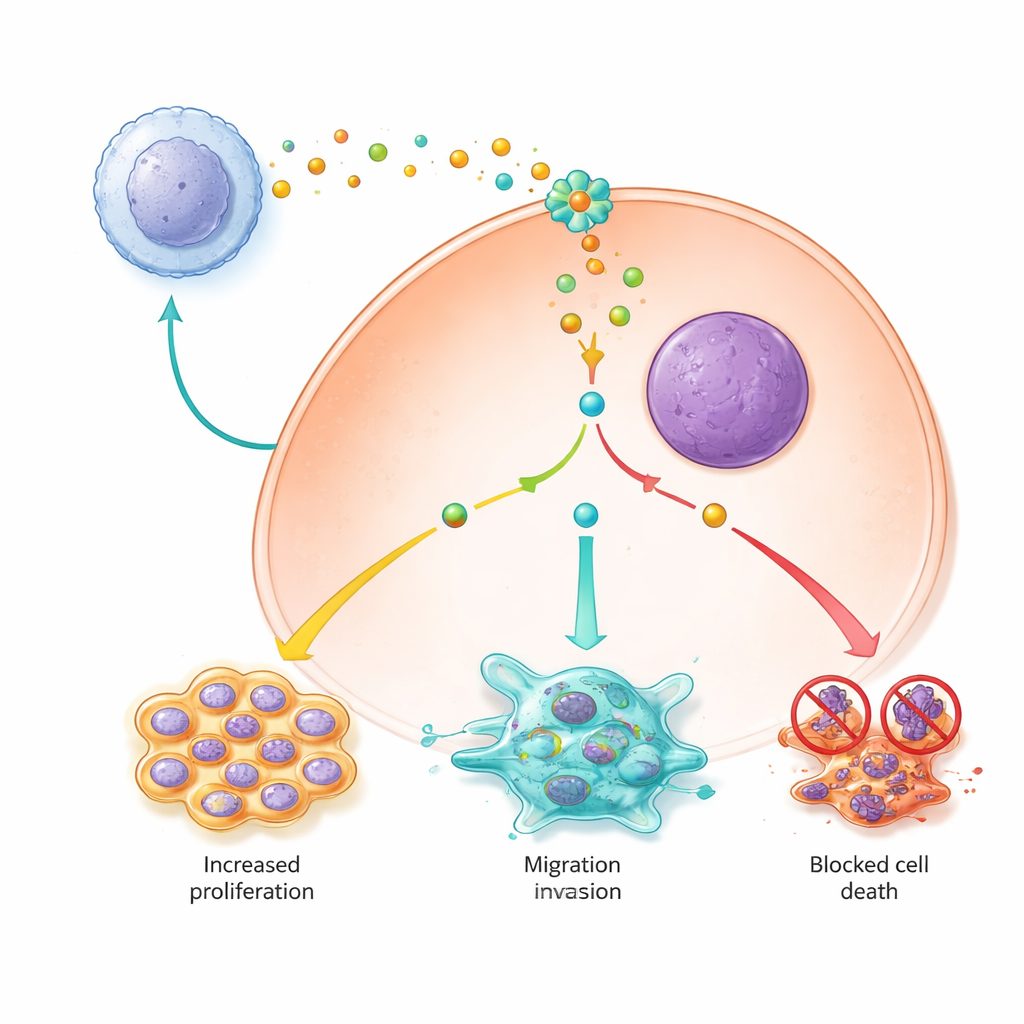
Maintenir les cellules cancéreuses en vie et en division
L’étude a également montré que les signaux des macrophages de type M2 aident les cellules du cancer du foie à rester en vie et à se multiplier en modifiant des voies de survie clés. Les cellules exposées au milieu conditionné par les M2 se divisaient plus rapidement, étaient moins susceptibles de subir la mort cellulaire programmée et moins enclines à une forme plus récente de mort cellulaire dépendante du fer appelée ferroptose. À l’intérieur des cellules, PYCR1 s’est avéré être un interrupteur central : lorsqu’il était actif, une voie de signalisation majeure appelée JAK2/STAT3 était plus fortement activée, les protéines pro‑survie augmentaient, et les protéines qui bloquent la ferroptose étaient élevées tandis que le fer délétère et les espèces réactives restaient bas. L’inhibition de PYCR1 ou le blocage de la signalisation JAK par un inhibiteur de petite molécule affaiblissaient cette cascade, ralentissaient la prolifération et rétablissaient à la fois l’apoptose et la ferroptose.
Ce que cela signifie pour les traitements futurs
Dans l’ensemble, les résultats présentent PYCR1 comme un facilitateur majeur qui permet aux cellules du cancer du foie d’exploiter pleinement le soutien des macrophages de type M2 : il stimule la croissance, permet le changement de forme et la dissémination, et protège les cellules contre deux formes de mort. Pour les patients, cela suggère que des médicaments conçus pour bloquer PYCR1, en particulier associés à des traitements qui reprogramment ou réduisent les macrophages qui soutiennent la tumeur, pourraient attaquer le cancer du foie sur plusieurs fronts à la fois. Bien que ces expériences aient été réalisées en cultures cellulaires et nécessitent encore une confirmation dans des modèles animaux et des études cliniques, elles mettent en évidence PYCR1 et le microenvironnement tumoral comme des cibles prometteuses dans la quête de thérapies hépatiques plus efficaces.
Citation: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Mots-clés: carcinome hépatocellulaire, microenvironnement tumoral, macrophages, PYCR1, JAK2 STAT3