Clear Sky Science · pl
Badanie nad efektami i mechanizmami działania makrofagów M2 na promowaną przez PYCR1 biologiczną aktywność komórek raka wątrobowokomórkowego
Dlaczego to badanie nad rakiem wątroby ma znaczenie
Pierwotny rak wątroby, głównie rak wątrobowokomórkowy, jest jednym z najbardziej śmiertelnych nowotworów na świecie, częściowo dlatego, że często wczesnie się rozsiewa i jest oporny na leczenie. W tym badaniu przyjrzano się stosunkowo mało znanemu enzymowi metabolicznemu, PYCR1, oraz grupie komórek odpornościowych zwanych makrofagami, aby zrozumieć, jak guzy wątroby rosną, rozprzestrzeniają się i unikają śmierci komórkowej. Odkrywając, jak ci aktorzy współdziałają w obrębie „sąsiedztwa” guza, praca wskazuje nowe słabe ogniwo, które przyszłe leki mogłyby wykorzystać, by spowolnić lub zatrzymać rozwój raka wątroby.
Sąsiedztwo wokół guza
Nowotwór nie rośnie w izolacji; funkcjonuje w złożonym „sąsiedztwie” naczyń krwionośnych, komórek podporowych i komórek odpornościowych znanym jako mikrośrodowisko guza. W raku wątroby jednym z najliczniejszych typów komórek odpornościowych są makrofagi związane z guzem. Komórki te mogą przyjmować różne „osobowości”: niektóre atakują guz, podczas gdy inne, zwane makrofagami typu M2, łagodzą zapalenie i mogą ostatecznie wspierać rozwój nowotworu. Wiele badań wykazało, że gdy dominują komórki typu M2, guzy zwykle rosną szybciej, łatwiej się rozsiewają i gorzej reagują na leczenie. To postawiło ważne pytanie: w jaki dokładnie sposób te pomocnicze makrofagi napędzają bardziej złośliwe zachowanie komórek raka wątroby?
Enzym, który zasila niebezpieczny wzrost
Naukowcy skupili się na PYCR1, enzymie pomagającym komórkom w syntezie aminokwasu prolina, istotnego składnika białek strukturalnych, takich jak kolagen, oraz ważnego paliwa dla szybko dzielących się komórek. Analizując dane pacjentów, odkryli, że poziomy PYCR1 są wyższe w guzach wątroby niż w zdrowej tkance wątrobowej, a pacjenci, których guzy wykazywały podwyższone stężenie PYCR1 i większą infiltrację makrofagów typu M2, mieli gorsze przeżycie. Sugerowało to, że PYCR1 może być kluczowym ogniwem łączącym zmieniony metabolizm komórek nowotworowych z szkodliwym wpływem ich odpornościowego otoczenia.
Jak makrofagi skłaniają komórki guza do rozsiewu
Aby przetestować tę hipotezę, zespół hodował linie komórek raka wątroby w naczyniach zawierających płyn pozyskany z makrofagów typu M2. W tych warunkach komórki nowotworowe stały się bardziej agresywne: szybciej przemieszczały się po sztucznych „ranach”, chętniej inwadowały przez membrany i wykazywały zmiany w profilach białek sugerujące przejście ze stabilnego, «brukowanego» stanu nabłonkowego do bardziej elastycznego, przygotowanego do migracji stanu mezenchymalnego. Ta zmiana, znana jako przejście epitelialno‑mezenchymalne, jest kluczowym krokiem w procesie przerzutowania. Gdy naukowcy użyli narzędzi genetycznych do obniżenia poziomu PYCR1 w komórkach nowotworowych, te efekty wywołane przez M2 zostały w dużej mierze odwrócone, a komórki stały się mniej ruchliwe i mniej inwazyjne, co wskazuje, że PYCR1 jest niezbędny, aby sygnały makrofagów w pełni wzmocniły komórki guza.
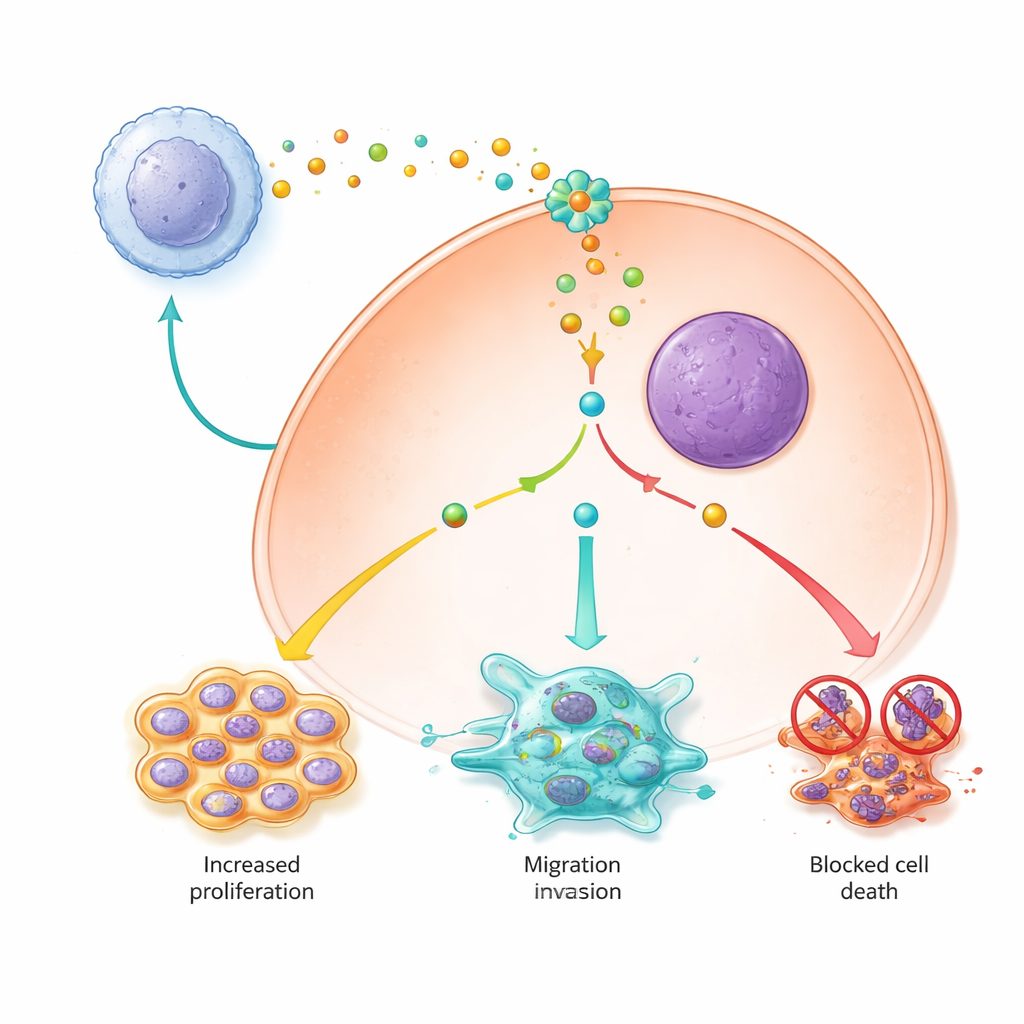
Utrzymywanie komórek rakowych przy życiu i w podziale
Badanie wykazało również, że sygnały makrofagów typu M2 pomagają komórkom raka wątroby przetrwać i mnożyć się poprzez modyfikację kluczowych szlaków przeżycia. Komórki narażone na medium kondycjonowane przez M2 dzieliły się szybciej, były mniej podatne na programowaną śmierć komórkową i rzadziej ulegały nowszej formie zależnej od żelaza śmierci — ferroptozie. Wewnątrz komórek PYCR1 okazał się centralnym przełącznikiem: gdy był aktywny, główny szlak sygnałowy JAK2/STAT3 był silniej włączony, białka pro‑przeżyciowe wzrastały, a białka blokujące ferroptoza były podwyższone, podczas gdy szkodliwe żelazo i reaktywne cząsteczki były utrzymywane na niskim poziomie. Zmniejszenie ekspresji PYCR1 lub zablokowanie sygnalizacji JAK małocząsteczkowym inhibitorem osłabiło tę kaskadę, spowolniło proliferację i przywróciło zarówno apoptozę, jak i ferroptozę.
Co to oznacza dla przyszłych terapii
Podsumowując, wyniki przedstawiają PYCR1 jako głównego pomocnika, który pozwala komórkom raka wątroby w pełni wykorzystać wsparcie makrofagów typu M2: zwiększa wzrost, umożliwia zmianę kształtu i rozsiew, oraz chroni komórki przed dwoma formami śmierci. Dla pacjentów sugeruje to, że leki zaprojektowane do blokowania PYCR1, zwłaszcza w połączeniu z terapiami, które przeprogramowują lub usuwają makrofagi wspierające guz, mogłyby jednocześnie zaatakować raka wątroby na kilku frontach. Chociaż eksperymenty te przeprowadzono w hodowlach komórkowych i wciąż wymagają potwierdzenia w modelach zwierzęcych i badaniach klinicznych, podkreślają PYCR1 i mikrośrodowisko guza jako obiecujące cele w poszukiwaniu skuteczniejszych terapii raka wątroby.
Cytowanie: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Słowa kluczowe: rak wątrobowokomórkowy, mikrośrodowisko guza, makrofagi, PYCR1, JAK2 STAT3