Clear Sky Science · de
Studie über die Auswirkungen und Mechanismen von M2‑Makrophagen auf das von PYCR1 geförderte biologische Verhalten von hepatozellulären Karzinomzellen
Warum diese Leberkrebsstudie wichtig ist
Primärer Leberkrebs, überwiegend hepatozelluläres Karzinom, gehört weltweit zu den tödlichsten Krebsarten, nicht zuletzt weil er oft früh metastasiert und behandlungsresistent ist. Diese Studie beleuchtet ein wenig untersuchtes Stoffwechselenzym, PYCR1, und eine Gruppe von Immunzellen, die Makrophagen genannt werden, um zu verstehen, wie Lebertumoren wachsen, sich ausbreiten und dem Zelltod entgehen. Indem untersucht wird, wie diese Akteure im Umfeld des Tumors zusammenwirken, eröffnet die Arbeit einen neuen Schwachpunkt, den zukünftige Medikamente anvisieren könnten, um das Fortschreiten von Leberkrebs zu verlangsamen oder zu stoppen.
Das Umfeld um einen Tumor
Krebs wächst nicht isoliert; er existiert in einer komplexen „Nachbarschaft“ aus Blutgefäßen, Stütz- und Immunzellen, die als Tumormikroumgebung bekannt ist. Bei Leberkrebs ist eine der häufigsten Immunzelltypen der tumorassoziierte Makrophage. Diese Zellen können verschiedene Rollen einnehmen: manche greifen Tumoren an, andere, die sogenannten M2‑Makrophagen, dämpfen Entzündungen und können am Ende dem Krebs helfen. Viele Studien haben gezeigt, dass Tumoren, in denen M2‑Zellen dominieren, tendenziell schneller wachsen, sich leichter ausbreiten und schlechter auf Therapien ansprechen. Das wirft eine wichtige Frage auf: Wie genau treiben diese helfenden Makrophagen das bösartige Verhalten von Leberkrebszellen voran?
Ein Enzym, das gefährliches Wachstum antreibt
Die Forschenden konzentrierten sich auf PYCR1, ein Enzym, das Zellen bei der Herstellung der Aminosäure Prolin unterstützt, einem wichtigen Bestandteil strukturgebender Proteine wie Kollagen und einer wichtigen Energiequelle für schnell teilende Zellen. Durch die Analyse von Patientendaten fanden sie heraus, dass die PYCR1‑Spiegel in Lebertumoren höher sind als im normalen Lebergewebe, und dass Patienten, deren Tumoren mehr PYCR1 und eine stärkere Infiltration durch M2‑Makrophagen aufweisen, tendenziell eine schlechtere Überlebensprognose haben. Das deutet darauf hin, dass PYCR1 eine entscheidende Verbindung zwischen dem veränderten Stoffwechsel der Tumorzellen und dem schädlichen Einfluss ihrer Immunumgebung sein könnte.
Wie Makrophagen Tumorzellen zum Ausbreiten anregen
Um diese Idee zu prüfen, kultivierte das Team Leberkrebszelllinien in Nährmedien, das aus M2‑Makrophagen gewonnen worden war. Unter diesen Bedingungen wurden die Krebszellen aggressiver: Sie bewegten sich schneller über künstliche „Wunden“, drangen leichter durch Membranen und zeigten Proteinveränderungen, die einen Übergang von einem stabilen, pflastersteinartigen epithelialen Zustand zu einem flexibleren, reisebereiten mesenchymalen Zustand signalisieren. Dieser Wechsel, bekannt als epithelial‑mesenchymale Transition, ist ein zentraler Schritt der Metastasierung. Als die Wissenschaftler mittels genetischer Werkzeuge PYCR1 in den Krebszellen herabregulierten, kehrten diese durch M2‑Zellen ausgelösten Effekte weitgehend um, und die Zellen wurden weniger beweglich und invasiv, was darauf hinweist, dass PYCR1 für die volle Wirkung der Makrophagen‑Signale erforderlich ist.
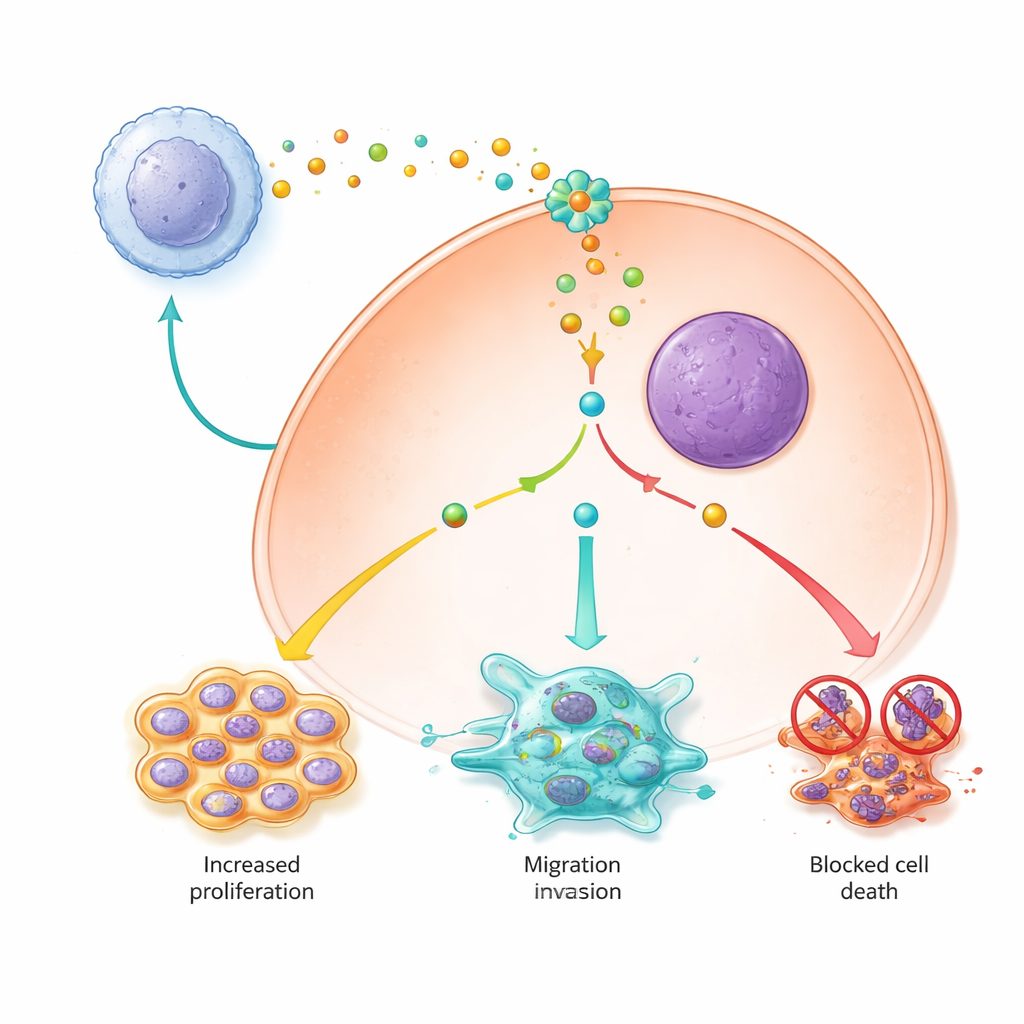
Das Überleben und die Teilung von Krebszellen erhalten
Die Studie zeigte außerdem, dass Signale von M2‑Makrophagen Leberkrebszellen helfen, am Leben zu bleiben und sich zu vermehren, indem sie wichtige Überlebenswege verändern. Krebszellen, die M2‑konditioniertem Medium ausgesetzt waren, teilten sich schneller, zeigten eine geringere Neigung zur programmierten Zellapoptose und waren weniger anfällig für eine neuere, eisenabhängige Form des Zelltods, genannt Ferroptose. Im Inneren der Zellen erwies sich PYCR1 als zentrales Schaltelement: Wenn es aktiv war, war der Signalweg JAK2/STAT3 stärker aktiviert, pro‑überlebensfördernde Proteine stiegen an und Proteine, die Ferroptose hemmen, waren erhöht, während schädliches Eisen und reaktive Moleküle niedrig gehalten wurden. Die Herunterregulierung von PYCR1 oder die Blockade der JAK‑Signalgebung mit einem niedermolekularen Inhibitor schwächte diese Kaskade ab, verlangsamte die Proliferation und stellte sowohl Apoptose als auch Ferroptose wieder her.
Was das für zukünftige Therapien bedeutet
In der Summe zeichnen die Ergebnisse PYCR1 als einen zentralen Unterstützer, der es Leberkrebszellen ermöglicht, die Hilfe von M2‑Makrophagen umfassend auszunutzen: Es fördert Wachstum, ermöglicht Formwandlung und Ausbreitung und schützt Zellen vor zwei Todesformen. Für Patientinnen und Patienten legt dies nahe, dass Wirkstoffe, die PYCR1 blockieren – besonders in Kombination mit Therapien, die tumorfördernde Makrophagen umprogrammieren oder reduzieren – den Leberkrebs an mehreren Fronten gleichzeitig angreifen könnten. Obwohl diese Experimente in Zellkulturen durchgeführt wurden und noch in Tiermodellen und klinischen Studien bestätigt werden müssen, heben sie PYCR1 und die Tumormikroumgebung als vielversprechende Ziele im Streben nach wirksameren Therapien gegen Leberkrebs hervor.
Zitation: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Schlüsselwörter: hepatozelluläres Karzinom, Tumormikroumgebung, Makrophagen, PYCR1, JAK2 STAT3