Clear Sky Science · it
Studio sugli effetti e sui meccanismi dei macrofagi M2 sul comportamento biologico delle cellule del carcinoma epatocellulare promosso da PYCR1
Perché questo studio sul cancro al fegato è importante
Il tumore primitivo del fegato, per lo più carcinoma epatocellulare, è uno dei tumori più letali a livello mondiale, in parte perché tende a diffondersi precocemente e a resistere alle terapie. Questo studio esamina un enzima metabolico poco conosciuto, PYCR1, e un gruppo di cellule immunitarie chiamate macrofagi per capire come i tumori epatici crescono, si diffondono e sfuggono alla morte cellulare. Svelando come questi attori cooperano all’interno del “quartiere” tumorale, il lavoro indica un nuovo punto debole che farmaci futuri potrebbero prendere di mira per rallentare o fermare il cancro al fegato.
Il quartiere intorno a un tumore
Il cancro non cresce in isolamento; vive in un complesso “quartiere” di vasi sanguigni, cellule di supporto e cellule immunitarie noto come microambiente tumorale. Nel cancro al fegato, uno dei tipi di cellule immunitarie più abbondanti è il macrofago associato al tumore. Queste cellule possono assumere diverse «personalità»: alcune attaccano i tumori, mentre altre, dette macrofagi di tipo M2, attenuano l’infiammazione e possono finire per aiutare il cancro. Molti studi hanno dimostrato che quando predominano le cellule M2, i tumori tendono a crescere più rapidamente, a diffondersi più facilmente e a rispondere peggio alle terapie. Questo ha sollevato una domanda importante: in che modo esattamente questi macrofagi di tipo «aiutante» spingono le cellule del carcinoma epatocellulare verso un comportamento più maligno?
Un enzima che alimenta una crescita pericolosa
I ricercatori si sono concentrati su PYCR1, un enzima che aiuta le cellule a sintetizzare l’amminoacido prolina, componente chiave di proteine strutturali come il collagene e importante carburante per cellule che si dividono rapidamente. Analizzando i dati dei pazienti, hanno scoperto che i livelli di PYCR1 sono più alti nei tumori del fegato rispetto al tessuto epatico normale, e che i pazienti i cui tumori presentano maggior espressione di PYCR1 e maggiore infiltrazione di macrofagi di tipo M2 tendono ad avere una sopravvivenza peggiore. Ciò suggerisce che PYCR1 potrebbe essere un collegamento cruciale tra il metabolismo alterato delle cellule tumorali e l’influenza dannosa del loro ambiente immunitario.
Come i macrofagi spingono le cellule tumorali a diffondersi
Per mettere alla prova questa idea, il gruppo ha coltivato linee cellulari di carcinoma epatico in piastre con il liquido raccolto da macrofagi di tipo M2. In queste condizioni, le cellule tumorali sono diventate più aggressive: si sono spostate più rapidamente attraverso “ferite” artificiali, hanno invaso le membrane più facilmente e hanno mostrato cambiamenti proteici che segnalano una transizione da uno stato epiteliale stabile e simile a un mosaico a uno stato mesenchimale più flessibile e predisposto alla migrazione. Questo switch, noto come transizione epitelio‑mesenchimale, è un passaggio chiave nella metastasi. Quando gli scienziati hanno abbassato i livelli di PYCR1 nelle cellule tumorali con strumenti genetici, questi effetti indotti dagli M2 sono stati in gran parte invertiti: le cellule sono diventate meno mobili e meno invasive, indicando che PYCR1 è necessario affinché i segnali dei macrofagi conferiscano pienamente potere alle cellule tumorali.
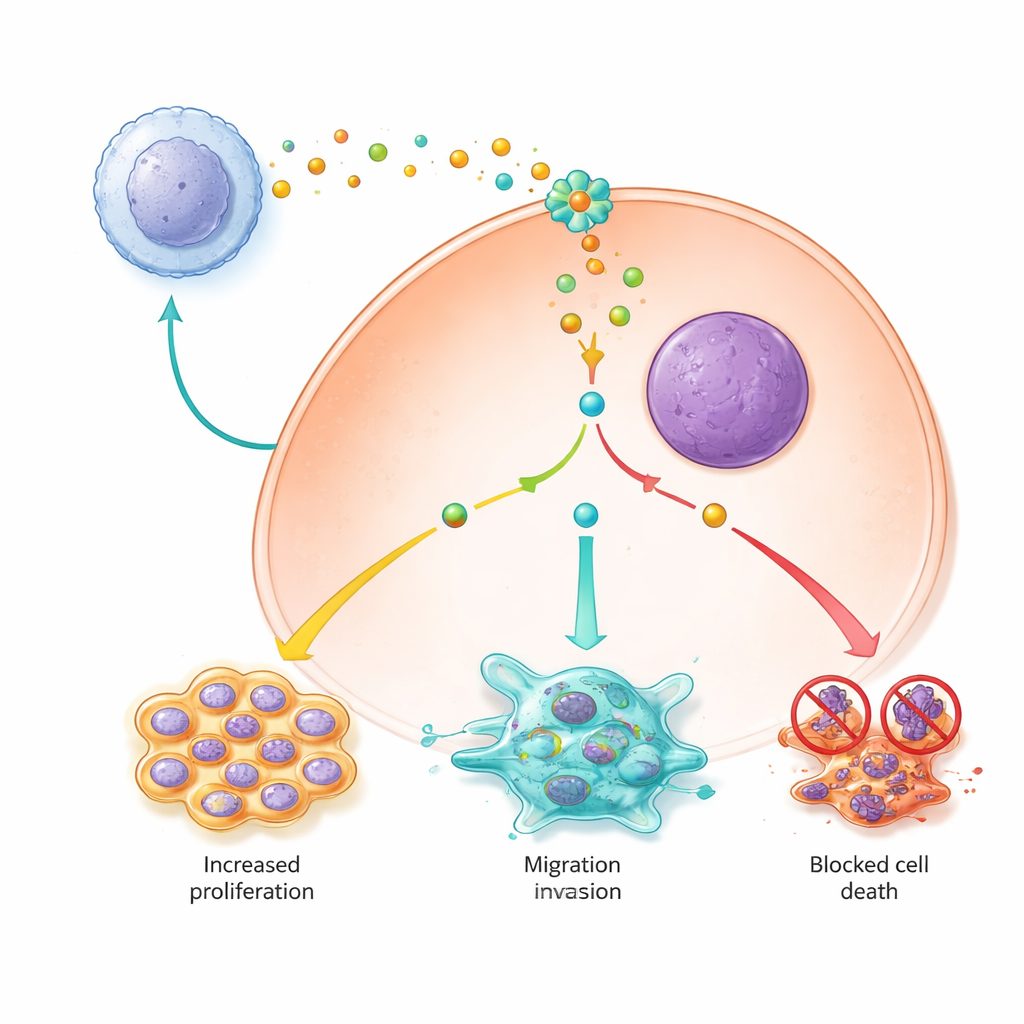
Mantenere le cellule tumorali vive e in proliferazione
Lo studio ha mostrato inoltre che i segnali dei macrofagi di tipo M2 aiutano le cellule del carcinoma epatocellulare a sopravvivere e a moltiplicarsi alterando vie chiave della sopravvivenza. Le cellule esposte a mezzo condizionato da M2 si dividevano più rapidamente, erano meno propense a subire la morte cellulare programmata e risultavano meno sensibili a una forma più recente di morte cellulare dipendente dal ferro chiamata ferroptosi. All’interno delle cellule, PYCR1 si è rivelato un interruttore centrale: quando era attivo, una via di segnalazione importante chiamata JAK2/STAT3 risultava più fortemente attivata, aumentavano proteine pro‑sopravvivenza e si alzavano i livelli di proteine che bloccano la ferroptosi, mentre ferro dannoso e specie reattive venivano mantenute basse. L’abbattimento di PYCR1 o il blocco della segnalazione JAK con un inibitore piccolo molecolare indebolivano questa cascata, rallentavano la proliferazione e ripristinavano sia l’apoptosi sia la ferroptosi.
Cosa significa questo per i trattamenti futuri
Nel complesso, i risultati delineano PYCR1 come un facilitatore principale che permette alle cellule del cancro al fegato di sfruttare appieno il supporto dei macrofagi di tipo M2: potenzia la crescita, favorisce il cambiamento morfologico e la diffusione, e protegge le cellule da due forme di morte. Per i pazienti, questo suggerisce che farmaci progettati per bloccare PYCR1, specialmente se combinati con terapie che riprogrammano o depletano i macrofagi che supportano il tumore, potrebbero attaccare il carcinoma epatocellulare su più fronti contemporaneamente. Sebbene questi esperimenti siano stati condotti in colture cellulari e debbano ancora essere confermati in modelli animali e studi clinici, evidenziano PYCR1 e il microambiente tumorale come bersagli promettenti nella ricerca di terapie più efficaci contro il cancro del fegato.
Citazione: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Parole chiave: carcinoma epatocellulare, microambiente tumorale, macrofagi, PYCR1, JAK2 STAT3