Clear Sky Science · pt
Estudo sobre os efeitos e mecanismos dos macrófagos M2 no comportamento biológico de células de carcinoma hepatocelular promovido por PYCR1
Por que este estudo sobre câncer de fígado é importante
O câncer primário de fígado, majoritariamente o carcinoma hepatocelular, está entre os cânceres mais letais do mundo, em parte porque costuma metastizar precocemente e resistir aos tratamentos. Este estudo examina uma enzima metabólica pouco conhecida, PYCR1, e um grupo de células imunes chamadas macrófagos para entender como tumores hepáticos crescem, se espalham e escapam da morte celular. Ao desvendar como esses atores cooperam no entorno do tumor, o trabalho aponta para uma nova vulnerabilidade que fármacos futuros poderiam explorar para retardar ou interromper o câncer de fígado.
O entorno de um tumor
O câncer não cresce isoladamente; ele vive em um “bairro” complexo de vasos sanguíneos, células de suporte e células imunes conhecido como microambiente tumoral. No câncer de fígado, um dos tipos de célula imune mais abundantes é o macrófago associado ao tumor. Essas células podem assumir personalidades diferentes: algumas atacam o tumor, enquanto outras, chamadas macrófagos do tipo M2, atenuam a inflamação e podem acabar ajudando o câncer. Muitos estudos mostraram que quando as células do tipo M2 prevalecem, os tumores tendem a crescer mais rápido, a metastizar com mais facilidade e a responder pior ao tratamento. Isso levanta uma questão importante: como exatamente esses macrófagos “auxiliares” empurram as células do câncer de fígado para um comportamento mais maligno?
Uma enzima que alimenta um crescimento perigoso
Os pesquisadores focaram em PYCR1, uma enzima que ajuda as células a sintetizar o aminoácido prolina, um componente chave de proteínas estruturais como o colágeno e um combustível importante para células que se dividem rapidamente. Ao analisar dados de pacientes, eles encontraram níveis mais altos de PYCR1 em tumores hepáticos do que em tecido hepático normal, e observaram que pacientes cujos tumores apresentam maior expressão de PYCR1 e maior infiltração de macrófagos do tipo M2 tendem a ter pior sobrevida. Isso sugeriu que PYCR1 pode ser um elo crucial entre o metabolismo alterado das células tumorais e a influência nociva do seu entorno imune.
Como os macrófagos impulsionam a disseminação tumoral
Para testar essa ideia, a equipe cultivou linhagens de células de câncer de fígado em pratos com meio condicionado coletado de macrófagos do tipo M2. Nestas condições, as células cancerosas tornaram‑se mais agressivas: migraram mais rápido através de “feridas” artificiais, invadiram membranas com mais facilidade e exibiram mudanças em proteínas que sinalizam a transição de um estado epitelial estável e em mosaico para um estado mesenquimal mais flexível e apto à migração. Essa mudança, conhecida como transição epitélio‑mesênquima, é um passo chave na metástase. Quando os cientistas empregaram ferramentas genéticas para reduzir os níveis de PYCR1 nas células tumorais, esses efeitos induzidos por M2 foram em grande parte revertidos, e as células ficaram menos móveis e menos invasivas, indicando que PYCR1 é necessário para que os sinais dos macrófagos potencializem plenamente as células tumorais.
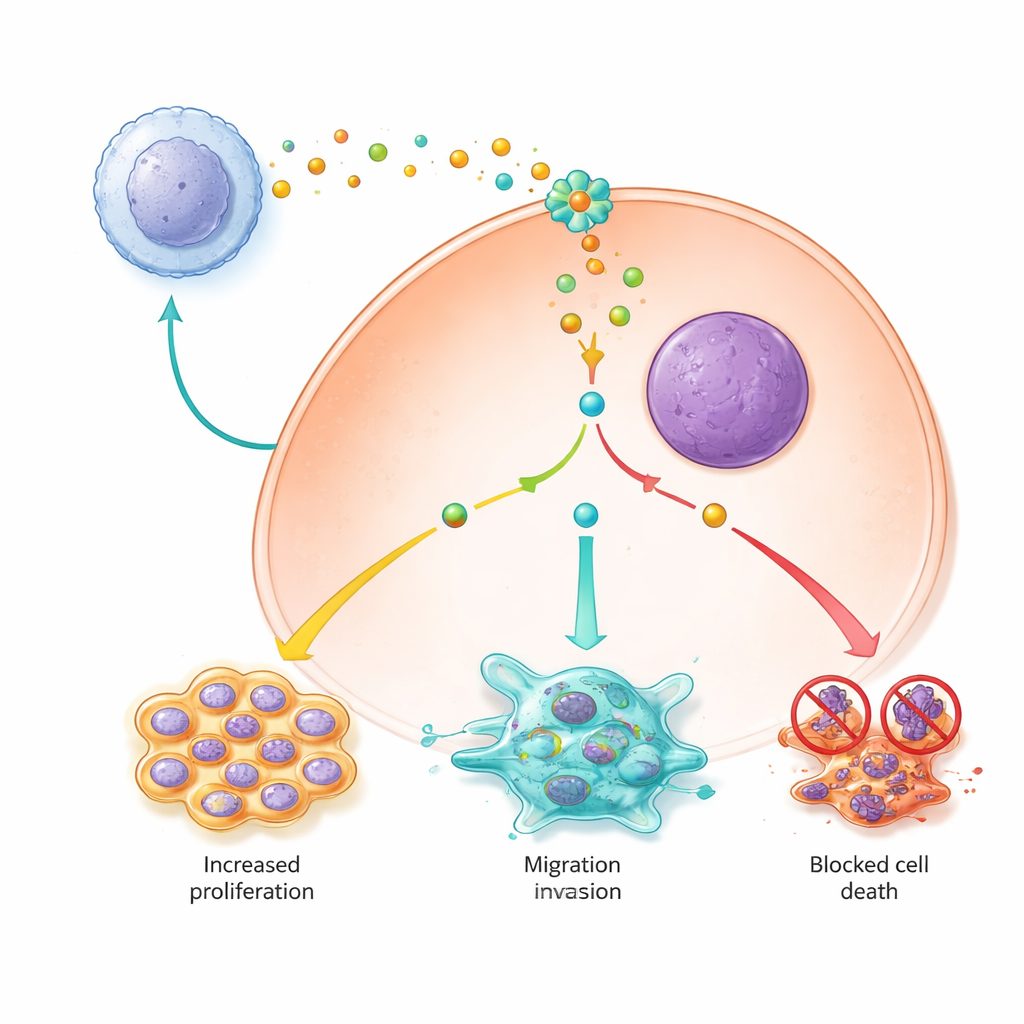
Manter as células cancerosas vivas e em divisão
O estudo também mostrou que os sinais dos macrófagos do tipo M2 ajudam as células de câncer de fígado a sobreviver e se multiplicar ao alterar vias celulares chave de sobrevivência. Células expostas ao meio condicionado por M2 dividiram‑se mais rapidamente, apresentaram menor tendência à morte celular programada e foram menos suscetíveis a uma forma mais recente de morte celular dependente de ferro chamada ferroptose. Dentro das células, PYCR1 revelou‑se um comutador central: quando ativo, uma via de sinalização major chamada JAK2/STAT3 apresentava maior ativação, proteínas pró‑sobrevivência aumentavam, e proteínas que bloqueiam a ferroptose eram elevadas enquanto o ferro livre e moléculas reativas prejudiciais eram mantidos em níveis baixos. Reduzir a expressão de PYCR1 ou bloquear a sinalização JAK com um inibidor de pequena molécula enfraqueceu essa cascata, desacelerou a proliferação e restaurou tanto a apoptose quanto a ferroptose.
O que isso significa para tratamentos futuros
Em conjunto, os achados retratam PYCR1 como um facilitador mestre que permite às células do câncer de fígado explorar plenamente o suporte dos macrófagos do tipo M2: ele impulsiona o crescimento, facilita a mudança de forma e a disseminação, e protege as células contra duas formas de morte. Para pacientes, isso sugere que fármacos projetados para bloquear PYCR1, especialmente quando combinados com tratamentos que reprogramem ou depletem macrófagos que suportam o tumor, poderiam atacar o câncer de fígado em várias frentes simultaneamente. Embora esses experimentos tenham sido realizados em culturas celulares e ainda precisem ser confirmados em modelos animais e estudos clínicos, eles destacam PYCR1 e o microambiente tumoral como alvos promissores na busca por terapias mais eficazes contra o câncer de fígado.
Citação: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Palavras-chave: carcinoma hepatocelular, microambiente tumoral, macrófagos, PYCR1, JAK2 STAT3