Clear Sky Science · es
Estudio sobre los efectos y mecanismos de los macrófagos M2 en el comportamiento biológico promovido por PYCR1 en células de carcinoma hepatocelular
Por qué importa este estudio sobre el cáncer de hígado
El cáncer primario de hígado, en su mayoría carcinoma hepatocelular, es uno de los cánceres más letales del mundo, en parte porque con frecuencia se disemina pronto y resiste los tratamientos. Este estudio examina una enzima metabólica poco conocida, PYCR1, y un grupo de células inmunitarias llamadas macrófagos para entender cómo los tumores hepáticos crecen, se diseminan y evaden la muerte celular. Al revelar cómo estos actores cooperan dentro del vecindario tumoral, el trabajo señala una nueva vulnerabilidad que fármacos futuros podrían explotar para frenar o detener el cáncer de hígado.
El vecindario alrededor de un tumor
El cáncer no crece aislado; vive en un “vecindario” complejo de vasos sanguíneos, células de sostén y células inmunitarias conocido como microambiente tumoral. En el cáncer de hígado, uno de los tipos de células inmunitarias más abundantes son los macrófagos asociados al tumor. Estas células pueden adoptar distintas personalidades: algunas atacan al tumor, mientras que otras, llamadas macrófagos de tipo M2, apaciguan la inflamación y pueden terminar favoreciendo al cáncer. Numerosos estudios han mostrado que cuando predominan las células de tipo M2, los tumores tienden a crecer más rápido, diseminarse con mayor facilidad y responder peor al tratamiento. Esto planteó una pregunta importante: ¿cómo, exactamente, empujan estos macrófagos “colaboradores” a las células del cáncer de hígado hacia un comportamiento más maligno?
Una enzima que alimenta el crecimiento peligroso
Los investigadores se centraron en PYCR1, una enzima que ayuda a las células a sintetizar el aminoácido prolina, un componente clave de proteínas estructurales como el colágeno y un combustible importante para células que se dividen rápidamente. Al analizar datos de pacientes, encontraron que los niveles de PYCR1 son más altos en tumores hepáticos que en tejido hepático normal, y que los pacientes cuyos tumores muestran más PYCR1 y mayor infiltración de macrófagos de tipo M2 tienden a tener una supervivencia peor. Esto sugirió que PYCR1 podría ser un vínculo crucial entre el metabolismo alterado de las células tumorales y la influencia perjudicial de su entorno inmunitario.
Cómo los macrófagos impulsan la diseminación tumoral
Para poner a prueba esta idea, el equipo cultivó líneas celulares de cáncer de hígado en platos con líquido recogido de macrófagos de tipo M2. En estas condiciones, las células cancerosas se volvieron más agresivas: se desplazaron más rápido a través de “heridas” artificiales, invadieron membranas con mayor facilidad y mostraron cambios en proteínas que señalan un cambio de un estado epitelial estable y parecido a un empedrado a un estado mesenquimal más flexible y apto para desplazarse. Este cambio, conocido como transición epitelio‑mesenquimal (EMT), es un paso clave en la metástasis. Cuando los científicos usaron herramientas genéticas para reducir los niveles de PYCR1 en las células tumorales, estos efectos inducidos por M2 se invirtieron en gran medida, y las células se volvieron menos móviles y menos invasivas, lo que indica que PYCR1 es necesario para que las señales de los macrófagos potencien plenamente a las células tumorales.
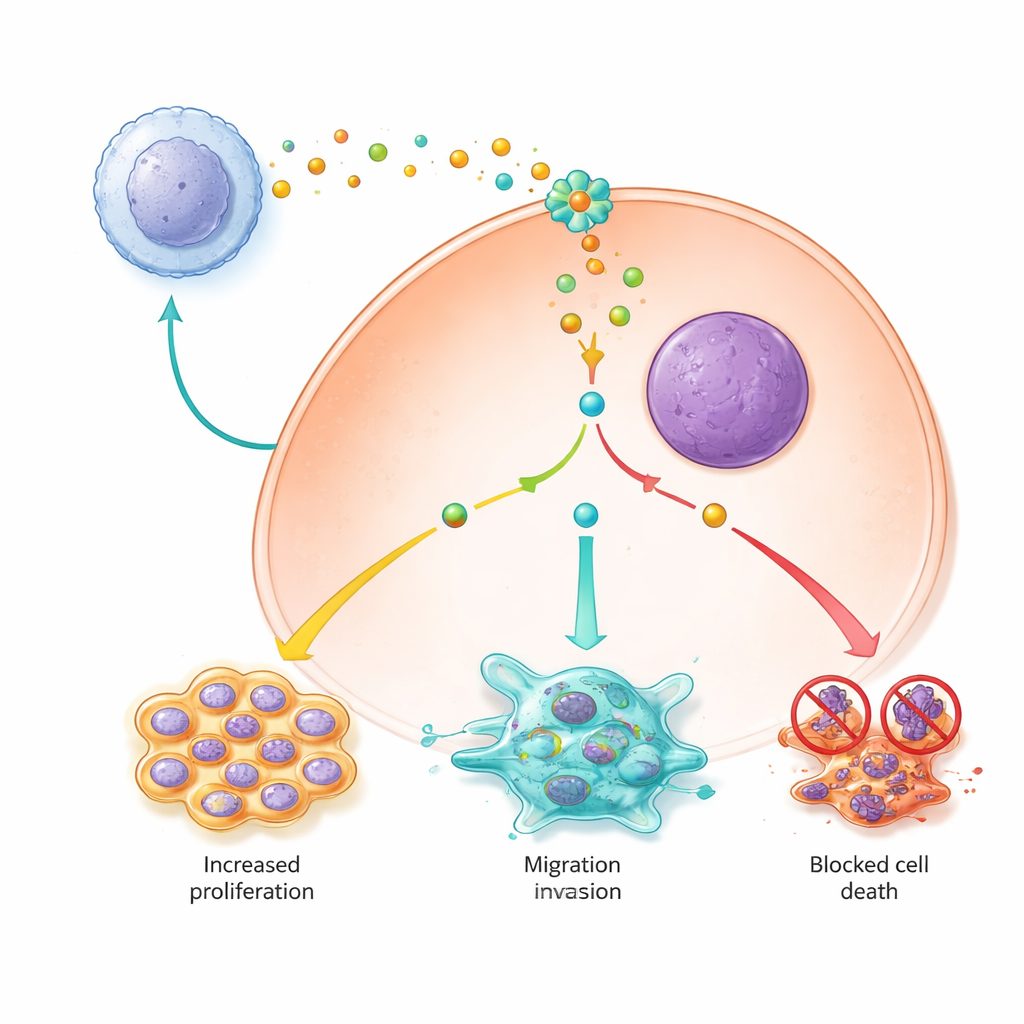
Mantener vivas y proliferando a las células cancerosas
El estudio también mostró que las señales de los macrófagos de tipo M2 ayudan a las células de cáncer de hígado a mantenerse vivas y multiplicarse al alterar vías clave de supervivencia. Las células expuestas al medio condicionado por M2 se dividían más rápido, eran menos propensas a sufrir muerte celular programada y presentaban menos probabilidad de un tipo más reciente de muerte celular dependiente del hierro llamado ferroptosis. Dentro de las células, PYCR1 resultó ser un interruptor central: cuando estaba activo, una vía de señalización principal llamada JAK2/STAT3 se activaba con mayor intensidad, aumentaban proteínas pro‑supervivencia y se elevaban proteínas que bloquean la ferroptosis, mientras que los niveles de hierro dañino y de especies reactivas se mantenían bajos. La reducción de PYCR1 o el bloqueo de la señalización JAK con un inhibidor de pequeña molécula debilitó esta cascada, frenó la proliferación y restauró tanto la apoptosis como la ferroptosis.
Qué significa esto para tratamientos futuros
En conjunto, los hallazgos presentan a PYCR1 como un colaborador maestro que permite a las células de carcinoma hepatocelular aprovechar por completo el apoyo de los macrófagos de tipo M2: potencia el crecimiento, facilita el cambio morfológico y la diseminación, y protege a las células de dos formas de muerte. Para los pacientes, esto sugiere que fármacos diseñados para bloquear PYCR1, especialmente combinados con tratamientos que reprogramen o depleten a los macrófagos que apoyan al tumor, podrían atacar el cáncer de hígado en varias frentes a la vez. Aunque estos experimentos se realizaron en cultivos celulares y aún deben confirmarse en modelos animales y estudios clínicos, ponen de relieve a PYCR1 y al microambiente tumoral como objetivos prometedores en la búsqueda de terapias más efectivas contra el cáncer de hígado.
Cita: Jin, X., Hou, Y., Guo, J. et al. Study on the effects and mechanisms of M2 macrophages on PYCR1-promoted biological behavior of hepatocellular carcinoma cells. Sci Rep 16, 13716 (2026). https://doi.org/10.1038/s41598-026-40817-8
Palabras clave: carcinoma hepatocelular, microambiente tumoral, macrófagos, PYCR1, JAK2 STAT3