Clear Sky Science · zh
通过调节Bhmt的肝细胞Brca1的矛盾促癌作用
当抗癌守护者反过来行动时
大多数人将像BRCA1这样的基因视为防癌的守护者。本研究对肝脏情形提出了相反的观点。研究人员展示了在某些条件下,肝细胞中正常的BRCA1活性反而能助长肝脏肿瘤生长,而关闭它则能保护免受癌变。理解这一出人意料的反转,或能揭示预防或治疗这一全球最致命癌症之一的新途径。
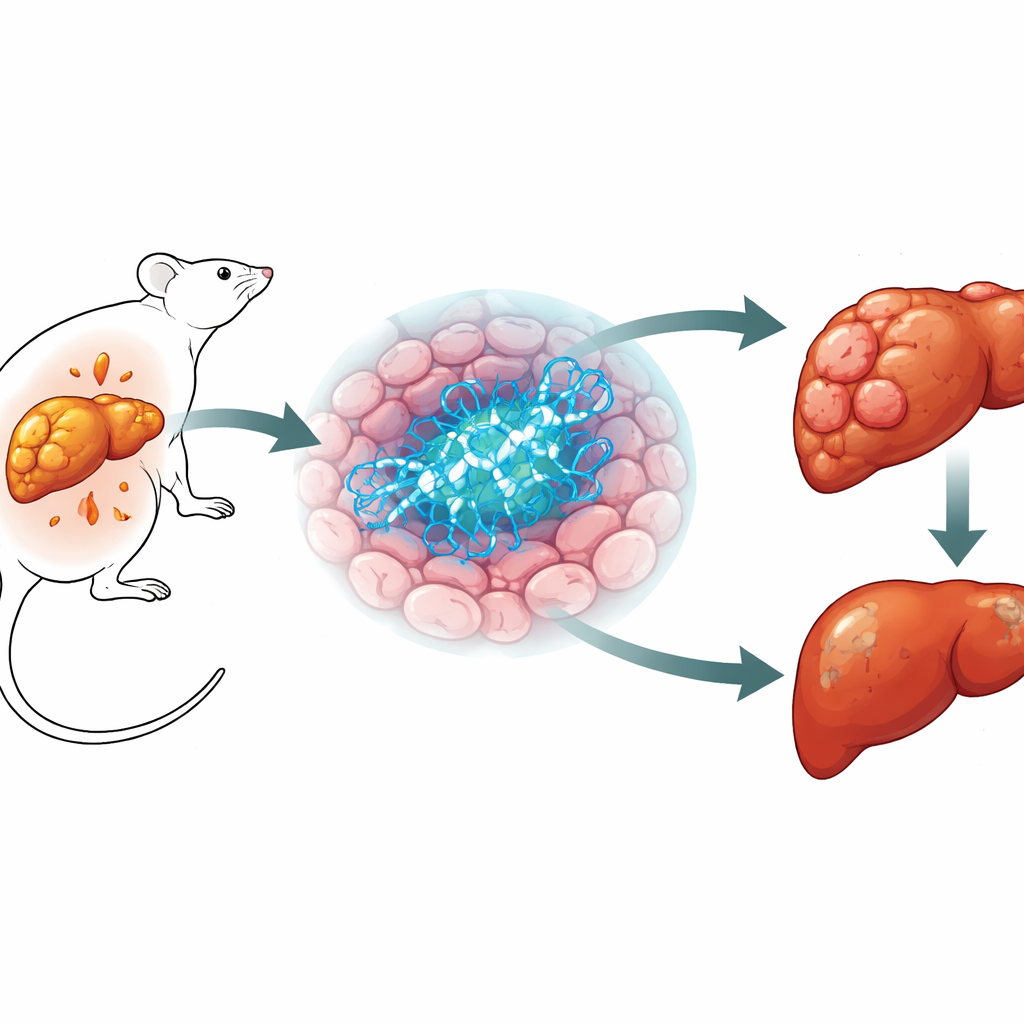
日益严重的致命性肝癌
肝癌,尤其是肝细胞癌,已经是最常见且致死率极高的癌症之一,而且负担仍在增加。肥胖和2型糖尿病相关的一种病况是一个主要驱动因素,在该病况中脂肪在肝脏内逐渐积累,可能进展为肝纤维化并最终演变为癌症。科学家们知道代谢与癌症紧密相连,但许多具体的分子参与者仍不清楚。由于BRCA1长期被认为是在乳腺和卵巢癌中的肿瘤抑制基因,并且与细胞处理脂类和糖类的方式有关,作者们探讨BRCA1是否会影响肝脏代谢及肝癌发生。
在肝细胞中关闭一位守护者
研究团队构建了仅在肝细胞中删除BRCA1的小鼠模型,身体其他部位不受影响。正如BRCA1在修复受损DNA中的传统作用所预期的,这些肝细胞显示出更多的DNA断裂。但动物的整体健康状况却讲述了不同的故事。在高脂饮食下,缺乏肝脏BRCA1的小鼠肝内脂肪积累更少,对糖代谢的耐受性也优于正常小鼠,尽管体重相近。最显著的是,当这些动物暴露于一种可靠产生肝肿瘤的致癌化学物质时,缺少肝脏BRCA1的动物比正常同窝仔发育出更少且更小的肿瘤。这种保护在两种不同的肿瘤模型中都出现,表明BRCA1在肝细胞中的存在反常地可能有利于肿瘤生长。
揭示一个隐蔽的代谢通路
为了解BRCA1缺失如何保护肝脏免受癌变,研究人员检查了数千个单个肝细胞细胞核中哪些基因处于活跃状态。他们发现有一个基因Bhmt在BRCA1缺失时始终表现出较低的活性。BHMT是一种几乎只在肝脏中发现的酶,位于蛋氨酸和胆碱代谢的交汇点——这些通路为DNA提供构件、支持分子化学标记并为膜脂合成提供原料。基因集分析显示,许多小分子和有机酸通路,尤其是与一碳代谢和胆碱利用相关的通路,在BRCA1缺陷的肝细胞中被下调,且与肝肿瘤形成相关的表达特征也减少。当团队在人的肝癌细胞中沈默BRCA1时,同样观察到BHMT活性下降,提示两基因间存在直接联系。
损伤过多,但肿瘤燃料不足
作者随后深入研究BRCA1与BHMT在功能上的相互作用。在人肝癌细胞中,关闭BRCA1会增加DNA断裂,关闭BHMT也会如此。当两者同时被抑制时,DNA损伤更加累积。在这些细胞暴露于照射后,BRCA1缺失显著增强了细胞死亡,且两基因共同缺失仍维持这种增强的易损性。与此同时,代谢方面的证据也浮出水面。胆碱水平——其在许多癌症中积累是一个公认标志——在正常小鼠的肝肿瘤中升高,但在BRCA1缺失小鼠的肿瘤和血液中则被抑制。将胆碱导入膜脂的酶也减少,广泛的代谢物谱分析显示磷脂酰胆碱、甘氨酸和多胺的生成受损,而这些分子对快速分裂的细胞都很重要。综合来看,这些变化表明缺少BRCA1时,肝细胞既积累致命的DNA损伤,又失去肿瘤生长所需的关键代谢燃料。
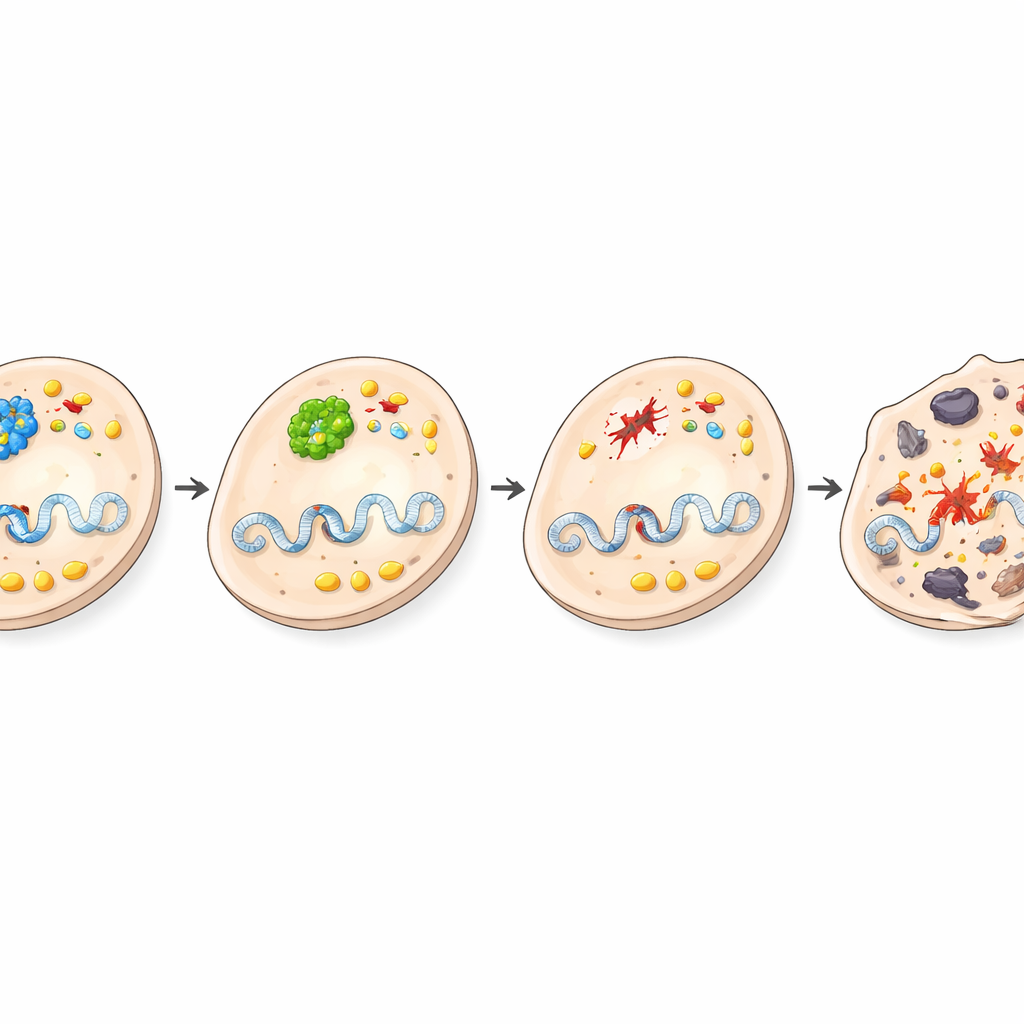
这一反转对癌症意味着什么
这项工作揭示了BRCA1在身体其他部位出名的抑癌作用之外,在肝脏中通过支持BHMT活性和以胆碱为中心的代谢,反而可能具有促癌效果。当BRCA1被特异性地从肝细胞移除时,BHMT活性下降,DNA损伤变得不可承受,胆碱相关通路被压抑,受损细胞倾向于死亡而非演变为肿瘤。该研究突出了同一基因可依据组织和代谢背景扮演相反角色的事实,并指出一碳代谢与胆碱代谢是有前景的肝癌预防或治疗靶点。
引用: Ghebreselassie, M., Park, Y.J., Nakib, D. et al. Paradoxical oncogenic effects of hepatic Brca1 through modulating Bhmt. Sci Rep 16, 13479 (2026). https://doi.org/10.1038/s41598-026-39581-6
关键词: 肝癌, BRCA1, 胆碱代谢, 一碳代谢, 肝细胞癌