Clear Sky Science · nl
Paradoxale oncogene effecten van hepatische Brca1 via modulatatie van Bhmt
Wanneer kankerveiligheid zich omkeert
De meesten van ons zien genen zoals BRCA1 als bewakers die kanker voorkomen. Deze studie keert dat idee echter om voor de lever. De onderzoekers tonen aan dat onder bepaalde omstandigheden normale BRCA1-activiteit in levercellen de groei van levertumoren juist kan bevorderen, terwijl het uitschakelen ervan juist bescherming tegen kanker kan bieden. Het begrijpen van deze onverwachte wending kan nieuwe manieren onthullen om een van de dodelijkste kankers wereldwijd te voorkomen of te behandelen.
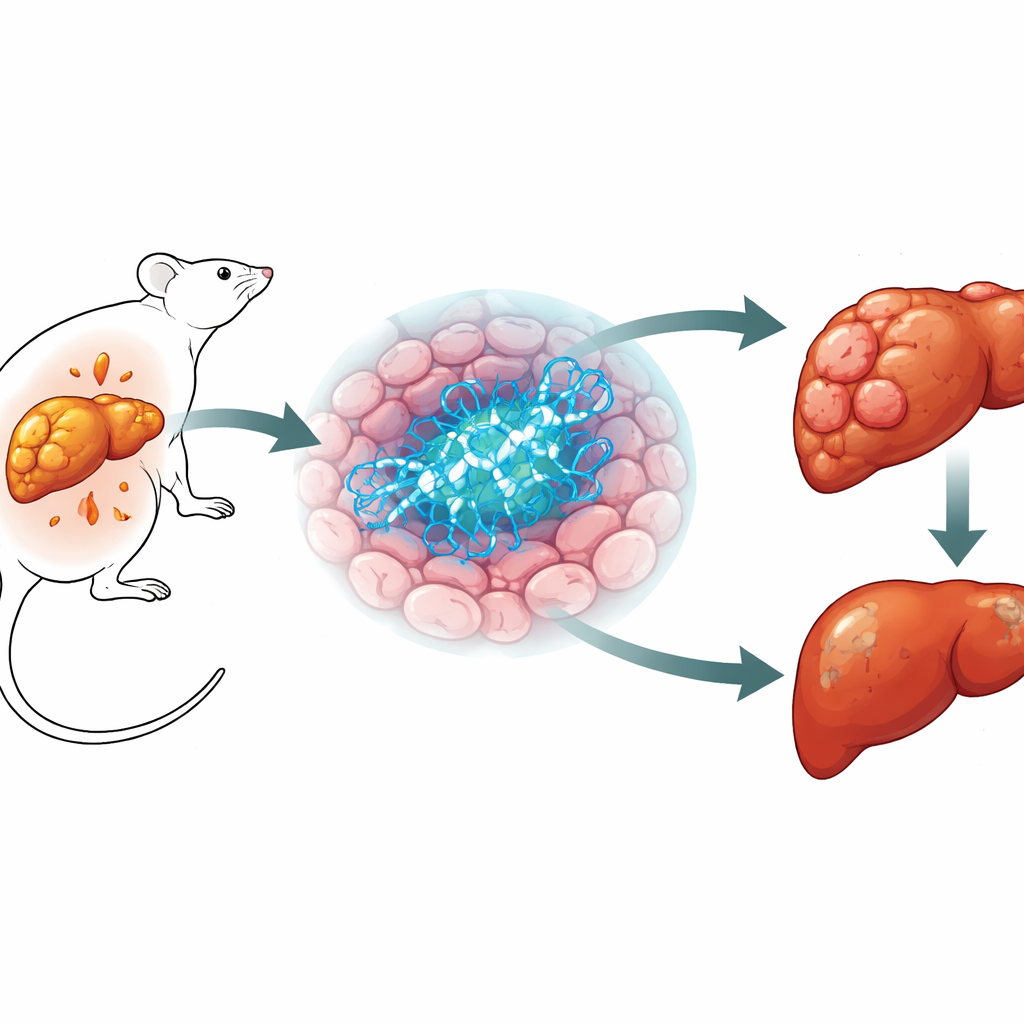
Een dodelijke leverkanker in opkomst
Leverkanker, en dan vooral hepatocellulair carcinoom, is al een van de meest voorkomende en dodelijke kankers, en de last blijft toenemen. Een belangrijke drijfveer is een aandoening die samenhangt met obesitas en type 2-diabetes, waarbij vet zich geleidelijk in de lever ophoopt en kan uitmonden in littekenvorming en uiteindelijk kanker. Wetenschappers weten dat metabolisme en kanker nauw met elkaar verbonden zijn, maar veel van de specifieke moleculaire spelers blijven onduidelijk. Omdat BRCA1 al lang erkend is als een tumorsuppressorgen bij borst- en eierstokkanker, en ook gekoppeld is aan hoe cellen vetten en suikers verwerken, vroegen de auteurs zich af of BRCA1 zowel het levermetabolisme als leverkanker zou kunnen beïnvloeden.
Een bewaker uitschakelen in levercellen
Het team creëerde muizen waarin BRCA1 alleen in levercellen werd verwijderd, terwijl de rest van het lichaam onaangetast bleef. Zoals te verwachten was vanwege de klassieke rol van BRCA1 in het repareren van beschadigd DNA, vertoonden deze levercellen meer DNA-breuken. Maar de algemene gezondheid van de dieren vertelde een ander verhaal. Wanneer ze een vetrijk dieet kregen, stapelden muizen zonder BRCA1 in hun lever minder vet in de lever op en gingen ze beter om met suiker dan normale muizen, ondanks een vergelijkbaar lichaamsgewicht. Het meest opvallend was dat wanneer de dieren werden blootgesteld aan een kankerverwekkend chemisch middel dat betrouwbaar levertumoren produceert, de dieren zonder BRCA1 in hun levercellen veel minder en kleinere tumoren ontwikkelden dan hun normale nestgenoten. Deze bescherming verscheen in twee verschillende tumormodellen, wat aangeeft dat de aanwezigheid van BRCA1 in levercellen paradoxaal genoeg tumorgroei kan bevorderen.
Een verborgen metabool pad blootleggen
Om te begrijpen hoe het verlies van BRCA1 de lever tegen kanker zou kunnen beschermen, onderzochten de onderzoekers welke genen actief waren in duizenden individuele levercelkernen. Ze ontdekten dat één gen, Bhmt, consistent minder actief was wanneer BRCA1 ontbrak. BHMT is een enzym dat bijna uitsluitend in de lever voorkomt en zich bevindt op een kruispunt van methionine- en cholinemetabolisme — routes die bouwstenen voor DNA leveren, chemische etikettering van moleculen ondersteunen en de productie van membraanlipiden voeden. Genensetanalyses toonden aan dat veel routes voor kleine moleculen en organische zuren, vooral die gekoppeld aan een-koolstofmetabolisme en cholinegebruik, afgeremd waren in BRCA1-deficiënte hepatocyten, en handtekeningen die geassocieerd zijn met levertumorvorming waren ook verminderd. Dezelfde daling in BHMT-activiteit verscheen toen het team BRCA1 in menselijke leverkankercellen stillegde, wat wijst op een directe verbinding tussen de twee genen.
Te veel schade, te weinig brandstof voor tumoren
De auteurs zochten vervolgens dieper naar hoe BRCA1 en BHMT functioneel met elkaar omgaan. In menselijke leverkankercellen leidde het uitschakelen van BRCA1 tot meer DNA-breuken, en het uitschakelen van BHMT deed dat ook. Wanneer beide tegelijk werden onderdrukt, stapelden DNA-schade en breuken zich nog meer op. Nadat deze cellen werden blootgesteld aan bestraling, versterkte het verlies van BRCA1 de celdood sterk, en gecombineerd verlies van beide genen hield deze verhoogde kwetsbaarheid in stand. Tegelijkertijd kwam de metabole kant van het verhaal naar voren. Choline-niveaus — een stof waarvan de ophoping een erkend kenmerk is van veel kankers — stegen in levertumoren van normale muizen maar waren geremd in tumoren en bloed van BRCA1-deficiënte muizen. Enzymen die choline naar membraanlipiden leiden, waren ook verminderd, en brede metabolietprofilering toonde verstoorde productie van fosfatidylcholine, glycine en polyaminen, allemaal belangrijk voor snel delende cellen. Samen suggereren deze veranderingen dat zonder BRCA1 levercellen zowel dodelijke DNA-schade ophopen als de toegang tot belangrijke metabole brandstof verliezen die nodig is voor tumorgroei.
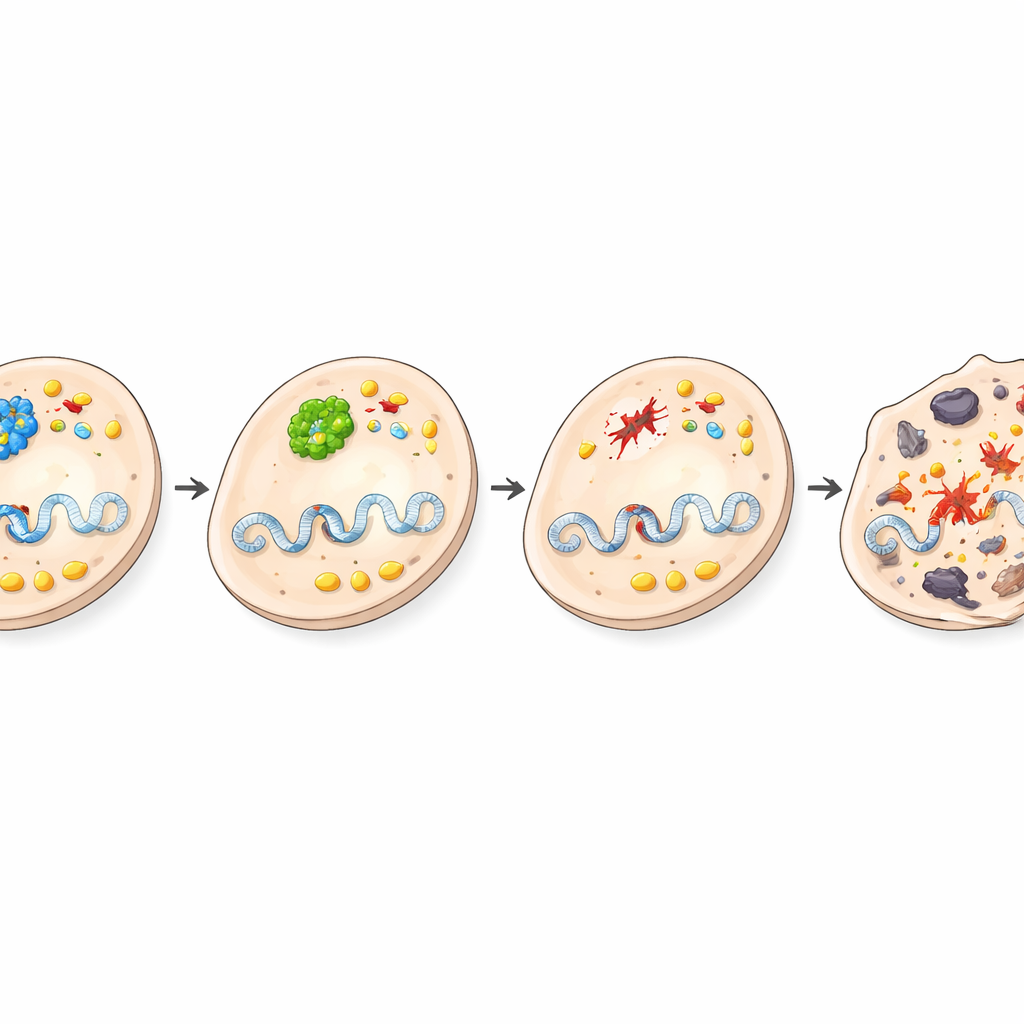
Wat deze wending betekent voor kanker
Dit werk laat zien dat BRCA1, beroemd als tumorsuppressor elders in het lichaam, in de lever juist tumorpromotende effecten kan hebben door BHMT-activiteit en choline-gecentreerd metabolisme te ondersteunen. Wanneer BRCA1 specifiek uit levercellen wordt verwijderd, daalt BHMT-activiteit, wordt DNA-schade overweldigend, worden choline-gerelateerde paden gedempt en sterven beschadigde cellen in plaats van dat ze uitgroeien tot tumoren. De studie benadrukt hoe hetzelfde gen tegengestelde rollen kan vervullen afhankelijk van weefsel en metabole context, en wijst op een-koolstof- en cholinemetabolisme als veelbelovende doelen voor nieuwe strategieën ter preventie of behandeling van leverkanker.
Bronvermelding: Ghebreselassie, M., Park, Y.J., Nakib, D. et al. Paradoxical oncogenic effects of hepatic Brca1 through modulating Bhmt. Sci Rep 16, 13479 (2026). https://doi.org/10.1038/s41598-026-39581-6
Trefwoorden: leverkanker, BRCA1, cholinemetabolisme, een‑koolstofmetabolisme, hepatocellulair carcinoom