Clear Sky Science · it
Effetti oncogeni paradossali di BRCA1 epatico tramite la modulazione di Bhmt
Quando la protezione dal cancro si comporta al contrario
La maggior parte di noi considera geni come BRCA1 come guardiani che prevengono il cancro. Questo studio capovolge quell’idea per il fegato. I ricercatori mostrano che, in certe condizioni, l’attività normale di BRCA1 nelle cellule epatiche può effettivamente favorire la crescita dei tumori al fegato, mentre la sua inattivazione può proteggere dal cancro. Comprendere questo sorprendente paradosso potrebbe rivelare nuovi modi per prevenire o trattare uno dei tumori più letali a livello globale.
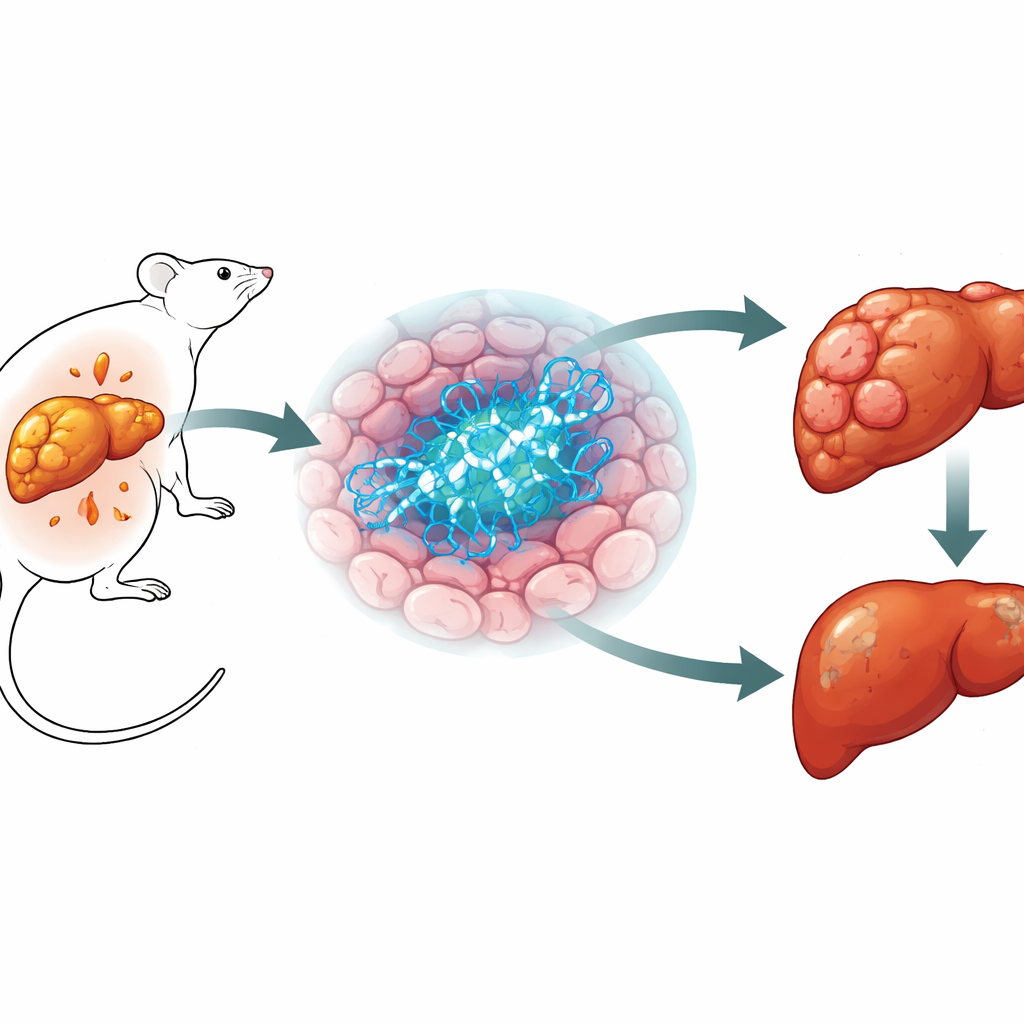
Un cancro al fegato mortale in aumento
Il cancro del fegato, in particolare il carcinoma epatocellulare, è già uno dei tumori più comuni e letali, e il suo impatto continua a crescere. Un fattore chiave è una condizione legata all’obesità e al diabete di tipo 2, in cui il grasso si accumula lentamente nel fegato e può progredire fino alla fibrosi e infine al cancro. Gli scienziati sanno che metabolismo e cancro sono strettamente connessi, ma molte delle singole componenti molecolari restano poco chiare. Poiché BRCA1 è stato a lungo riconosciuto come gene oncosoppressore in tumori della mammella e dell’ovaio, ed è anche collegato al modo in cui le cellule gestiscono grassi e zuccheri, gli autori si sono chiesti se BRCA1 potesse influenzare sia il metabolismo epatico sia il cancro del fegato.
Spegnere un guardiano nelle cellule del fegato
Il gruppo ha creato topi in cui BRCA1 è stato rimosso solo dalle cellule epatiche, lasciando il resto dell’organismo intatto. Come previsto dal ruolo classico di BRCA1 nella riparazione del DNA danneggiato, queste cellule epatiche hanno mostrato più rotture nel DNA. Ma la salute complessiva degli animali racconta una storia diversa. Alimentati con una dieta ricca di grassi, i topi privi di BRCA1 nel fegato accumulavano meno grasso epatico e gestivano meglio gli zuccheri rispetto ai topi normali, pur avendo un peso corporeo simile. Ancora più sorprendente, quando gli animali sono stati esposti a una sostanza chimica cancerogena che produce in modo affidabile tumori al fegato, quelli senza BRCA1 nelle cellule epatiche hanno sviluppato molti meno tumori e di dimensioni inferiori rispetto ai fratelli normali. Questa protezione è emersa in due diversi modelli tumorali, mostrando che la presenza di BRCA1 nelle cellule epatiche può, paradossalmente, favorire la crescita tumorale.
Scoprire una via metabolica nascosta
Per capire come la perdita di BRCA1 potesse proteggere il fegato dal cancro, i ricercatori hanno esaminato quali geni erano attivi in migliaia di singoli nuclei cellulari epatici. Hanno scoperto che un gene, Bhmt, si distingueva per essere costantemente meno attivo quando BRCA1 mancava. BHMT è un enzima quasi esclusivamente presente nel fegato che si trova all’incrocio tra il metabolismo della metionina e della colina—vie che forniscono mattoni per il DNA, supportano la marcatura chimica delle molecole e alimentano la produzione di lipidi di membrana. Le analisi di insiemi genici hanno rivelato che molte vie dei piccoli metaboliti e degli acidi organici, in particolare quelle legate al metabolismo a un carbonio e all’impiego della colina, erano attenuate negli epatociti privi di BRCA1, e anche le firme associate alla formazione di tumori epatici risultavano ridotte. La stessa diminuzione dell’attività di BHMT è apparsa quando il team ha silenziato BRCA1 in cellule tumorali epatiche umane, suggerendo una connessione diretta tra i due geni.
Troppo danno, troppo poco carburante per i tumori
Gli autori hanno poi approfondito come BRCA1 e BHMT interagiscano funzionalmente. In cellule tumorali epatiche umane, lo spegnimento di BRCA1 ha aumentato le rotture del DNA, e anche lo spegnimento di BHMT le ha accentuate. Quando entrambi sono stati soppressi insieme, il danno al DNA si è accumulato ancora di più. Dopo l’esposizione a radiazioni, la perdita di BRCA1 ha nettamente incrementato la morte cellulare, e la perdita combinata di entrambi i geni ha mantenuto questa aumentata vulnerabilità. Allo stesso tempo, è emerso il lato metabolico della storia. I livelli di colina—una molecola il cui accumulo è un noto segno distintivo di molti tumori—sono aumentati nei tumori epatici dei topi normali ma sono risultati attenuati nei tumori e nel sangue dei topi privi di BRCA1. Gli enzimi che convogliano la colina nei lipidi di membrana erano anch’essi ridotti, e un profilo metabolico ampio ha mostrato una produzione alterata di fosfatidilcolina, glicina e poliamine, tutte importanti per cellule in rapida divisione. Insieme, questi cambiamenti suggeriscono che senza BRCA1 le cellule epatiche accumulano danni al DNA letali e perdono accesso a carburanti metabolici chiave necessari per la crescita tumorale.
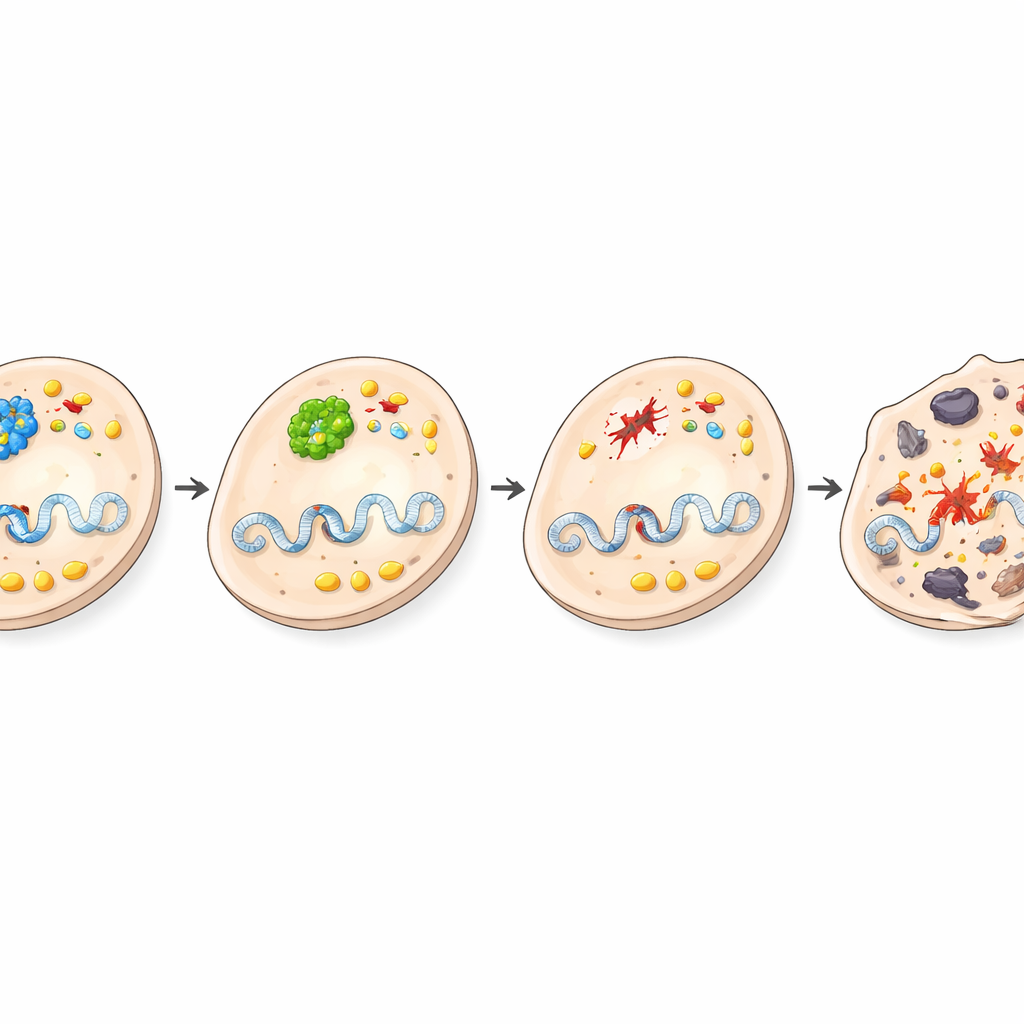
Cosa significa questo rovesciamento per il cancro
Questo lavoro rivela che BRCA1, celebre come oncosoppressore in altre parti del corpo, può invece avere effetti promotori del tumore nel fegato supportando l’attività di BHMT e il metabolismo centrato sulla colina. Quando BRCA1 viene rimosso specificamente dalle cellule epatiche, l’attività di BHMT diminuisce, il danno al DNA diventa opprimente, le vie legate alla colina vengono attenuate e le cellule danneggiate muoiono invece di evolvere in tumori. Lo studio sottolinea come lo stesso gene possa avere ruoli opposti a seconda del tessuto e del contesto metabolico, e individua il metabolismo a un carbonio e della colina come bersagli promettenti per nuove strategie di prevenzione o trattamento del cancro del fegato.
Citazione: Ghebreselassie, M., Park, Y.J., Nakib, D. et al. Paradoxical oncogenic effects of hepatic Brca1 through modulating Bhmt. Sci Rep 16, 13479 (2026). https://doi.org/10.1038/s41598-026-39581-6
Parole chiave: cancro al fegato, BRCA1, metabolismo della colina, metabolismo a un carbonio, carcinoma epatocellulare