Clear Sky Science · fr
Effets oncogéniques paradoxaux de Brca1 hépatique via la modulation de Bhmt
Quand la protection contre le cancer fonctionne à l’envers
La plupart d’entre nous considèrent des gènes comme BRCA1 comme des gardiens qui empêchent le cancer. Cette étude renverse cette idée à propos du foie. Les chercheurs montrent que, dans certaines conditions, l’activité normale de BRCA1 dans les cellules hépatiques peut en réalité favoriser la croissance des tumeurs hépatiques, tandis que sa suppression peut protéger contre le cancer. Comprendre ce retournement surprenant pourrait révéler de nouvelles façons de prévenir ou de traiter l’un des cancers les plus mortels au monde.
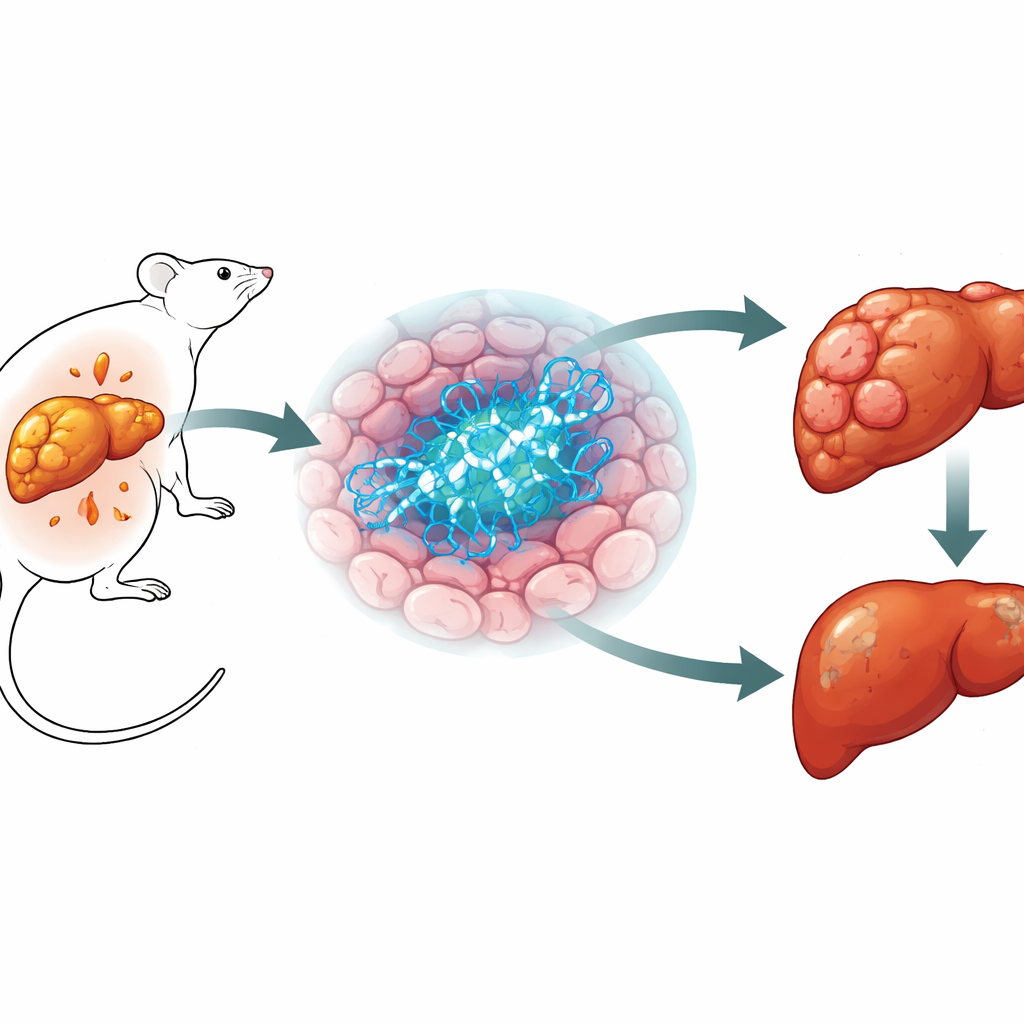
Un cancer du foie meurtrier en hausse
Le cancer du foie, en particulier le carcinome hépatocellulaire, est déjà l’un des cancers les plus fréquents et les plus meurtriers, et son fardeau continue d’augmenter. Un des moteurs principaux est une condition liée à l’obésité et au diabète de type 2, dans laquelle la graisse s’accumule progressivement dans le foie et peut évoluer vers la fibrose puis le cancer. Les scientifiques savent que le métabolisme et le cancer sont étroitement liés, mais de nombreux acteurs moléculaires précis restent flous. Parce que BRCA1 est depuis longtemps reconnu comme un gène suppresseur de tumeur dans les cancers du sein et de l’ovaire, et qu’il a également été associé à la gestion des lipides et des sucres par la cellule, les auteurs se sont demandé si BRCA1 pourrait influencer à la fois le métabolisme hépatique et le cancer du foie.
Éteindre un gardien dans les cellules hépatiques
L’équipe a créé des souris chez lesquelles BRCA1 était supprimé uniquement dans les cellules hépatiques, le reste du corps étant intact. Comme attendu au vu du rôle classique de BRCA1 dans la réparation de l’ADN endommagé, ces cellules hépatiques présentaient davantage de cassures de l’ADN. Mais l’état général des animaux racontait une histoire différente. Nourries avec un régime riche en graisses, les souris dépourvues de BRCA1 dans le foie accumulaient moins de lipides intra-hépatiques et géraient mieux le glucose que les souris normales, bien que leur poids corporel soit similaire. De façon encore plus frappante, lorsque les animaux ont été exposés à un agent cancérogène qui induit de façon fiable des tumeurs hépatiques, ceux sans BRCA1 dans leurs hépatocytes ont développé beaucoup moins de tumeurs et de plus petite taille que leurs congénères normaux. Cette protection est apparue dans deux modèles tumoraux différents, montrant que la présence de BRCA1 dans les cellules hépatiques peut, paradoxalement, favoriser la croissance tumorale.
Mise au jour d’une voie métabolique cachée
Pour comprendre comment la perte de BRCA1 pouvait protéger le foie du cancer, les chercheurs ont examiné les gènes actifs dans des milliers de noyaux cellulaires hépatiques individuels. Ils ont découvert qu’un gène, Bhmt, se distinguait par une activité constamment réduite en l’absence de BRCA1. BHMT est une enzyme presque exclusivement présente dans le foie qui occupe un carrefour entre le métabolisme de la méthionine et celui de la choline — des voies qui fournissent des briques pour l’ADN, soutiennent le marquage chimique des molécules et alimentent la production de lipides membranaires. Les analyses d’ensembles de gènes ont révélé que de nombreuses voies de petits composés et d’acides organiques, en particulier celles liées au métabolisme à un carbone et à l’utilisation de la choline, étaient atténuées dans les hépatocytes déficients en BRCA1, et les signatures associées à la formation de tumeurs hépatiques étaient également réduites. La même baisse d’activité de BHMT est apparue lorsque l’équipe a silencé BRCA1 dans des cellules humaines de cancer du foie, suggérant une connexion directe entre les deux gènes.
Trop de dommages, pas assez de carburant pour les tumeurs
Les auteurs ont ensuite étudié de plus près l’interaction fonctionnelle entre BRCA1 et BHMT. Dans des cellules humaines de carcinome hépatocellulaire, l’inactivation de BRCA1 a augmenté les cassures de l’ADN, et l’inactivation de BHMT a eu le même effet. Lorsque les deux ont été supprimés simultanément, les dommages à l’ADN se sont accumulés encore davantage. Après irradiation de ces cellules, la perte de BRCA1 a fortement renforcé la mort cellulaire, et la perte combinée des deux gènes a maintenu cette vulnérabilité accrue. Parallèlement, l’aspect métabolique de l’histoire est devenu clair. Les niveaux de choline — une molécule dont l’accumulation est un marqueur reconnu de nombreux cancers — augmentaient dans les tumeurs hépatiques des souris normales mais étaient atténués dans les tumeurs et le sang des souris déficientes en BRCA1. Les enzymes qui orientent la choline vers les lipides membranaires étaient également réduites, et le profilage métabolique large a montré une production perturbée de phosphatidylcholine, de glycine et de polyamines, tous importants pour les cellules en division rapide. Ensemble, ces changements suggèrent que sans BRCA1, les cellules hépatiques accumulent à la fois des dommages à l’ADN létaux et perdent l’accès à un carburant métabolique clé nécessaire à la croissance tumorale.
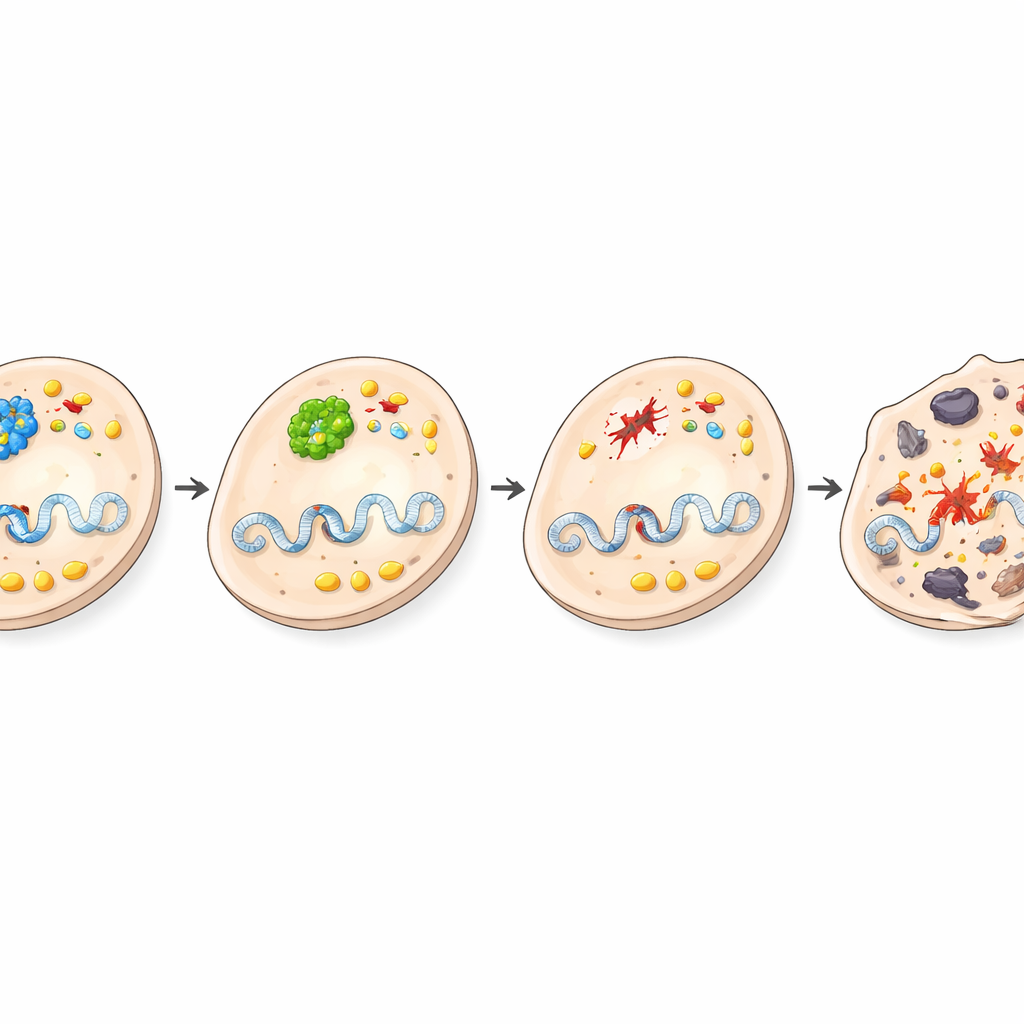
Ce que ce renversement signifie pour le cancer
Ce travail révèle que BRCA1, célèbre comme suppresseur de tumeur dans d’autres tissus, peut au contraire avoir des effets promoteurs de tumeur dans le foie en soutenant l’activité de BHMT et le métabolisme centré sur la choline. Lorsque BRCA1 est supprimé spécifiquement dans les cellules hépatiques, l’activité de BHMT diminue, les dommages à l’ADN deviennent accablants, les voies liées à la choline sont atténuées et les cellules endommagées meurent plutôt que d’évoluer en tumeurs. L’étude met en lumière comment un même gène peut jouer des rôles opposés selon le tissu et le contexte métabolique, et elle identifie le métabolisme à un carbone et de la choline comme des cibles prometteuses pour de nouvelles stratégies de prévention ou de traitement du cancer du foie.
Citation: Ghebreselassie, M., Park, Y.J., Nakib, D. et al. Paradoxical oncogenic effects of hepatic Brca1 through modulating Bhmt. Sci Rep 16, 13479 (2026). https://doi.org/10.1038/s41598-026-39581-6
Mots-clés: cancer du foie, BRCA1, métabolisme de la choline, métabolisme à un carbone, carcinome hépatocellulaire