Clear Sky Science · de
Paradoxe onkogene Effekte von hepatischem Brca1 durch Modulation von Bhmt
Wenn Krebsabwehr sich umkehrt
Die meisten von uns betrachten Gene wie BRCA1 als Wächter, die Krebs verhindern. Diese Studie stellt diese Vorstellung für die Leber auf den Kopf. Die Forschenden zeigen, dass unter bestimmten Bedingungen normale BRCA1‑Aktivität in Leberzellen das Tumorwachstum fördern kann, während das Abschalten dieses Gens vor Krebs schützt. Das Verständnis dieser überraschenden Wendung könnte neue Wege zur Prävention oder Behandlung einer der tödlichsten Krebserkrankungen weltweit eröffnen.
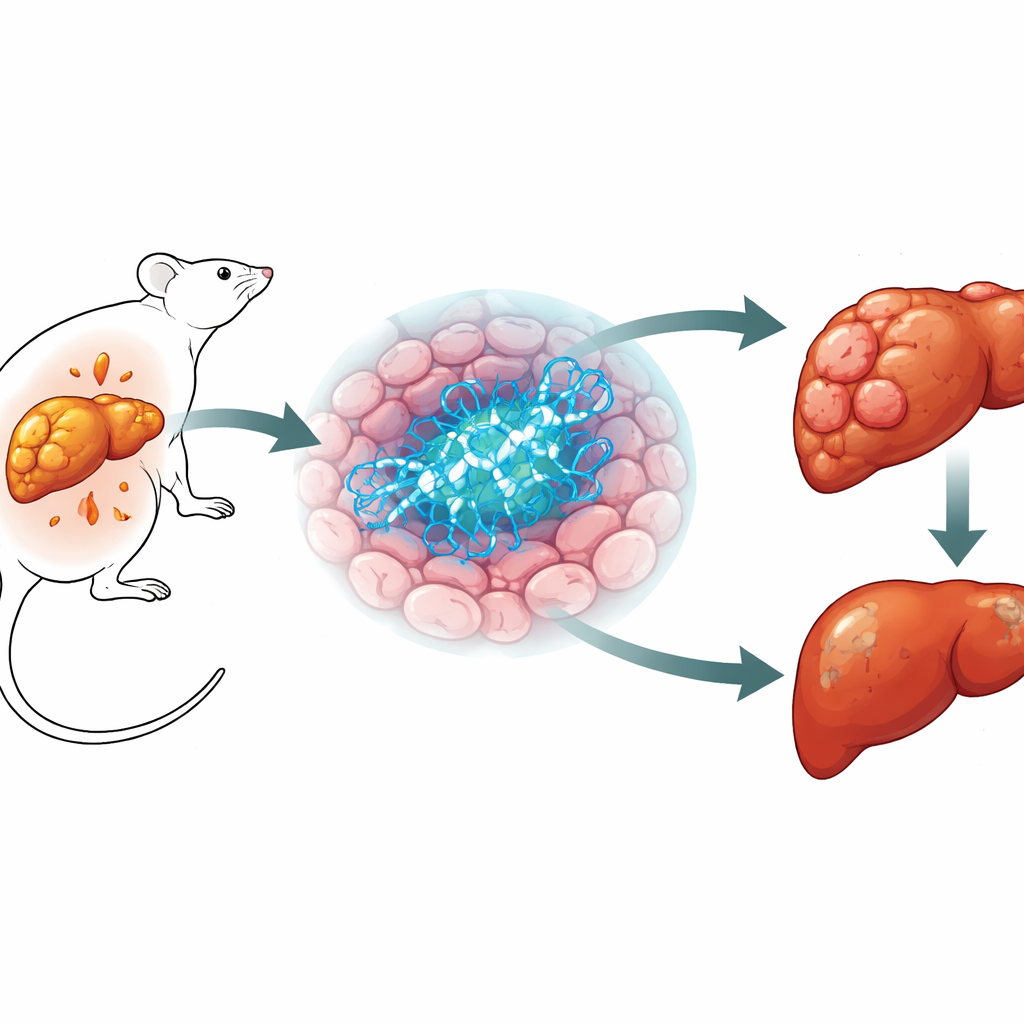
Ein tödlicher Leberkrebs nimmt zu
Leberkrebs, insbesondere das hepatozelluläre Karzinom, gehört bereits zu den häufigsten und tödlichsten Krebsarten, und die Belastung steigt weiterhin. Ein wichtiger Treiber ist eine Erkrankung, die mit Adipositas und Typ‑2‑Diabetes verknüpft ist, bei der sich langsam Fett in der Leber ansammelt und bis zur Vernarbung und schließlich zum Krebs fortschreiten kann. Forschende wissen, dass Stoffwechsel und Krebs eng miteinander verbunden sind, doch viele der konkreten molekularen Akteure bleiben unklar. Da BRCA1 lange als Tumorsuppressorgen bei Brust‑ und Eierstockkrebs anerkannt ist und zudem mit der zellulären Handhabung von Fetten und Zuckern in Verbindung gebracht wurde, fragten die Autorinnen und Autoren, ob BRCA1 sowohl den Leberstoffwechsel als auch Leberkrebs beeinflussen könnte.
Den Wächter in Leberzellen abschalten
Das Team erzeugte Mäuse, bei denen BRCA1 nur aus Leberzellen entfernt wurde, während der Rest des Körpers unverändert blieb. Wie zu erwarten bei BRCA1s klassischer Rolle in der Reparatur beschädigter DNA zeigten diese Leberzellen mehr DNA‑Brüche. Die Gesamtverfassung der Tiere erzählte jedoch eine andere Geschichte. Unter einer fettreichen Diät akkumulierten Mäuse ohne BRCA1 in der Leber weniger Fett in der Leber und regulierten Zucker besser als normale Tiere, obwohl das Körpergewicht ähnlich war. Am auffälligsten war, dass nach Exposition gegenüber einem krebserzeugenden Chemikal, das zuverlässig Lebertumoren produziert, die Tiere ohne BRCA1 in ihren Leberzellen deutlich weniger und kleinere Tumoren entwickelten als ihre normalen Wurfgeschwister. Dieser Schutz zeigte sich in zwei verschiedenen Tumormodellen und deutet darauf hin, dass die Anwesenheit von BRCA1 in Leberzellen paradoxerweise Tumorwachstum begünstigen kann.
Aufdeckung eines verborgenen Stoffwechselwegs
Um zu verstehen, wie der Verlust von BRCA1 die Leber vor Krebs schützen kann, untersuchten die Forschenden, welche Gene in Tausenden einzelner Leberzellkerne aktiv waren. Sie entdeckten, dass ein Gen, Bhmt, konstant weniger aktiv war, wenn BRCA1 fehlte. BHMT ist ein Enzym, das fast ausschließlich in der Leber vorkommt und an einer Schnittstelle des Methionin‑ und Cholinstoffwechsels liegt — Wege, die Bausteine für DNA liefern, die chemische Markierung von Molekülen unterstützen und die Produktion von Membranlipiden versorgen. Gen‑Set‑Analysen zeigten, dass viele kleine Molekül‑ und organische Säurewege, besonders solche, die mit Ein‑Kohlenstoff‑Stoffwechsel und Cholinverwendung verbunden sind, in BRCA1‑defizienten Hepatozyten heruntergefahren waren, und auch Signaturen, die mit Lebertumorbildung assoziiert sind, waren reduziert. Derselbe Rückgang der BHMT‑Aktivität trat auf, wenn das Team BRCA1 in menschlichen Leberkrebszellen stumm schaltete, was auf eine direkte Verbindung zwischen den beiden Genen hindeutet.
Zu viel Schaden, zu wenig Treibstoff für Tumoren
Die Autorinnen und Autoren untersuchten dann, wie BRCA1 und BHMT funktionell zusammenwirken. In menschlichen Leberkrebszellen führte das Abschalten von BRCA1 zu mehr DNA‑Brüchen, ebenso das Abschalten von BHMT. Wenn beide gemeinsam unterdrückt wurden, häuften sich die DNA‑Schäden noch stärker. Nachdem diese Zellen Bestrahlung ausgesetzt wurden, verstärkte der Verlust von BRCA1 den Zelltod deutlich, und der kombinierte Verlust beider Gene hielt diese erhöhte Verwundbarkeit aufrecht. Gleichzeitig rückte die metabolische Seite der Geschichte in den Fokus. Cholinspiegel — ein Molekül, dessen Anreicherung ein anerkanntes Kennzeichen vieler Krebserkrankungen ist — stiegen in Lebertumoren normaler Mäuse an, waren aber in Tumoren und Blut von BRCA1‑defizienten Mäusen abgeschwächt. Enzyme, die Cholin in Membranlipide einbinden, waren ebenfalls reduziert, und breit angelegte Metabolitenprofile zeigten gestörte Produktion von Phosphatidylcholin, Glycin und Polyaminen, die alle für schnell teilende Zellen wichtig sind. Zusammengenommen deuten diese Veränderungen darauf hin, dass ohne BRCA1 Leberzellen einerseits tödliche DNA‑Schäden anhäufen und andererseits den Zugang zu wichtigen metabolischen Treibstoffen verlieren, die für Tumorwachstum benötigt werden.
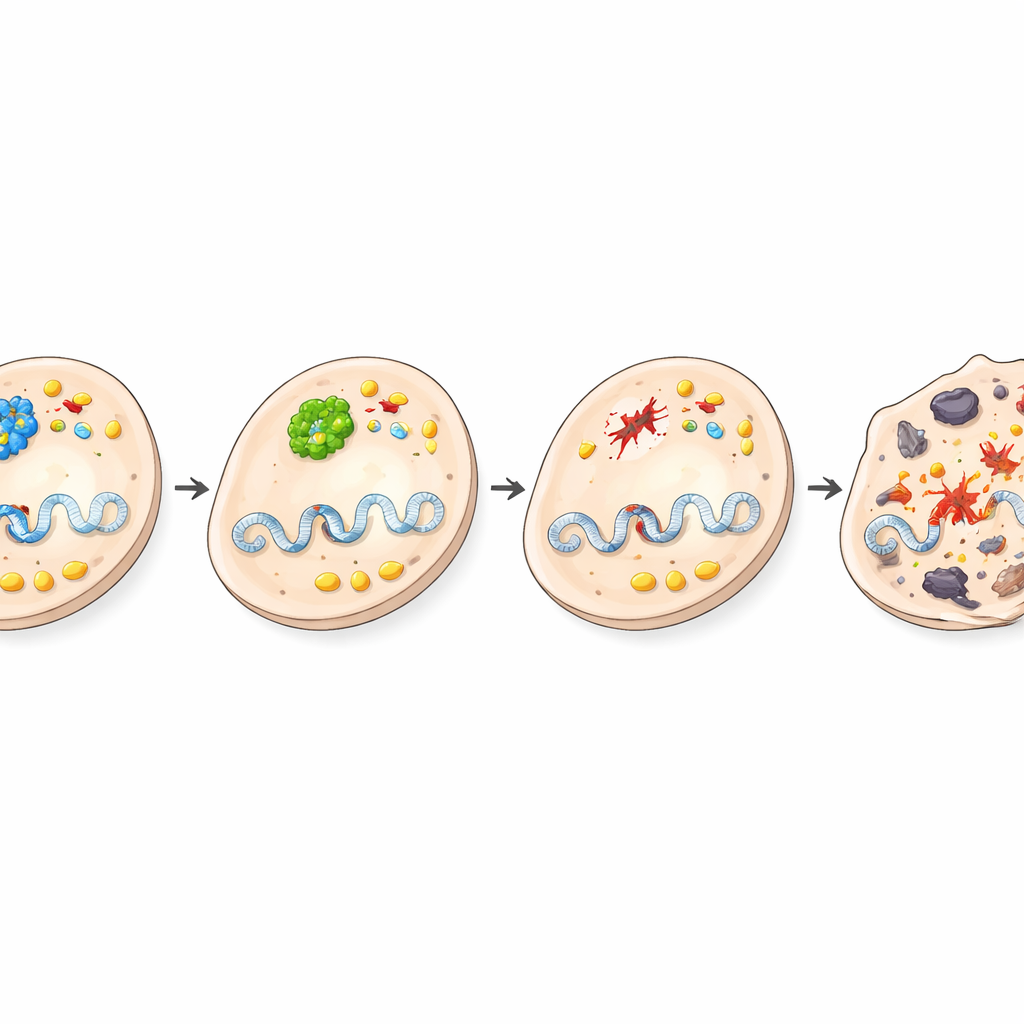
Was diese Wendung für Krebs bedeutet
Diese Arbeit zeigt, dass BRCA1, bekannt als Tumorsuppressor in anderen Körperregionen, in der Leber stattdessen tumorfördernde Effekte haben kann, indem es BHMT‑Aktivität und cholinzentrierten Stoffwechsel unterstützt. Wenn BRCA1 spezifisch aus Leberzellen entfernt wird, fällt die BHMT‑Aktivität, die DNA‑Schäden werden überwältigend, cholinbezogene Stoffwechselwege werden gedämpft und geschädigte Zellen sterben, anstatt sich zu Tumoren zu entwickeln. Die Studie macht deutlich, wie dasselbe Gen je nach Gewebe und metabolischem Kontext gegensätzliche Rollen spielen kann, und weist auf Ein‑Kohlenstoff‑ und Cholin‑Stoffwechsel als vielversprechende Zielbereiche für neue Strategien zur Prävention oder Behandlung von Leberkrebs hin.
Zitation: Ghebreselassie, M., Park, Y.J., Nakib, D. et al. Paradoxical oncogenic effects of hepatic Brca1 through modulating Bhmt. Sci Rep 16, 13479 (2026). https://doi.org/10.1038/s41598-026-39581-6
Schlüsselwörter: Leberkrebs, BRCA1, Cholin‑Stoffwechsel, Ein‑Kohlenstoff‑Stoffwechsel, hepatozelluläres Karzinom