Clear Sky Science · zh
骨髓供者来源与粪菌移植后小鼠肠道微生物组组成之间的关联
为什么肠道微生物的重要性不容忽视
医生越来越多地使用粪菌移植(FMT)——将健康供者的粪便转移到患者体内——以重置肠道微生物群,治疗顽固性疾病。但并非每次移植都能同样成功。这项小鼠研究提出了一个出乎意料但非常实用的问题:如果受者先前接受过骨髓移植,从而拥有不同来源的免疫系统,骨髓的来源是否会改变供者肠道微生物定植的程度?答案有助于设计更安全、更可靠的基于微生物组的治疗方案。
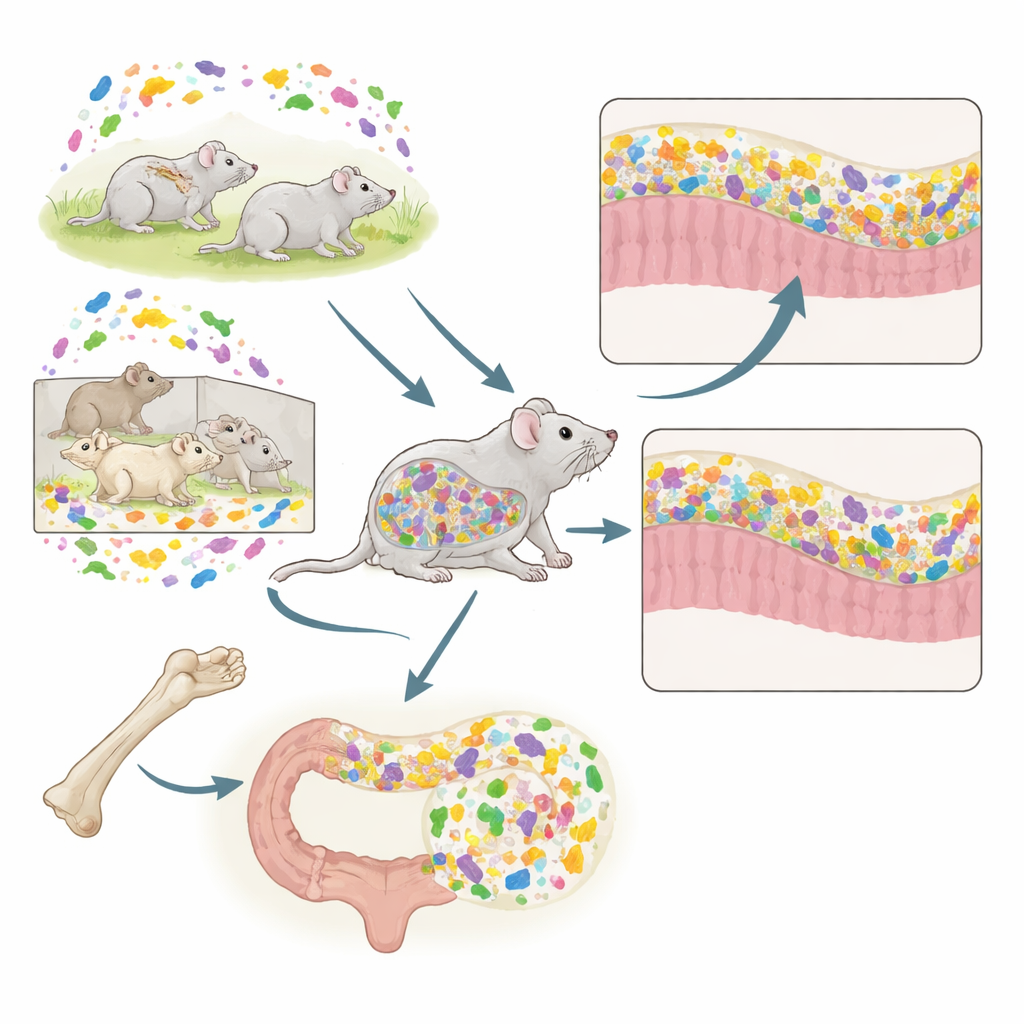
两次移植,一只小鼠
研究者在小鼠身上结合了两种强大的手段:骨髓移植(BMT),用于替换免疫细胞;以及粪菌移植(FMT),用于替换肠道微生物。供者小鼠来自两种不同的生活环境。常规(CV)小鼠生活在标准开放笼中,携带丰富且多样的微生物群。无特定致病原(SPF)小鼠生活在受保护的屏障设施中,携带较简单、较少样化的微生物群和发育较不成熟的免疫系统。受体小鼠始终生活在常规环境中,但在不同组合下接受来自CV或SPF供者的骨髓和/或粪便。该设计让团队能够检验由骨髓来源塑造的免疫背景如何与进入的粪便微生物相互作用。
检查谁定居了肠道
在FMT后一周,科学家收集粪便样本并分析细菌DNA,重点查看哪些类型的微生物存在以及它们的丰度。总体多样性——微生物的种类和相对平衡——在各组间差异不大。然而,群落的详细结构有所不同。使用能捕捉哪些物种存在(而不是每种优势程度)的距离度量,他们发现骨髓供者的来源显著改变了FMT后建立的微生物模式。当粪便来自常规供者时,这些影响最为明显,表明更丰富、更复杂的微生物混合物对由骨髓设定的免疫环境特别敏感。
微生物代谢的隐性功能变化
为了超越“谁在那里”的问题并探寻“它们可能在做什么”,研究团队使用计算工具从细菌DNA谱预测代谢途径。当骨髓和粪便均来自具有相同类型微生物组的供者(CV配CV或SPF配SPF)时,肠道群落的预测功能以一致的方式发生变化。在接受匹配CV材料的小鼠中,与构建精氨酸和多胺等氨基酸相关的通路更为突出。在接受匹配SPF材料的小鼠中,与酪氨酸和苯丙氨酸等芳香族氨基酸相关的通路被预测会增加。这些预测是间接的,需通过更深入的分子分析来证实,但它们暗示供者来源的匹配可能微妙地引导移植微生物能够产生的产物。
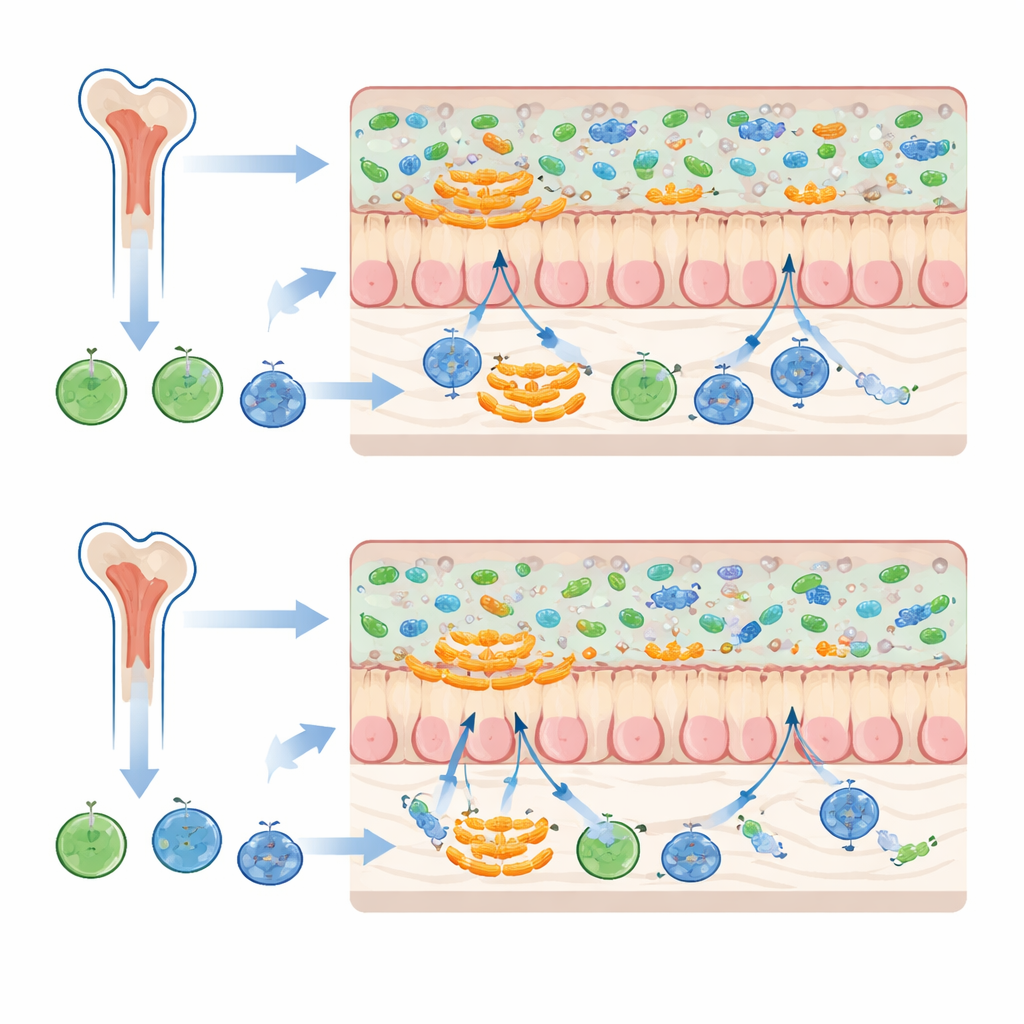
一类特别的黏液喜好细菌
最显著的变化涉及一类名为Muribaculaceae的细菌, 它们倾向于靠近肠道黏液层生存,而不是悬浮在肠内容物中。当小鼠同时接受来自相同微生物背景供者的骨髓和粪便时,某些Muribaculaceae的丰度增加,受体的整体微生物群更接近粪便供者的构成。而当骨髓与粪便来自不同微生物背景时,这些细菌的扩增较少,受体中呈现供者样群落的程度也较低。由于黏液相关微生物处于肠内容物与肠上皮之间的界面,它们可能对供者来源骨髓细胞设定的免疫基调尤其敏感。
这对未来治疗意味着什么
简单来说,该研究表明,个体免疫系统与进入的肠道微生物之间的“匹配”会影响FMT后哪些细菌得以持续存在,尤其是靠近肠壁的那些。小鼠实验中,匹配骨髓与粪便供者背景有利于某些黏液定居细菌的生长,并使受体微生物群更接近供者,尽管总体多样性并未发生显著变化。尽管放射预处理和其他移植前处理也会影响肠道,且在本研究中未被完全分离开来,这些结果强调了免疫史对于微生物组治疗的重要性。随着FMT及相关方法在患者中推进,尤其是免疫功能受损者,仔细考虑供–受者配对可能会使这些治疗更可预测、更有效。
引用: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
关键词: 粪菌移植, 骨髓移植, 肠道微生物组, 免疫系统, 黏液相关细菌