Clear Sky Science · fr
Association entre l’origine du donneur de moelle osseuse et la composition du microbiote intestinal après transplantation de microbiote fécal chez la souris
Pourquoi les petits habitants de l’intestin ont de l’importance
Les médecins utilisent de plus en plus la transplantation de microbiote fécal (TMF) — transfert de selles d’un donneur sain vers un patient — pour réinitialiser la communauté microbienne intestinale et traiter des maladies récalcitrantes. Mais toutes les transplantations ne « prennent » pas de la même façon. Cette étude chez la souris pose une question étonnamment pratique : si un patient a précédemment reçu une transplantation de moelle osseuse et possède donc un système immunitaire d’origine différente, l’origine de cette moelle change-t-elle la capacité des microbes fécaux du donneur à s’implanter ? La réponse pourrait aider à concevoir des thérapies microbiomiques plus sûres et plus fiables.
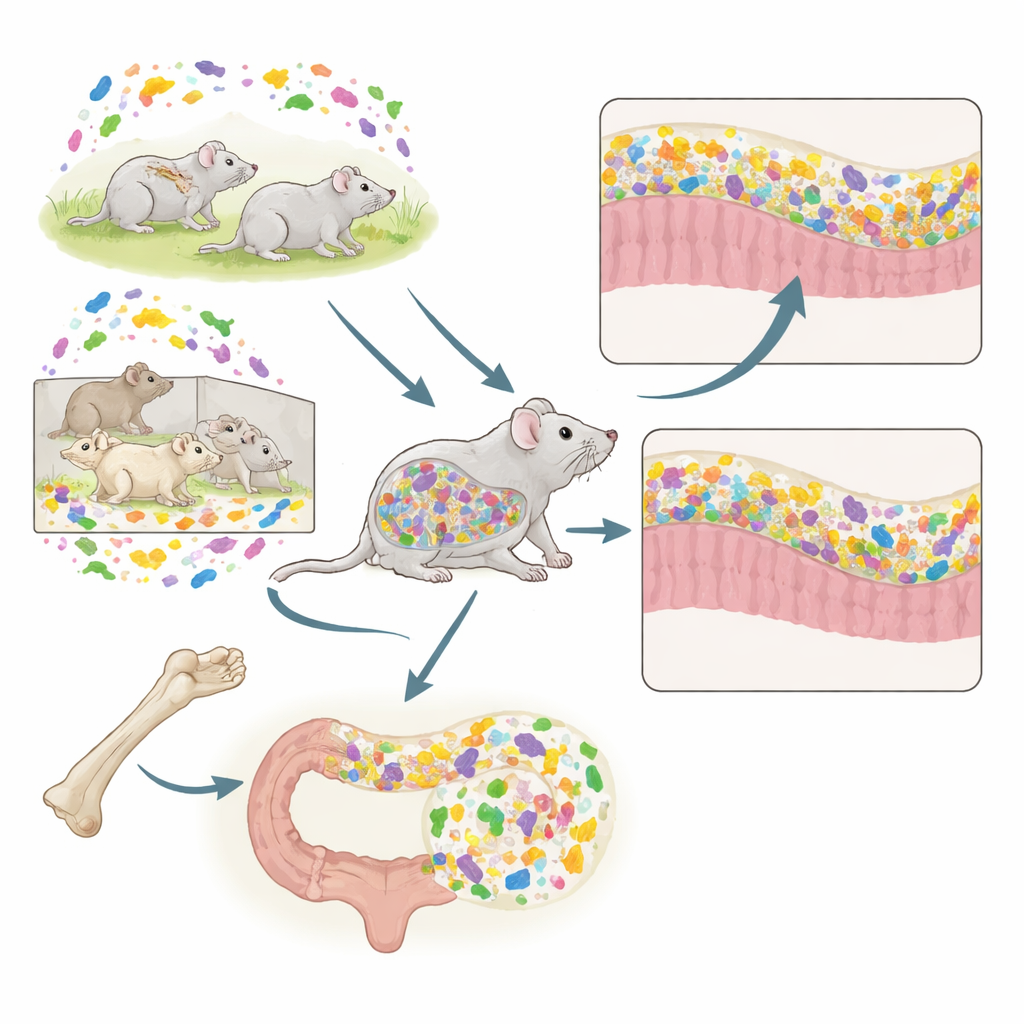
Deux transplantations, une souris
Les chercheurs ont combiné deux outils puissants chez la souris : la transplantation de moelle osseuse (TMO), qui remplace les cellules immunitaires, et la TMF, qui remplace les microbes intestinaux. Les souris donneuses provenaient de deux conditions de vie distinctes. Les souris conventionnelles (CV) vivent en cages ouvertes standard et hébergent un microbiote riche et varié. Les souris spécifiques-pathogènes libres (SPF) vivent en installations barrières protégées et portent une communauté microbienne plus simple et moins diversifiée ainsi qu’un système immunitaire moins mature. Les souris receveuses vivaient toujours en conditions conventionnelles mais recevaient de la moelle osseuse et/ou des fèces de donneurs CV ou SPF selon différentes combinaisons. Ce plan expérimental a permis à l’équipe de tester comment le fond immunitaire façonné par l’origine de la moelle osseuse interagissait avec les microbes fécaux entrants.
Vérifier qui s’installe dans l’intestin
Une semaine après la TMF, les scientifiques ont collecté des échantillons fécaux et analysé l’ADN bactérien, en se concentrant sur les types de microbes présents et leur abondance. La diversité globale — la variété et l’équilibre des microbes — ne différait pas beaucoup entre les groupes. Cependant, la structure détaillée des communautés variait. En utilisant des mesures de distance qui capturent quelles espèces sont présentes (plutôt que leur dominance), ils ont constaté que l’origine du donneur de moelle osseuse modifiait significativement le profil des microbes qui s’établissaient après la TMF. Ces effets étaient les plus marqués lorsque le matériel fécal provenait de donneurs conventionnels, ce qui suggère qu’un mélange microbien plus riche et complexe est particulièrement sensible à l’environnement immunitaire déterminé par la moelle osseuse.
Modifications fonctionnelles cachées du métabolisme microbien
Pour aller au-delà du « qui est là » et s’intéresser à « ce qu’ils pourraient faire », l’équipe a utilisé des outils computationnels pour prédire des voies métaboliques à partir des profils d’ADN bactérien. Lorsque la moelle osseuse et les fèces provenaient toutes deux de donneurs avec le même type de microbiote (CV avec CV, ou SPF avec SPF), les fonctions prédites de la communauté intestinale évoluaient de manière cohérente. Chez les souris recevant du matériel CV apparié, les voies liées à la synthèse d’acides aminés tels que l’arginine et les polyamines étaient plus proéminentes. Chez les souris avec du matériel SPF apparié, les voies relatives aux acides aminés aromatiques comme la tyrosine et la phénylalanine semblaient augmenter. Ces prévisions sont indirectes et doivent être confirmées par des analyses moléculaires plus approfondies, mais elles suggèrent que l’appariement des sources de donneurs peut orienter subtilement ce que les microbes transplantés sont capables de produire.
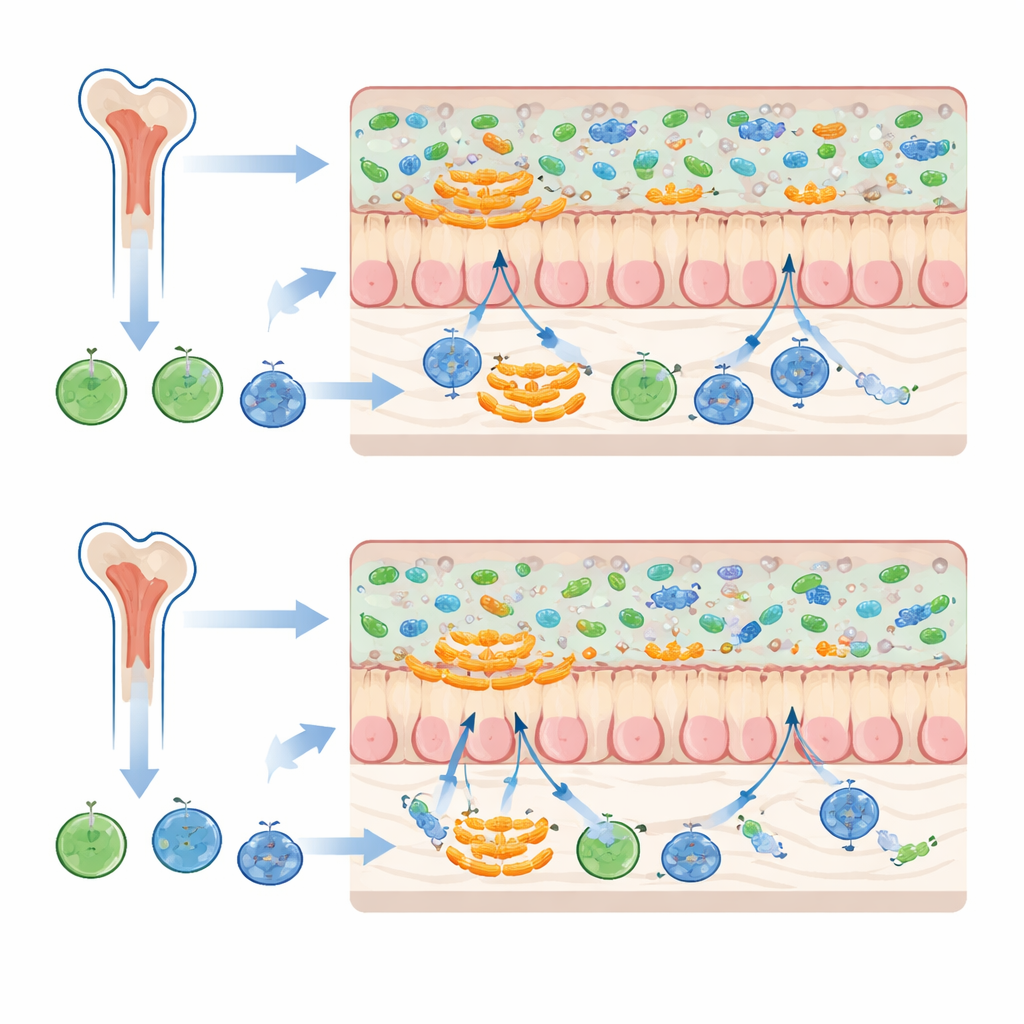
Un groupe particulier de bactéries attirées par le mucus
Les changements les plus marquants concernaient une famille de bactéries appelée Muribaculaceae, qui ont tendance à vivre près de la couche de mucus intestinale plutôt qu’en suspension dans le contenu intestinal. Lorsque les souris recevaient à la fois la moelle osseuse et les fèces de donneurs ayant le même arrière-plan microbiotique, certains Muribaculaceae devenaient plus abondants et la communauté microbienne globale des receveurs ressemblait davantage à celle des donneurs fécaux. Lorsque la moelle osseuse et les fèces provenaient d’arrière-plans microbiotiques différents, ces bactéries se développaient moins et les communautés de type donneur étaient moins fidèlement reproduites. Comme les microbes associés au mucus se situent à l’interface entre le contenu intestinal et la muqueuse, ils peuvent être particulièrement sensibles au ton immunitaire imposé par les cellules de moelle osseuse d’origine donneur.
Ce que cela signifie pour les traitements futurs
En termes simples, l’étude suggère que la « compatibilité » entre le système immunitaire d’une personne et les microbes intestinaux entrants peut influencer quelles bactéries persistent après une TMF, en particulier celles vivant près de la paroi intestinale. L’appariement des origines de la moelle osseuse et des fèces chez la souris favorisait la croissance de certaines bactéries du mucus et aidait les microbiotes des receveurs à ressembler davantage à ceux des donneurs, même si la diversité globale n’était pas fortement modifiée. Bien que la radiothérapie et d’autres traitements préparatoires influencent aussi l’intestin et n’aient pas été complètement dissociés ici, ces résultats mettent en évidence que l’historique immunitaire compte pour les thérapies du microbiome. À mesure que la TMF et des approches apparentées progressent chez les patients, en particulier chez les immunodéprimés, considérer attentivement les appariements donneur–receveur pourrait rendre ces traitements plus prévisibles et efficaces.
Citation: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Mots-clés: transplantation de microbiote fécal, transplantation de moelle osseuse, microbiome intestinal, système immunitaire, bactéries associées au mucus