Clear Sky Science · pt
Associação entre a origem do doador de medula óssea e a composição da microbiota intestinal após transplante de microbiota fecal em camundongos
Por que os pequenos habitantes do intestino importam
Médicos usam cada vez mais o transplante de microbiota fecal (TMF) — a transferência de fezes de um doador saudável para um paciente — para redefinir a comunidade microbiana intestinal e tratar doenças difíceis de curar. Mas nem todo transplante “pega” da mesma forma. Este estudo em camundongos faz uma pergunta surpreendentemente prática: se um paciente recebeu previamente um transplante de medula óssea e, portanto, tem um sistema imunológico diferente, a origem dessa medula muda a capacidade dos micróbios doador de se estabelecerem? A resposta pode ajudar a projetar terapias baseadas no microbioma mais seguras e confiáveis.
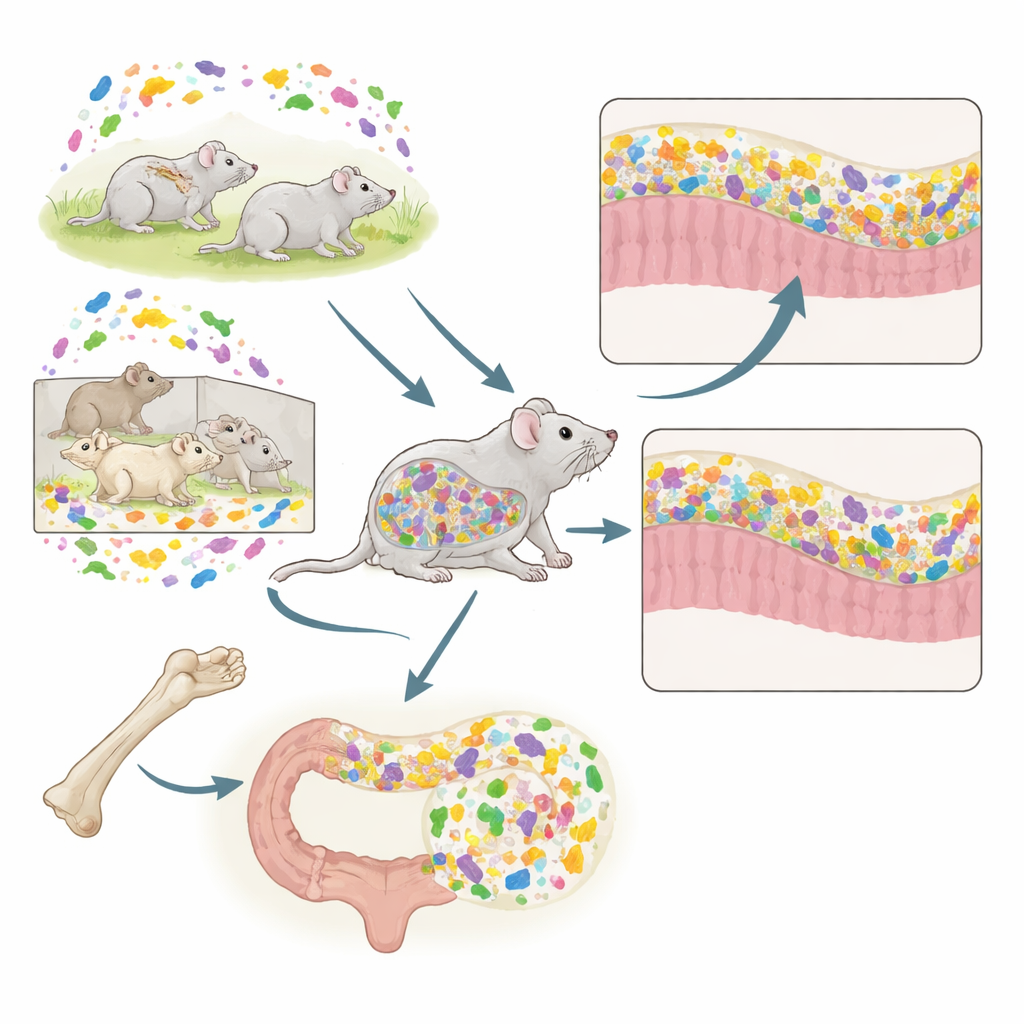
Dois transplantes, um camundongo
Os pesquisadores combinaram duas ferramentas poderosas em camundongos: transplante de medula óssea (TMO), que substitui células imunes, e TMF, que substitui micróbios intestinais. Os camundongos doadores vieram de duas condições de vida distintas. Camundongos convencionais (CV) vivem em gaiolas abertas padrão e abrigam uma microbiota rica e variada. Camundongos livres de patógenos específicos (SPF) vivem em instalações com barreira protegida e carregam uma comunidade microbiana mais simples, menos diversa e um sistema imunológico menos maduro. Os camundongos receptores viviam sempre em condições convencionais, mas receberam medula óssea e/ou fezes de doadores CV ou SPF em diferentes combinações. Esse desenho permitiu testar como o pano de fundo imune moldado pela origem da medula óssea interagia com os micróbios fecais entrantes.
Verificando quem se instala no intestino
Uma semana após o TMF, os cientistas coletaram amostras fecais e analisaram o DNA bacteriano, focando em quais tipos de micróbios estavam presentes e quão abundantes eram. A diversidade geral — a variedade e o equilíbrio de micróbios — não diferiu muito entre os grupos. No entanto, a estrutura detalhada da comunidade sim. Usando medidas de distância que capturam quais espécies estão presentes (em vez de quão dominantes são), eles descobriram que a origem do doador de medula óssea alterou significativamente o padrão de micróbios que se estabeleceram após o TMF. Esses efeitos foram mais óbvios quando o material fecal veio de doadores convencionais, sugerindo que uma mistura microbiana mais rica e complexa é particularmente sensível ao ambiente imune estabelecido pela medula óssea.
Mudanças funcionais ocultas no metabolismo microbiano
Para ir além de “quem está lá” e perguntar “o que eles podem estar fazendo”, a equipe usou ferramentas computacionais para prever vias metabólicas a partir dos perfis de DNA bacteriano. Quando medula óssea e fezes vieram ambos de doadores com o mesmo tipo de microbiota (CV com CV, ou SPF com SPF), as funções previstas da comunidade intestinal mudaram de maneiras consistentes. Em camundongos que receberam material CV combinado, vias ligadas à síntese de aminoácidos como arginina e poliaminas foram mais proeminentes. Em camundongos com material SPF combinado, vias relacionadas a aminoácidos aromáticos como tirosina e fenilalanina foram previstas como aumentadas. Essas previsões são indiretas e precisam de confirmação com análises moleculares mais profundas, mas sugerem que o pareamento das fontes doadoras pode orientar sutilmente o que os micróbios transplantados são capazes de produzir.
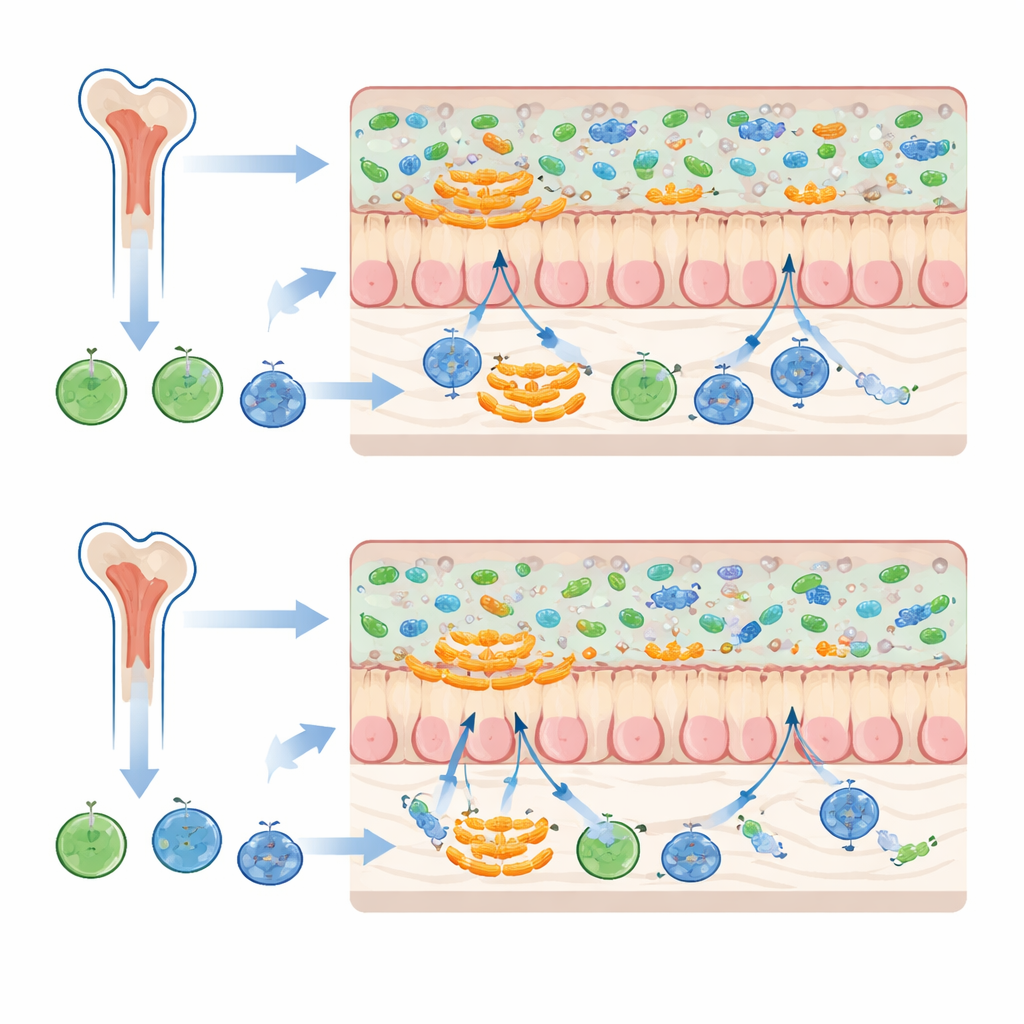
Um grupo especial de bactérias amantes do muco
As mudanças mais marcantes envolveram uma família de bactérias chamada Muribaculaceae, que tendem a viver perto da camada de muco intestinal em vez de flutuar livremente no conteúdo intestinal. Quando os camundongos receberam tanto medula óssea quanto fezes de doadores com o mesmo histórico de microbiota, certas Muribaculaceae se tornaram mais abundantes, e a comunidade microbiana geral nos receptores se assemelhou mais à dos doadores fecais. Quando medula óssea e fezes vieram de históricos de microbiota diferentes, essas bactérias expandiram-se menos e as comunidades semelhantes às dos doadores foram reproduzidas com menos fidelidade. Como micróbios associados ao muco ficam na interface entre o conteúdo intestinal e o revestimento intestinal, eles podem ser especialmente sensíveis ao tom imune estabelecido por células de medula óssea derivadas do doador.
O que isso significa para tratamentos futuros
Em termos simples, o estudo sugere que o “encaixe” entre o sistema imunológico de uma pessoa e seus micróbios intestinais entrantes pode influenciar quais bactérias permanecem após o TMF, especialmente aquelas que vivem perto da parede intestinal. Parear a origem da medula óssea e das fezes em camundongos favoreceu o crescimento de certas bactérias residentes do muco e ajudou as microbiotas dos receptores a espelhar mais de perto as dos doadores, mesmo que a diversidade geral não tenha mudado dramaticamente. Embora radiação e outros tratamentos pré-transplante também afetem o intestino e não tenham sido totalmente separados aqui, esses resultados ressaltam que a história imune importa para terapias do microbioma. À medida que o TMF e abordagens relacionadas avançam em pacientes, especialmente os imunocomprometidos, considerar cuidadosamente o pareamento doador–receptor pode tornar esses tratamentos mais previsíveis e eficazes.
Citação: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Palavras-chave: transplante de microbiota fecal, transplante de medula óssea, microbioma intestinal, sistema imunológico, bactérias associadas ao muco