Clear Sky Science · it
Associazione tra l'origine del donatore del midollo osseo e la composizione del microbiota intestinale dopo il trapianto di microbiota fecale nei topi
Perché contano i minuscoli abitanti dell’intestino
I medici utilizzano sempre più il trapianto di microbiota fecale (FMT)—il trasferimento di feci da un donatore sano a un paziente—per resettare la comunità microbica intestinale e trattare malattie ostinate. Ma non tutti i trapianti attecchiscono allo stesso modo. Questo studio sui topi pone una domanda sorprendentemente pratica: se un paziente ha ricevuto in precedenza un trapianto di midollo osseo e quindi possiede un sistema immunitario d’origine diversa, l’origine di quel midollo influisce sulla capacità dei microbi intestinali donati di stabilirsi? La risposta potrebbe aiutare a progettare terapie basate sul microbioma più sicure e affidabili.
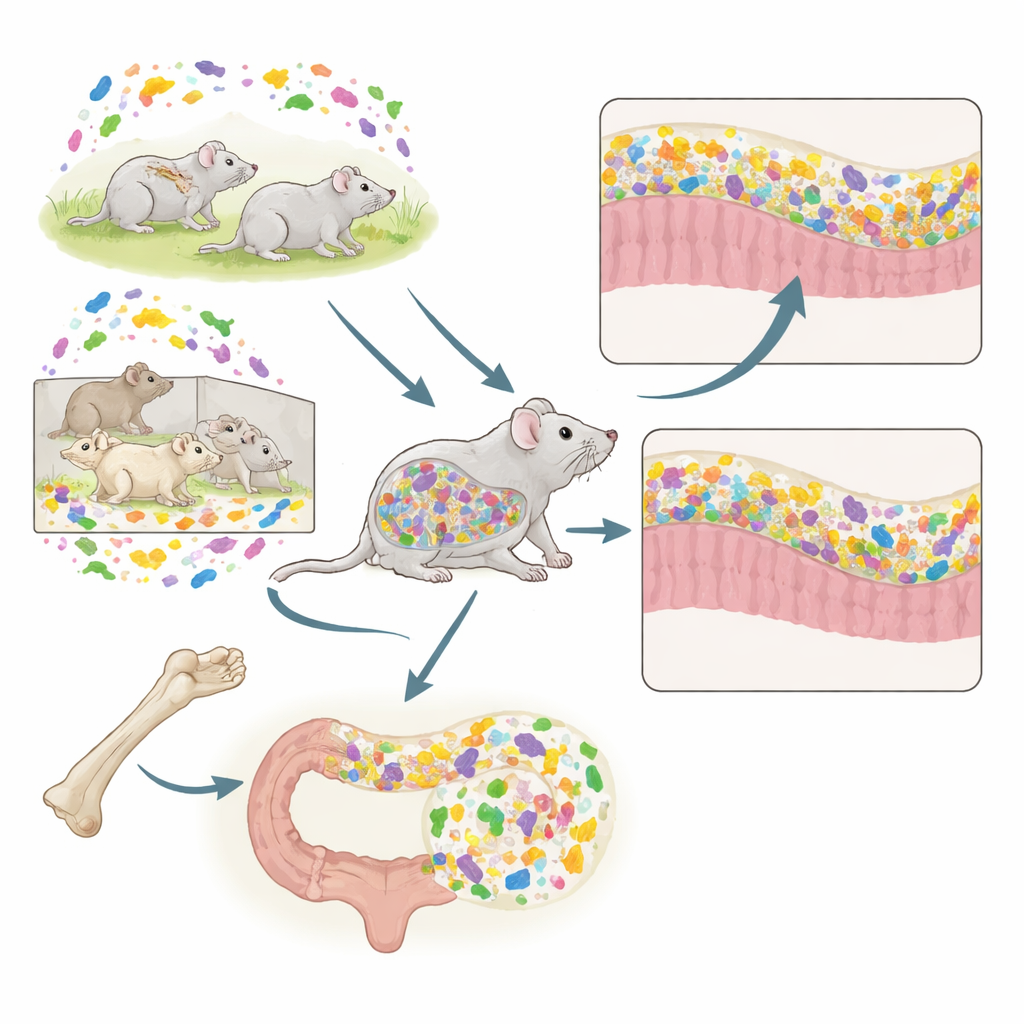
Due trapianti, un solo topo
I ricercatori hanno combinato due strumenti potenti nei topi: il trapianto di midollo osseo (BMT), che sostituisce le cellule immunitarie, e l’FMT, che sostituisce i microbi intestinali. I topi donatori provenivano da due condizioni di vita distinte. I topi convenzionali (CV) vivono in gabbie aperte standard e ospitano un microbiota ricco e variegato. I topi esenti da patogeni specifici (SPF) vivono in strutture protette a barriera e portano una comunità microbica più semplice, meno diversificata, e un sistema immunitario meno maturo. I topi riceventi vivevano sempre in condizioni convenzionali ma ricevevano midollo e/o feci da donatori CV o SPF in diverse combinazioni. Questo disegno sperimentale ha permesso al team di testare come il background immunitario plasmato dall’origine del midollo interagisse con i microbi fecali in arrivo.
Controllare chi si insedia nell’intestino
Una settimana dopo l’FMT, gli scienziati hanno raccolto campioni fecali e analizzato il DNA batterico, concentrandosi sui tipi di microbi presenti e sulla loro abbondanza. La diversità complessiva—la varietà e l’equilibrio dei microbi—non differiva molto tra i gruppi. Tuttavia, la struttura dettagliata della comunità sì. Utilizzando misure di distanza che catturano quali specie sono presenti (piuttosto che quanto ciascuna sia dominante), hanno scoperto che l’origine del donatore del midollo osseo cambiava in modo significativo il pattern dei microbi che si stabilivano dopo l’FMT. Questi effetti erano più evidenti quando il materiale fecale proveniva da donatori convenzionali, suggerendo che una miscela microbica più ricca e complessa sia particolarmente sensibile all’ambiente immunitario determinato dal midollo osseo.
Cambiamenti funzionali nascosti nel metabolismo microbico
Per andare oltre il “chi c’è” e chiedersi “cosa potrebbero fare”, il gruppo ha usato strumenti computazionali per prevedere le vie metaboliche a partire dai profili di DNA batterico. Quando midollo e feci provenivano entrambi da donatori con lo stesso tipo di microbiota (CV con CV, o SPF con SPF), le funzioni previste della comunità intestinale cambiavano in modi coerenti. Nei topo che ricevevano materiale CV corrispondente, risultavano più prominenti vie legate alla sintesi di aminoacidi come arginina e poliamine. Nei topo con materiale SPF corrispondente, si prevedeva un aumento delle vie legate ad aminoacidi aromatici come tirosina e fenilalanina. Queste previsioni sono indirette e richiedono conferme con analisi molecolari più approfondite, ma suggeriscono che l’abbinamento delle fonti del donatore potrebbe indirizzare sottilmente ciò che i microbi trapiantati sono in grado di produrre.
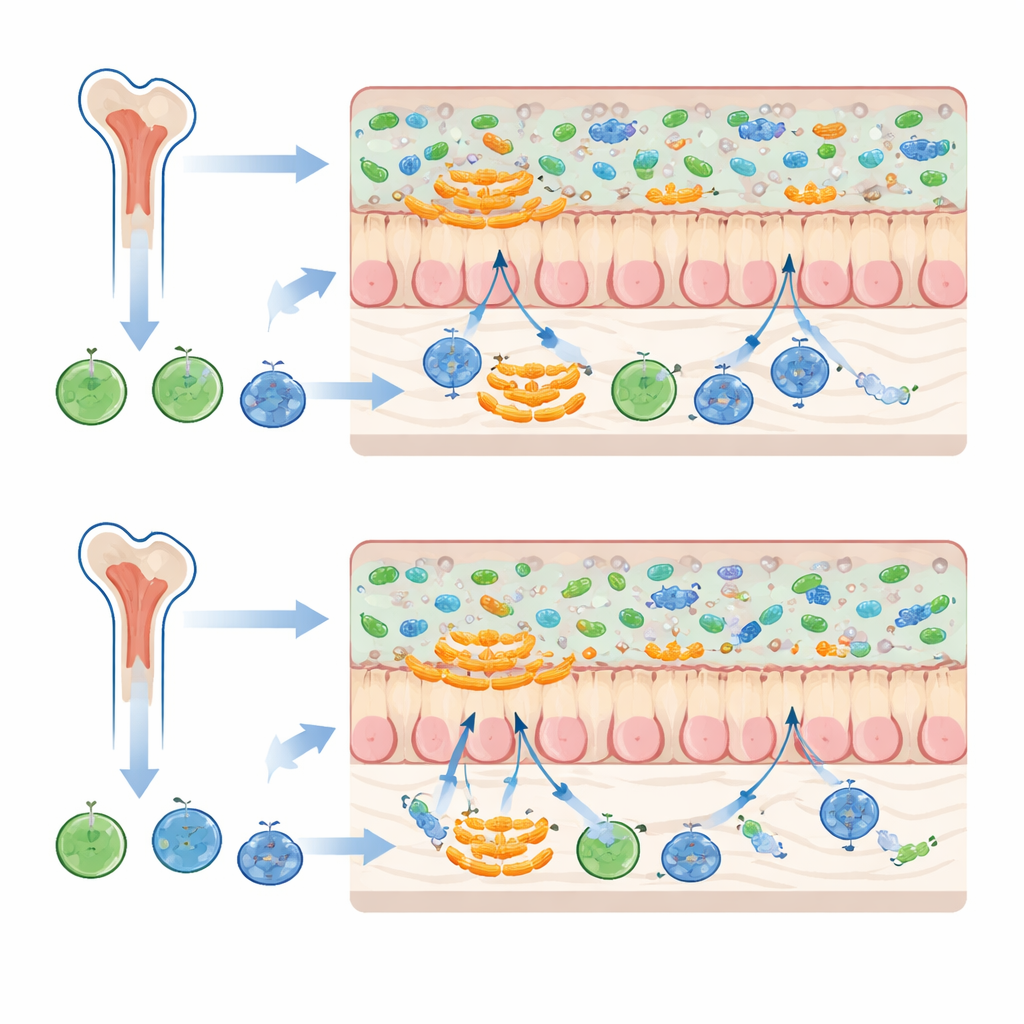
Un gruppo speciale di batteri amanti del muco
I cambiamenti più marcati hanno riguardato una famiglia di batteri chiamata Muribaculaceae, che tendono a vivere vicino allo strato di muco intestinale piuttosto che fluttuare liberamente nel contenuto intestinale. Quando i topi ricevevano sia midollo sia feci da donatori con lo stesso background di microbiota, alcune Muribaculaceae diventavano più abbondanti e la comunità microbica complessiva dei riceventi somigliava più da vicino a quella dei donatori fecali. Quando midollo e feci provenivano da background di microbiota differenti, questi batteri si espandevano meno e le comunità simili ai donatori si ricostituivano meno fedelmente. Poiché i microbi associati al muco si trovano all’interfaccia tra il contenuto intestinale e la parete intestinale, potrebbero essere particolarmente sensibili al tono immunitario stabilito dalle cellule del midollo osseo derivate dal donatore.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio suggerisce che il “match” tra il sistema immunitario di una persona e i microbi intestinali in arrivo può influenzare quali batteri rimangono dopo l’FMT, in particolare quelli che vivono vicino alla parete intestinale. L’abbinamento tra donatori di midollo e feci nei topi favoriva la crescita di certi batteri che abitano il muco e aiutava i microbioti dei riceventi ad avvicinarsi di più a quelli dei donatori, anche se la diversità complessiva non cambiava drasticamente. Pur considerando che la radiazione e altri trattamenti pre-trapianto influenzano anch’essi l’intestino e non sono stati completamente separati in questo studio, questi risultati sottolineano che la storia immunitaria conta per le terapie sul microbioma. Con il progresso dell’FMT e di approcci correlati nei pazienti, soprattutto negli immunocompromessi, valutare attentamente gli abbinamenti donatore–ricevente potrebbe rendere questi trattamenti più prevedibili ed efficaci.
Citazione: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Parole chiave: trapianto di microbiota fecale, trapianto di midollo osseo, microbioma intestinale, sistema immunitario, batteri associati al muco