Clear Sky Science · ru
Связь происхождения донора костного мозга и состава кишечной микробиоты после трансплантации фекальной микробиоты у мышей
Почему важны крошечные обитатели кишечника
Врачи всё чаще используют пересадку фекальной микробиоты (ФМТ) — перенос стула от здорового донора пациенту — чтобы «перезагрузить» сообщество микробов в кишечнике и лечить упорные заболевания. Но не каждая трансплантация приживается одинаково хорошо. В этом исследовании на мышах задают практичный вопрос: если пациент ранее получал пересадку костного мозга и, следовательно, имеет другую иммунную систему, изменяет ли происхождение этого костного мозга способность донорских кишечных микробов приживаться? Ответ может помочь в разработке более безопасных и предсказуемых микробиомных терапий.
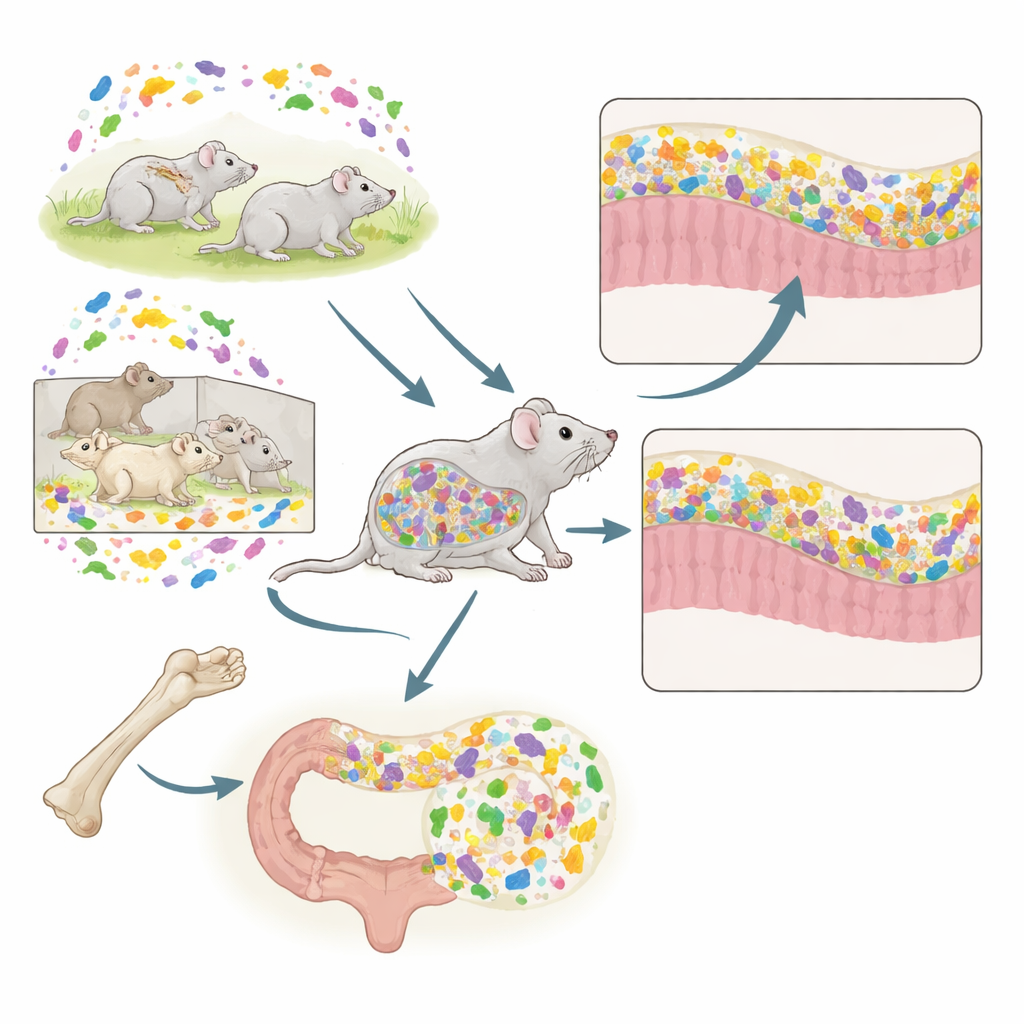
Две трансплантации — одна мышь
Исследователи сочетали два мощных подхода у мышей: трансплантацию костного мозга (ТКМ), которая заменяет иммунные клетки, и ФМТ, которая заменяет кишечные микроорганизмы. Донорские мыши происходили из двух разных условий содержания. Обычные (CV) мыши жили в стандартных открытых клетках и обладали богатой, разнообразной микробиотой. Мыши в условиях, свободных от специфических патогенов (SPF), содержались в защищённых барьерных условиях и имели более простое, менее разнообразное микробное сообщество и менее зрелую иммунную систему. Рецепиенты всегда жили в обычных условиях, но получали костный мозг и/или фекалии от CV или SPF доноров в разных комбинациях. Такой дизайн позволил команде проверить, как иммунный фон, сформированный происхождением костного мозга, взаимодействует с поступающими фекальными микробами.
Проверка, кто заселяет кишечник
Через неделю после ФМТ учёные собрали образцы кала и проанализировали бактериальную ДНК, сосредоточившись на том, какие типы микробов присутствуют и каковы их относительные численности. Общая разнообразность — совокупность видов и их равновесие — существенно не различалась между группами. Тем не менее детальная структура сообществ изменилась. С помощью мер расстояния, которые фиксируют, какие виды присутствуют (а не насколько каждый из них доминантен), они обнаружили, что происхождение донора костного мозга существенно изменяло картину микробов, установившихся после ФМТ. Эти эффекты были наиболее явными, когда фекальный материал поступал от обычных (CV) доноров, что указывает на то, что более богатая и сложная микробная смесь особенно чувствительна к иммунной среде, сформированной костным мозгом.
Скрытые функциональные сдвиги в микробном метаболизме
Чтобы заглянуть дальше «кто там есть» и спросить «что они могут делать», команда использовала вычислительные инструменты для предсказания метаболических путей по профилям бактериальной ДНК. Когда костный мозг и фекалии происходили от доноров с одинаковым типом микробиоты (CV с CV или SPF с SPF), предсказанные функции кишечного сообщества изменялись согласованным образом. У мышей, получавших согласованный CV материал, прогнозировалось усиление путей, связанных со синтезом аминокислот, таких как аргинин и полиамины. У мышей с согласованным SPF материалом ожидалось увеличение путей, связанных с ароматическими аминокислотами, такими как тирозин и фенилаланин. Эти прогнозы являются косвенными и требуют подтверждения при более глубоком молекулярном анализе, но они намекают, что совпадение источников доноров может тонко направлять то, что трансплантированные микробы способны продуцировать.
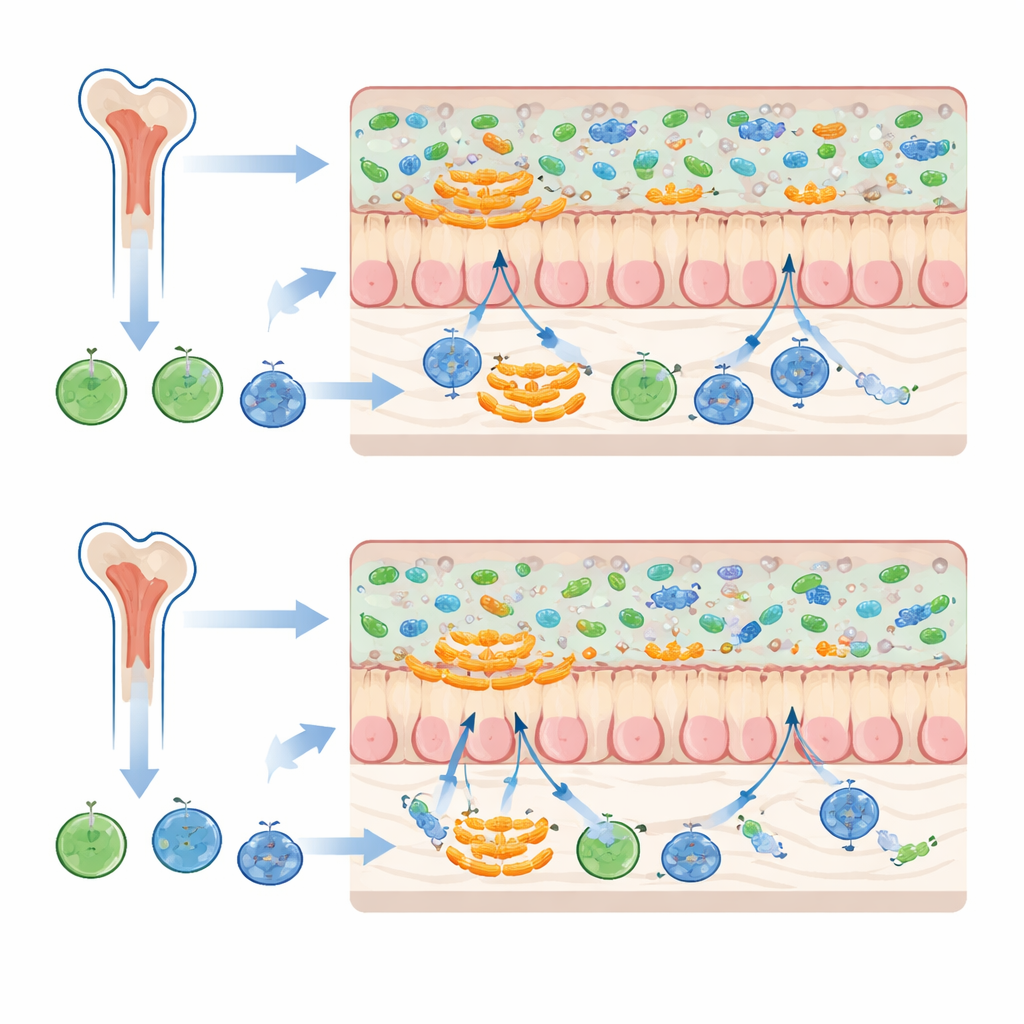
Особая группа бактерий, любящих слизь
Наиболее заметные изменения касались семейства бактерий Muribaculaceae, которые склонны жить близко к слою кишечной слизи, а не свободно плавать в содержимом кишки. Когда мыши получали и костный мозг, и фекалии от доноров с одинаковым микробиотным фоном, некоторые представители Muribaculaceae становились более многочисленными, и общее сообщество микробов у рецепиентов более точно напоминало микробиоту фекальных доноров. Когда костный мозг и фекалии происходили из разных микробиотных фонов, эти бактерии расширялись в меньшей степени, и донороподобные сообщества воспроизводились менее точно. Поскольку микроорганизмы, ассоциированные со слизью, располагаются на границе между содержимым кишечника и его слизистой оболочкой, они, вероятно, особенно чувствительны к иммунному тону, заданному клетками костного мозга донора.
Что это значит для будущих терапий
Проще говоря, исследование показывает, что «совпадение» между иммунной системой человека и поступающими кишечными микробами может влиять на то, какие бактерии сохраняются после ФМТ, особенно те, что живут близко к стенке кишечника. Совпадение происхождения костного мозга и фекалий у мышей способствовало росту определённых слизелюбивых бактерий и помогало микробиотам рецепиентов ближе соответствовать донорам, хотя общая разнообразность не претерпела драматичных изменений. Хотя радиация и другие предтрансплантационные процедуры также влияют на кишечник и не были полностью разнесены в этом исследовании, эти результаты подчёркивают, что иммунная история важна для микробиомных терапий. По мере продвижения ФМТ и родственных подходов к пациентам, особенно с ослабленным иммунитетом, тщательное рассмотрение пар донор–реципиент может сделать такие лечения более предсказуемыми и эффективными.
Цитирование: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Ключевые слова: пересадка фекальной микробиоты, трансплантация костного мозга, кишечный микробиом, иммунная система, бактерии, ассоциированные со слизью