Clear Sky Science · es
Asociación entre el origen del donante de médula ósea y la composición del microbiota intestinal tras el trasplante de microbiota fecal en ratones
Por qué importan los pequeños inquilinos del intestino
Los médicos recurren cada vez más al trasplante de microbiota fecal (TMF): transferir heces de un donante sano a un paciente para reiniciar la comunidad microbiana intestinal y tratar enfermedades persistentes. Pero no todos los trasplantes “prenden” por igual. Este estudio en ratones plantea una pregunta sorprendentemente práctica: si un paciente ha recibido previamente un trasplante de médula ósea y, por lo tanto, tiene un sistema inmunitario distinto, ¿cambia el origen de esa médula ósea la capacidad de los microbios donantes para colonizar? La respuesta podría ayudar a diseñar terapias basadas en el microbioma más seguras y fiables.
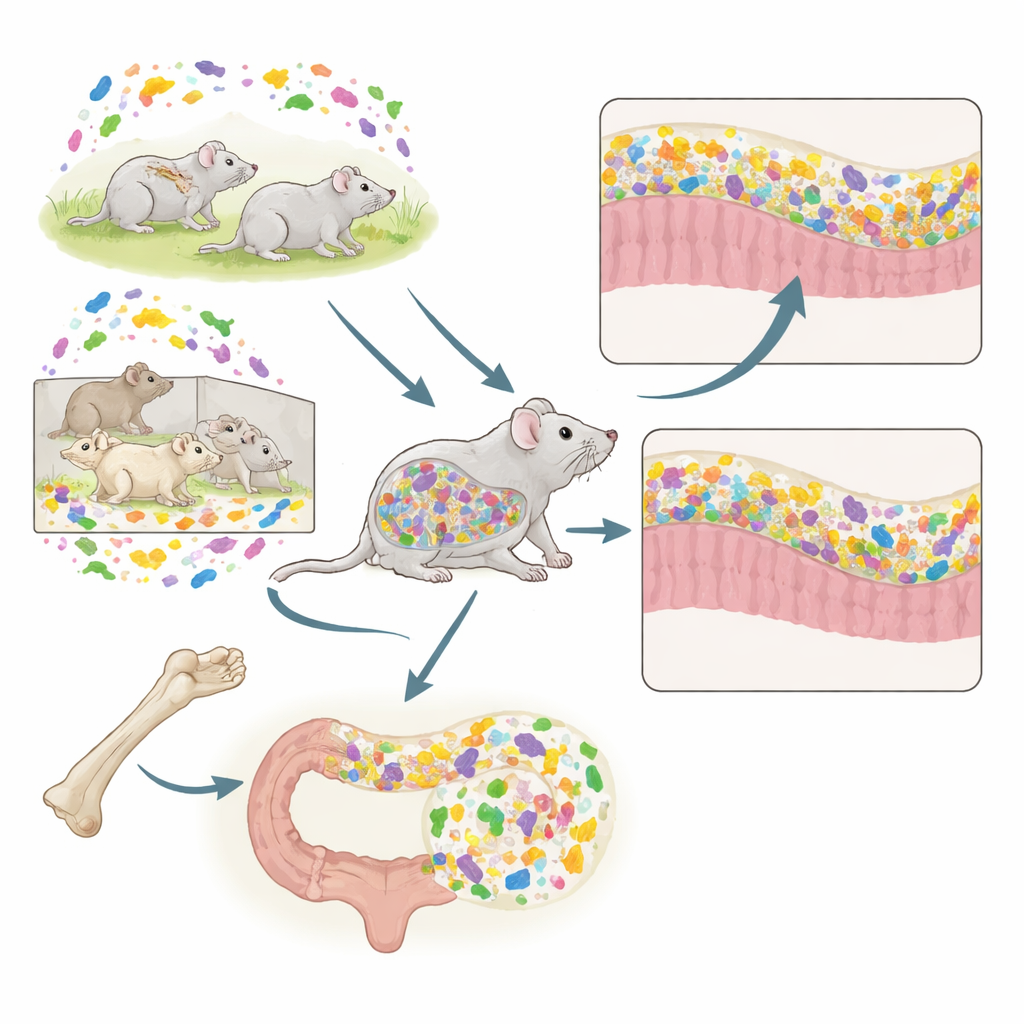
Dos trasplantes, un mismo ratón
Los investigadores combinaron dos herramientas potentes en ratones: el trasplante de médula ósea (TMO), que reemplaza las células inmunitarias, y el TMF, que reemplaza los microbios intestinales. Los ratones donantes procedían de dos condiciones de cría distintas. Los convencionales (CV) viven en jaulas abiertas estándar y albergan una microbiota rica y variada. Los libres de patógenos específicos (SPF) viven en instalaciones con barrera protectora y portan una comunidad microbiana más simple, menos diversa y un sistema inmunitario menos maduro. Los ratones receptores siempre vivían en condiciones convencionales pero recibieron médula ósea y/o heces de donantes CV o SPF en distintas combinaciones. Este diseño permitió al equipo probar cómo el trasfondo inmunitario modelado por el origen de la médula ósea interactuaba con los microbios fecales entrantes.
Comprobar quién se instala en el intestino
Una semana después del TMF, los científicos recogieron muestras fecales y analizaron el ADN bacteriano, centrándose en qué tipos de microbios estaban presentes y cuán abundantes eran. La diversidad global —la pura variedad y el equilibrio de microbios— no difirió mucho entre los grupos. Sin embargo, la estructura detallada de la comunidad sí lo hizo. Usando medidas de distancia que capturan qué especies están presentes (más que cuán dominantes son), encontraron que el origen del donante de médula ósea cambió de forma significativa el patrón de microbios que se establecieron tras el TMF. Estos efectos fueron más evidentes cuando el material fecal procedía de donantes convencionales, lo que sugiere que una mezcla microbiana más rica y compleja es particularmente sensible al entorno inmunitario fijado por la médula ósea.
Cambios funcionales ocultos en el metabolismo microbiano
Para ir más allá de “quién está ahí” y preguntar “qué podrían estar haciendo”, el equipo utilizó herramientas computacionales para predecir vías metabólicas a partir de los perfiles de ADN bacteriano. Cuando la médula ósea y las heces provenían ambas de donantes con el mismo tipo de microbiota (CV con CV, o SPF con SPF), las funciones predichas de la comunidad intestinal cambiaron de maneras consistentes. En ratones que recibieron material CV emparejado, las vías vinculadas a la síntesis de aminoácidos como la arginina y las poliaminas fueron más prominentes. En ratones con material SPF emparejado, se predijo un aumento en vías relacionadas con aminoácidos aromáticos como la tirosina y la fenilalanina. Estas predicciones son indirectas y requieren confirmación con análisis moleculares más profundos, pero sugieren que emparejar las fuentes de donante puede orientar sutilmente lo que los microbios trasplantados pueden producir.
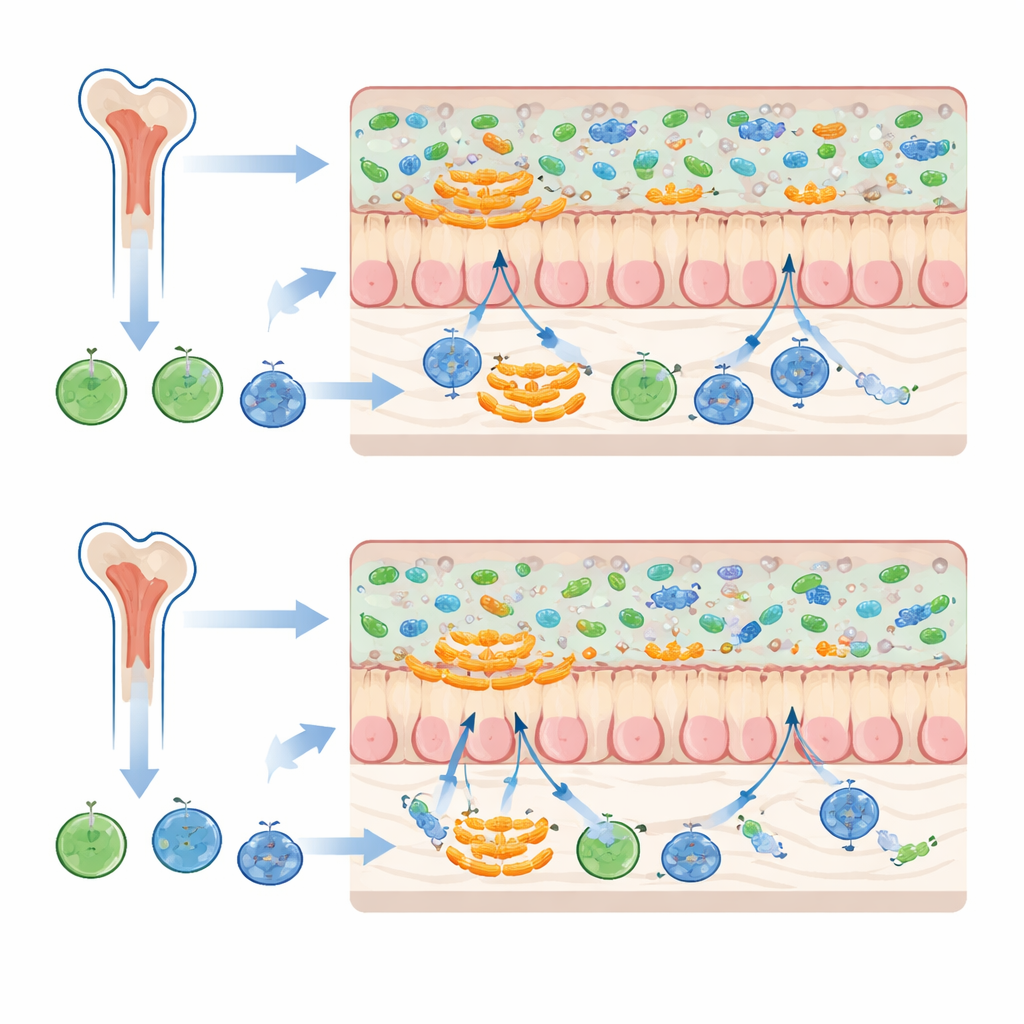
Un grupo especial de bacterias amantes del moco
Los cambios más llamativos involucraron a una familia de bacterias llamadas Muribaculaceae, que tienden a vivir cerca de la capa de moco intestinal en lugar de flotar libremente en el contenido intestinal. Cuando los ratones recibieron tanto médula ósea como heces de donantes con el mismo trasfondo microbiota, ciertas Muribaculaceae aumentaron su abundancia y la comunidad microbiana global de los receptores se pareció más a la de los donantes fecales. Cuando la médula ósea y las heces procedían de trasfondos microbiota distintos, estas bacterias se expandieron menos y las comunidades similares a las del donante se reprodujeron con menor fidelidad. Como los microbios asociados al moco están en la interfase entre el contenido intestinal y el revestimiento intestinal, pueden ser especialmente sensibles al tono inmunitario establecido por las células de la médula ósea derivadas del donante.
Qué significa esto para tratamientos futuros
En términos sencillos, el estudio sugiere que la “compatibilidad” entre el sistema inmunitario de una persona y los microbios intestinales entrantes puede influir en qué bacterias perduran tras un TMF, especialmente las que viven cerca de la pared intestinal. Emparejar el trasplante de médula ósea y las heces en ratones favoreció el crecimiento de ciertas bacterias que habitan el moco y ayudó a que las microbiotas de los receptores se parecieran más a las de sus donantes, aunque la diversidad global no cambiara de forma notable. Aunque la radiación y otros tratamientos previos al trasplante también afectan al intestino y no se separaron completamente aquí, estos resultados subrayan que la historia inmunitaria importa para las terapias del microbioma. A medida que el TMF y enfoques relacionados avancen en pacientes, especialmente en inmunocomprometidos, considerar con cuidado los emparejamientos donante–receptor podría hacer que estos tratamientos sean más predecibles y efectivos.
Cita: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Palabras clave: trasplante de microbiota fecal, trasplante de médula ósea, microbioma intestinal, sistema inmunitario, bacterias asociadas al moco