Clear Sky Science · de
Zusammenhang zwischen Herkunft des Knochenmarkspenders und der Zusammensetzung des Darmmikrobiota nach fäkaler Mikrobiota-Transplantation bei Mäusen
Warum die winzigen Bewohner des Darms wichtig sind
Ärzte verwenden zunehmend fäkale Mikrobiota-Transplantation (FMT) — die Übertragung von Stuhl eines gesunden Spenders auf einen Patienten — um die mikrobielle Gemeinschaft des Darms zurückzusetzen und hartnäckige Erkrankungen zu behandeln. Aber nicht jede Transplantation „nimmt“ in gleichem Maße an. Diese Mäusestudie stellt eine überraschend praktische Frage: Wenn ein Patient zuvor eine Knochenmarktransplantation erhalten hat und damit ein anderes Immunsystem besitzt, verändert die Herkunft dieses Knochenmarks, wie gut die Spender-Darmmikroben sich ansiedeln können? Die Antwort könnte helfen, sicherere und verlässlichere Microbiom-basierte Therapien zu entwickeln.
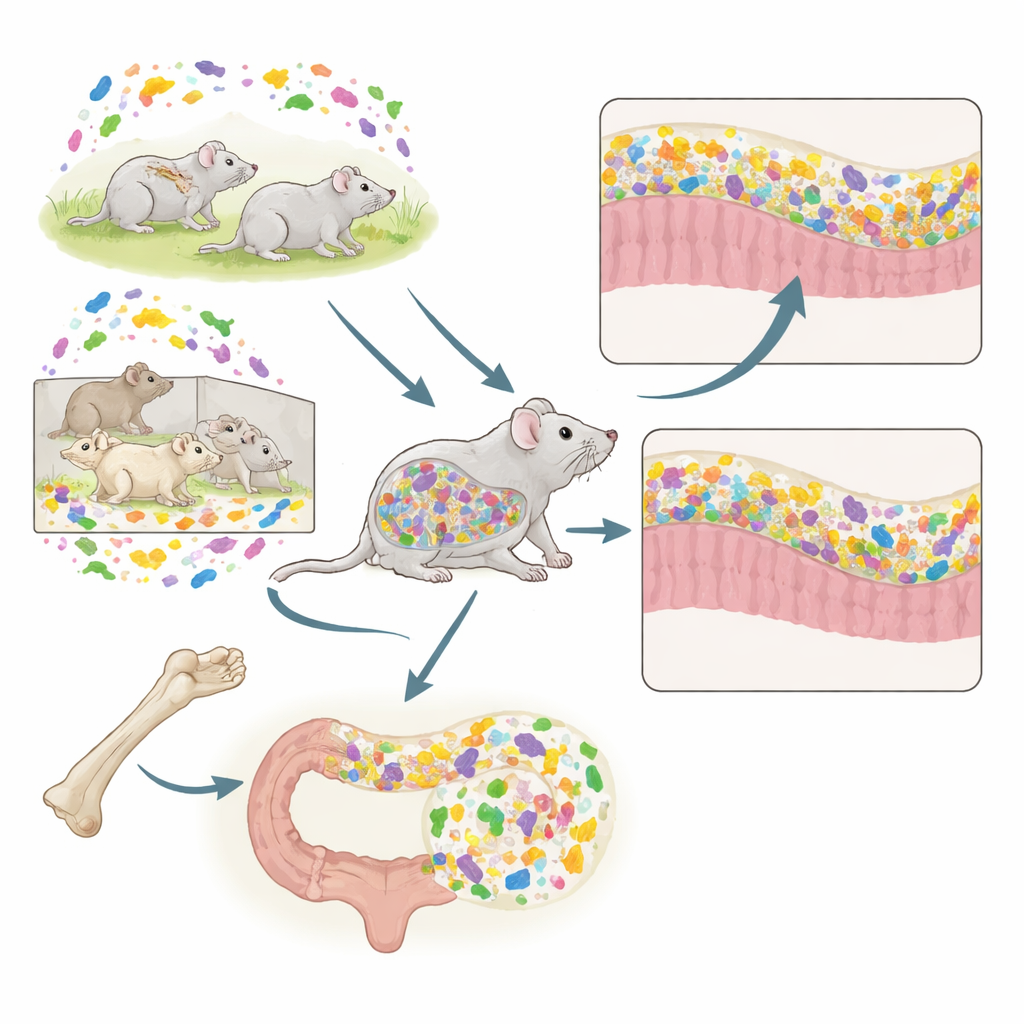
Zwei Transplantationen, eine Maus
Die Forschenden kombinierten in Mäusen zwei mächtige Werkzeuge: Knochenmarktransplantation (BMT), die Immunzellen ersetzt, und FMT, die Darmmikroben ersetzt. Spendermäuse stammten aus zwei unterschiedlichen Haltungsbedingungen. Konventionelle (CV) Mäuse leben in standardmäßigen offenen Käfigen und beherbergen ein reichhaltiges, vielfältiges Mikrobiom. Spezifisch-pathogenfrei (SPF) gehaltene Mäuse leben in geschützten Barrierestationen und tragen eine einfachere, weniger vielfältige mikrobielle Gemeinschaft und ein weniger ausgereiftes Immunsystem. Empfängermäuse lebten stets unter konventionellen Bedingungen, erhielten aber in unterschiedlichen Kombinationen Knochenmark und/oder Stuhl von CV- oder SPF-Spendern. Dieses Design ermöglichte dem Team zu testen, wie der durch die Herkunft des Knochenmarks geprägte Immunhintergrund mit den eintreffenden fäkalen Mikroben interagiert.
Nachsehen, wer sich im Darm niederlässt
Eine Woche nach der FMT sammelten die Wissenschaftler Kotproben und analysierten bakterielle DNA, wobei sie sich darauf konzentrierten, welche Mikrobenarten vorhanden waren und wie häufig sie auftraten. Die Gesamtdiversität — die reine Vielfalt und das Gleichgewicht der Mikroben — unterschied sich zwischen den Gruppen kaum. Die detaillierte Gemeinschaftsstruktur hingegen schon. Mit Distanzmaßen, die erfassen, welche Arten vorhanden sind (statt wie dominant jede ist), stellten sie fest, dass die Herkunft des Knochenmarkspenders das Muster der nach FMT etablierten Mikroben signifikant veränderte. Diese Effekte waren am deutlichsten, wenn das fäkale Material von konventionellen Spendern stammte, was darauf hindeutet, dass eine reichhaltigere, komplexere mikrobielle Mischung besonders empfindlich auf das vom Knochenmark gesetzte Immunumfeld reagiert.
Verborgene funktionelle Verschiebungen im mikrobiellen Stoffwechsel
Um über das „wer ist da“ hinauszugehen und zu fragen „was könnten sie tun“, nutzte das Team computergestützte Werkzeuge, um aus den bakteriellen DNA-Profilen vorhergesagte Stoffwechselwege zu rekonstruieren. Wenn Knochenmark und Stuhl beide von Spendern mit demselben Mikrobiota-Typ stammten (CV mit CV oder SPF mit SPF), verschoben sich die vorhergesagten Funktionen der Darmgemeinschaft auf konsistente Weise. Bei Mäusen, die abgestimmtes CV-Material erhielten, waren Wege, die mit dem Aufbau von Aminosäuren wie Arginin und Polyaminen verknüpft sind, stärker ausgeprägt. Bei Mäusen mit abgestimmtem SPF-Material wurden vermehrt Wege im Zusammenhang mit aromatischen Aminosäuren wie Tyrosin und Phenylalanin vorhergesagt. Diese Vorhersagen sind indirekt und müssen durch tiefere molekulare Analysen bestätigt werden, deuten aber darauf hin, dass das Abstimmen der Spenderquellen subtil beeinflussen kann, was die transplantierten Mikroben produzieren können.
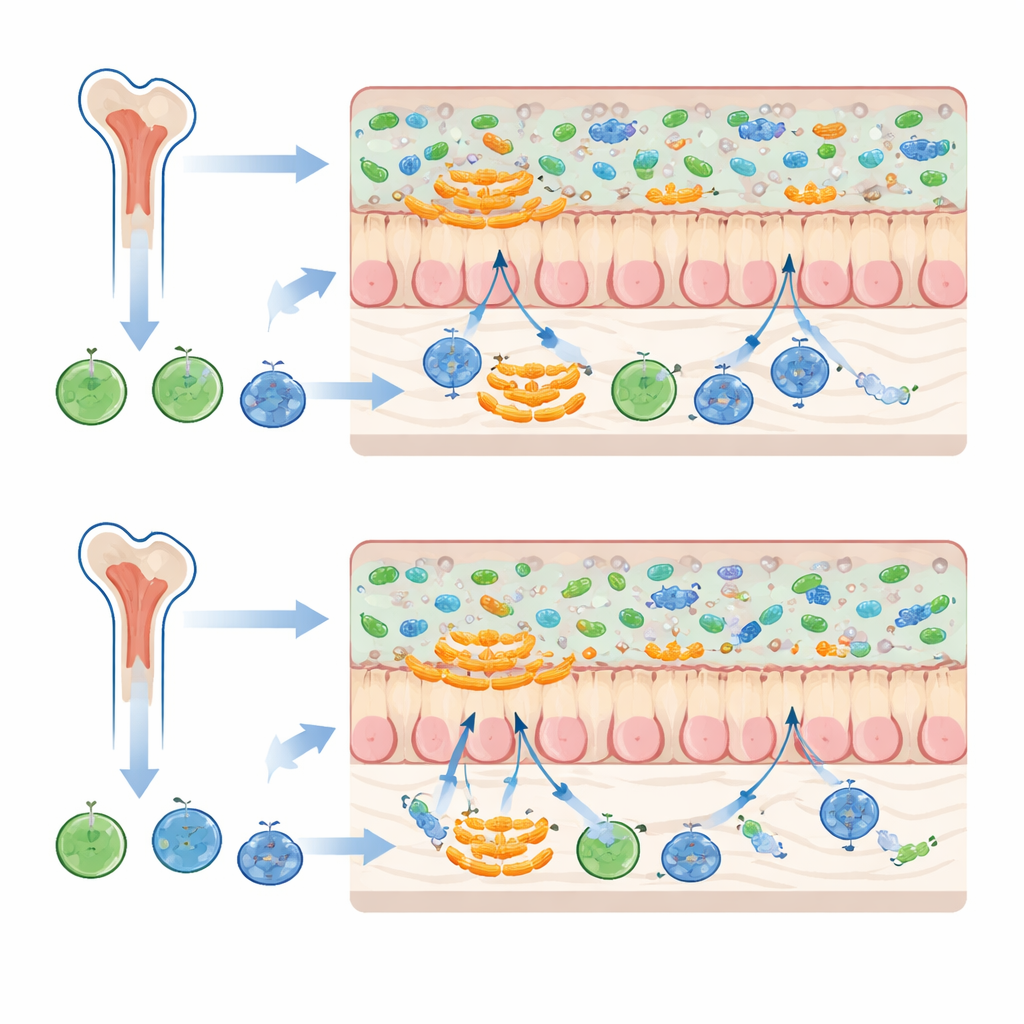
Eine besondere Gruppe schleimliebender Bakterien
Die auffälligsten Veränderungen betrafen eine Bakterienfamilie namens Muribaculaceae, die dazu neigen, nahe der Darmschleimschicht zu leben, statt frei im Darminhalt zu schweben. Wenn Mäuse sowohl Knochenmark als auch Stuhl von Spendern mit demselben Mikrobiota-Hintergrund erhielten, wurden bestimmte Muribaculaceae häufiger, und die gesamte mikrobielle Gemeinschaft der Empfänger ähnelte stärker der der Stuhlspender. Wenn Knochenmark und Stuhl aus unterschiedlichen Mikrobiota-Hintergründen stammten, vermehrten sich diese Bakterien weniger und spenderähnliche Gemeinschaften wurden weniger getreu reproduziert. Da schleimhautassoziierte Mikroben an der Schnittstelle zwischen Darminhalt und der Darmwand sitzen, könnten sie besonders empfindlich auf den Immunzustand reagieren, der durch donor-abgeleitete Knochenmarkzellen gesetzt wird.
Was das für künftige Behandlungen bedeutet
Einfach ausgedrückt legt die Studie nahe, dass die „Übereinstimmung“ zwischen dem Immunsystem einer Person und ihren eintreffenden Darmmikroben beeinflussen kann, welche Bakterien nach einer FMT bestehen bleiben — besonders diejenigen, die in der Nähe der Darmwand leben. Das Abstimmen von Knochenmark- und Stuhlspenderhintergründen bei Mäusen begünstigte das Wachstum bestimmter schleimbewohnender Bakterien und half den Empfängermikrobiota, ihre Spender stärker zu spiegeln, obwohl sich die Gesamtdiversität nicht dramatisch veränderte. Während Bestrahlung und andere Vorbehandlungen den Darm ebenfalls beeinflussen und hier nicht vollständig getrennt wurden, heben diese Ergebnisse hervor, dass die Immunvorgeschichte für Mikrobiomtherapien wichtig ist. Wenn FMT und verwandte Ansätze bei Patienten voranschreiten, insbesondere bei immunsupprimierten Personen, könnte eine sorgfältige Berücksichtigung von Spender–Empfänger-Kombinationen diese Behandlungen vorhersagbarer und wirksamer machen.
Zitation: Ichimura, R., Tanaka, K., Song, I. et al. Association between bone marrow donor origin and gut microbiota composition following fecal microbiota transplantation in mice. Sci Rep 16, 13314 (2026). https://doi.org/10.1038/s41598-026-36933-0
Schlüsselwörter: fäkale Mikrobiota-Transplantation, Knochenmarktransplantation, Darmmikrobiom, Immunsystem, schleimhautassoziierte Bakterien