Clear Sky Science · zh
栖居血管的巨噬细胞保护斑马鱼的血液和血管完整性
血流中的隐秘守护者
每一秒,血液都在一张庞大的血管网络中奔流,即便在微小的动物体内,将这些血管首尾相连也能延伸数英里。我们依赖这条隐形高速公路输送氧气、营养和免疫细胞。然而,有一个基本问题长期未被清楚回答:谁在持续检查血液本身的质量并保护脆弱的血管壁?这项在透明斑马鱼胚胎中开展并扩展到小鼠的研究,发现了一类此前未被认识的免疫细胞,它们生活在血管内部,充当在位的检查员和循环系统的清道夫。
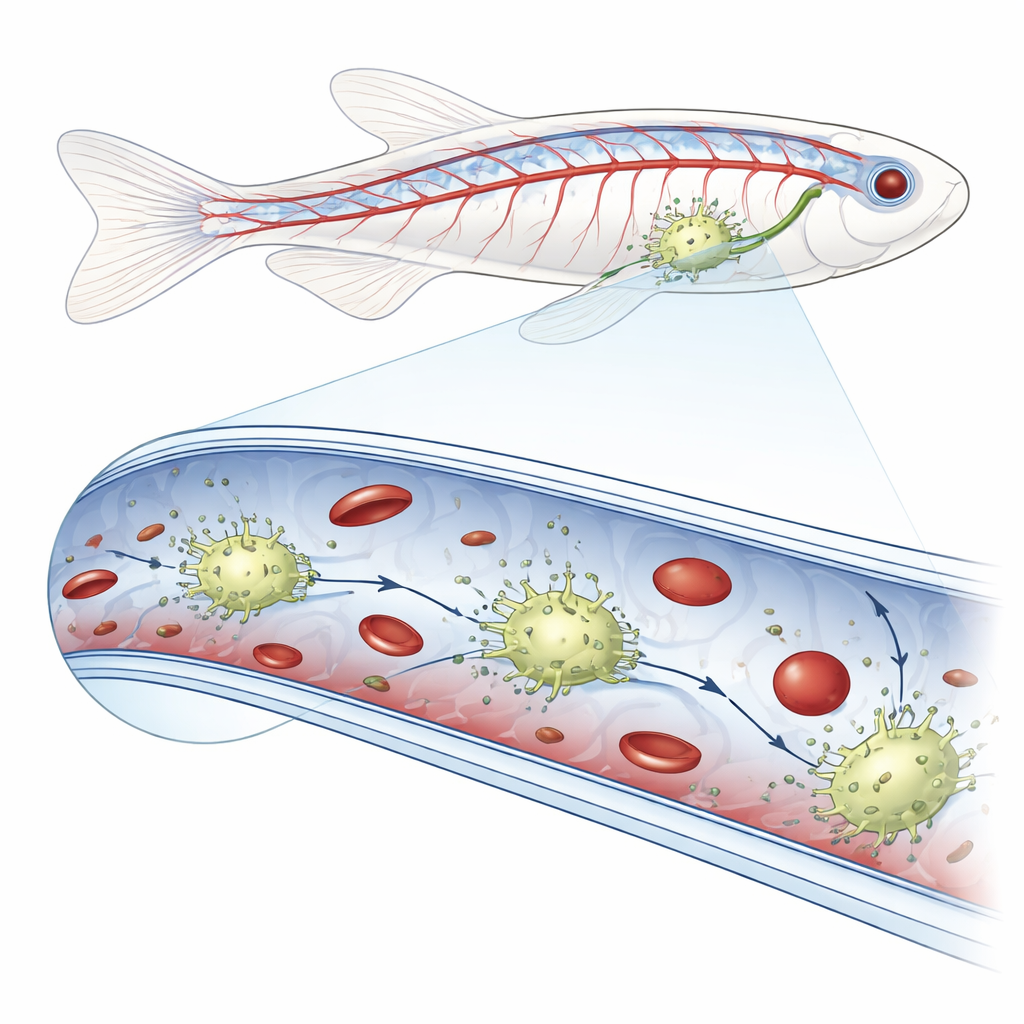
血管内部的新巡逻细胞
研究者在斑马鱼胚胎中使用高分辨率活体成像,注意到尾部静脉内表面爬行着一些异常明亮的细胞。当他们向血流中注入荧光细菌、真菌颗粒、合成微球或供体红细胞时,这些血管内细胞是唯一吞噬外来物质的细胞。精细的基因标记显示,这些细胞同时具有血管内皮细胞和经典吞噬性免疫细胞——巨噬细胞的特征。由于它们居住在血管内部而非周围组织,研究组将其命名为血管驻留巨噬细胞,或称 bMΦs。
这些细胞如何监视并清理血液
特写时间推移录像显示,bMΦs 以类变形虫的方式沿血管内膜爬行,有时短暂阻碍血流,表明它们与血管牢固附着。它们的表面布满细长灵活的突起,帮助它们抓住血管壁并捕捉通过的颗粒。当研究者用药物破坏这些细胞的细胞骨架时,这些突起消失,bMΦs 从血管表面脱落,无法有效清除注入的颗粒,颗粒因此在循环中自由漂浮。此类细胞还与机体自身的血细胞相互作用:它们抓住经过的红细胞以及造血干/祖细胞,在表面检查后要么完整释放,要么吞噬那些体积异常或形态异常的细胞,从而帮助维持血液质量。
受损血管的第一响应者
除了日常清理外,bMΦs 在血管受损时还充当快速的第一响应者。研究者使用一种光遗传学工具——本质上是一个受光激活的分子开关——触发少量被选择的内皮细胞死亡,这些内皮细胞构成血管壁。在这种针对性损伤发生后,bMΦs 立即赶到现场并高效清除死亡细胞碎片。相比之下,传统的组织巨噬细胞和快速移动的中性粒细胞到达得较少、在损伤处停留时间更短且几乎不进行清理。这些观察表明,bMΦs 在血管内部具有特殊的位置和装备,能够从血内感知异常并维护血液—血管界面的清洁与完整。
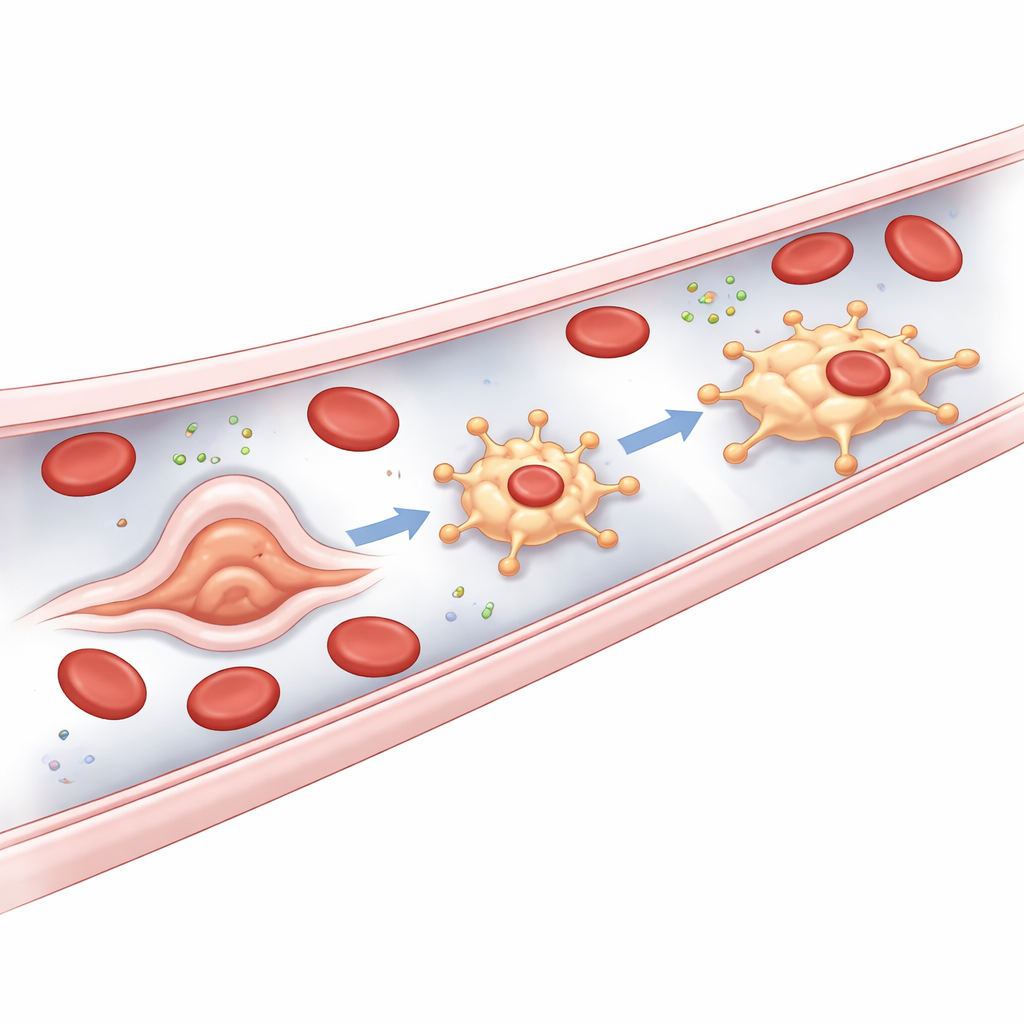
这些守护者的来源
研究的一个关键惊讶在于 bMΦs 的起源。大多数组织驻留的巨噬细胞来自早期的造血前体或后期的骨髓细胞。相比之下,bMΦs 似乎直接从血管内膜萌生。在斑马鱼胚胎中,在血流开始不久后,主干血管,尤其是尾静脉丛中的某些内皮细胞发生快速的形态变化,向血管腔突出,然后脱落成为自由运动的 bMΦs。作者将这一不寻常过程称为内皮向巨噬细胞转变(endothelial‑to‑macrophage transition)。该过程依赖于已知的髓系免疫谱系调控因子,但显著的是,它并不需要通常对将血管细胞转化为造血干细胞至关重要的 Runx1。这使得 bMΦs 成为斑马鱼中不同于前三条路径的第四条巨噬细胞发生路线。
跨物种的保守作用与未来前景
为了确定类似细胞是否存在于哺乳动物中,研究组向小鼠血液中注入真菌颗粒并检查哪些细胞将其吞噬。他们发现了一小群稀有的循环细胞,与斑马鱼的 bMΦs 类似,这些细胞吞噬能力强,表面同时表达免疫和血管相关标志,并在显微镜下显示触手状延伸。这些细胞有别于已知的单核细胞和中性粒细胞群体,提示 bMΦs 样的守护者在进化上是保守的。有趣的是,即便缺失一个对大多数其他巨噬细胞通常必需的关键受体,这类细胞仍然可以发育并发挥功能,这也许解释了它们长期未被发现。总体而言,这些发现重绘了我们对血液与血管如何被监视的认知,并暗示未来可能利用或工程化这些驻留巡逻细胞来治疗血流传播的感染或损伤血管内壁的疾病。
这对我们的健康意味着什么
通俗来说,这项工作表明我们的血管内有自身的内置保安。这些保安以出人意料的方式由血管壁产生,定居于内表面,并持续检查血液和血管内膜以发现问题——清除病原体和有缺陷的细胞,并在受损后进行清理。通过揭示这一在鱼类和小鼠中被忽视的防护层,该研究为未来可能增强或模拟这些细胞的疗法打开了大门,以在从血流感染到血管损伤和心血管疾病等多种状况下保持血液更清洁、血管更健康。
引用: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
关键词: 巨噬细胞, 血管, 免疫监视, 斑马鱼, 血管生物学