Clear Sky Science · de
Gefäßansässige Makrophagen schützen Blut und Gefäßintegrität bei Zebrafisch
Verborgene Wächter in unserem Blutstrom
Sekunden für Sekunde fließt Blut durch ein riesiges Gefäßnetz, das selbst bei einem kleinen Tier, aneinandergereiht, viele Meilen lang wäre. Wir sind auf diese verborgene Autobahn angewiesen, damit Sauerstoff, Nährstoffe und Immunzellen transportiert werden. Doch eine grundlegende Frage blieb überraschend unklar: Wer kontrolliert kontinuierlich die Qualität des Bluts selbst und schützt die empfindlichen Gefäßwände? Diese Studie, durchgeführt an transparenten Zebrafischembryonen und auf Mäuse ausgeweitet, deckt einen zuvor unerkannten Typ von Immunzellen auf, der innerhalb der Blutgefäße lebt und als Inspektor und Reiniger direkt am Ort des Geschehens für den Kreislauf fungiert.
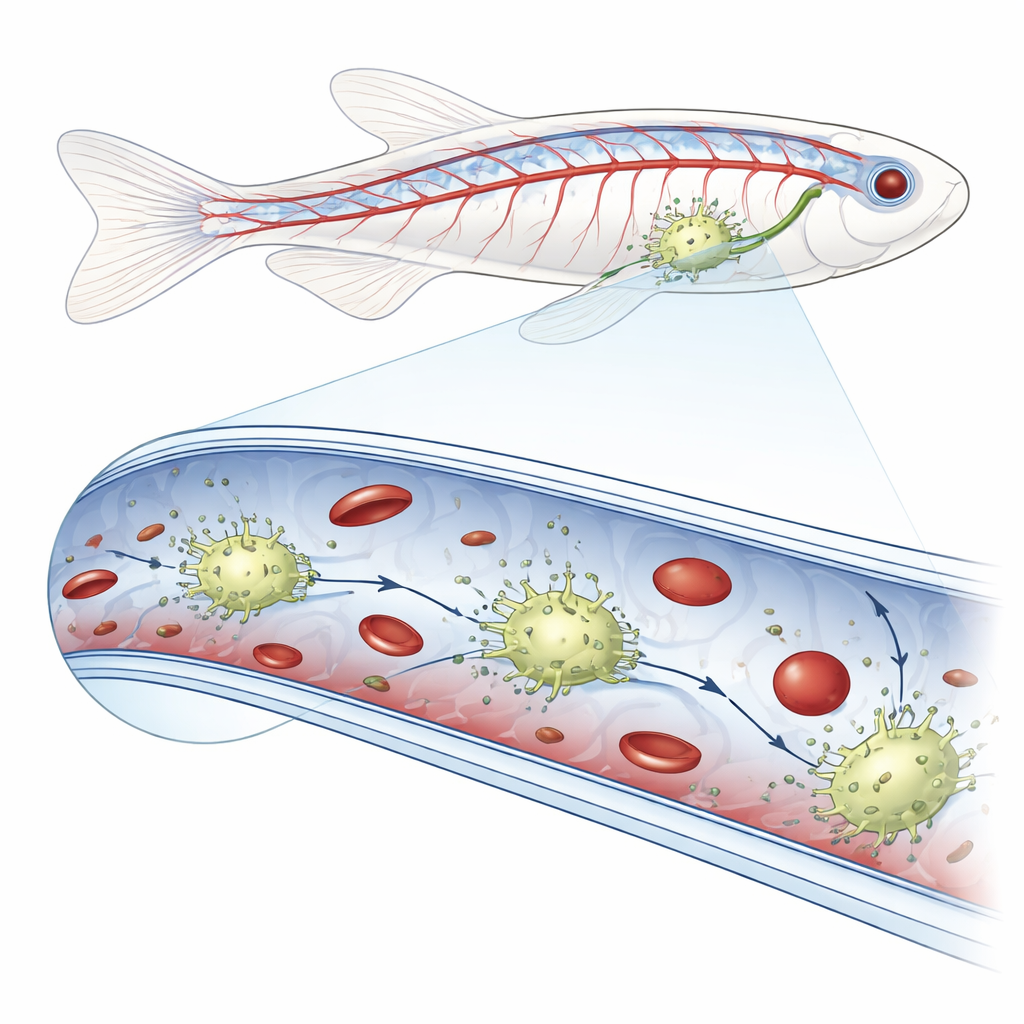
Neue Patrouillenzellen innerhalb von Blutgefäßen
Mithilfe hochaufgelöster Live‑Bildgebung in Zebrafischembryonen entdeckten die Forschenden ungewöhnlich helle Zellen, die entlang der inneren Oberfläche von Venen im Schwanzbereich krabbelten. Als sie fluoreszierende Bakterien, Pilzpartikel, synthetische Kügelchen oder gespendete rote Blutkörperchen in den Blutkreislauf injizierten, waren diese intravaskulären Zellen die einzigen, die das fremde Material aufnahmen. Sorgfältige genetische Markierungen zeigten, dass diese Zellen Merkmale sowohl von gefäßauskleidenden Zellen als auch von klassischen immunologischen Fressern, den Makrophagen, trugen. Da sie im Gefäßinneren und nicht im umliegenden Gewebe wohnen, nannten die Autoren sie gefäßansässige Makrophagen, oder bMΦs.
Wie diese Zellen Blut überwachen und reinigen
Detailaufnahmen als Zeitrafferfilme zeigten, dass bMΦs sich am Gefäßinnenrand amoeboide bewegen und dabei die Strömung manchmal kurz blockieren, ein Zeichen starker Anhaftung. Ihre Oberfläche ist mit dünnen, flexiblen Fortsätzen besetzt, die ihnen helfen, an der Wand Halt zu finden und vorbeiziehendes Material zu erfassen. Wenn die Forschenden das innere Gerüst der Zellen mit einem Medikament zerstörten, verschwanden diese Fortsätze, bMΦs lösten sich von der Gefäßoberfläche und konnten injizierte Partikel nicht mehr effizient entfernen, die dann frei im Kreislauf trieben. Die Zellen interagierten auch mit den körpereigenen Blutzellen: Sie griffen vorbeiziehende rote Blutkörperchen sowie blutbildende Stamm‑ und Vorläuferzellen, untersuchten sie an der Oberfläche und setzten sie entweder unversehrt wieder frei oder verschlangen solche, die ungewöhnlich groß oder anderweitig auffällig waren, wodurch die Blutqualität erhalten blieb.
Ersthelfer bei Gefäßverletzungen
Über die alltägliche Reinigung hinaus agieren bMΦs auch als schnelle Ersthelfer, wenn Gefäße beschädigt werden. Die Forschenden nutzten ein optogenetisches Werkzeug—im Grunde einen lichtaktivierbaren molekularen Schalter—um den Tod einiger ausgewählter Endothelzellen, die die Gefäßwand bilden, auszulösen. Unmittelbar nach dieser gezielten Verletzung stürmten bMΦs zur Stelle und entfernten effizient die sterbenden Zellfragmente. Traditionelle Gewebs‑Makrophagen und schnell bewegliche weiße Blutkörperchen, die Neutrophilen, trafen seltener ein, verweilten kürzer an der Schadensstelle und führten wenig Aufräumarbeiten durch. Diese Beobachtungen deuten darauf hin, dass bMΦs besonders positioniert und ausgestattet sind, um Probleme von innen im Gefäß wahrzunehmen und die Sauberkeit und Integrität der Blut‑Gefäß‑Grenzfläche zu erhalten.
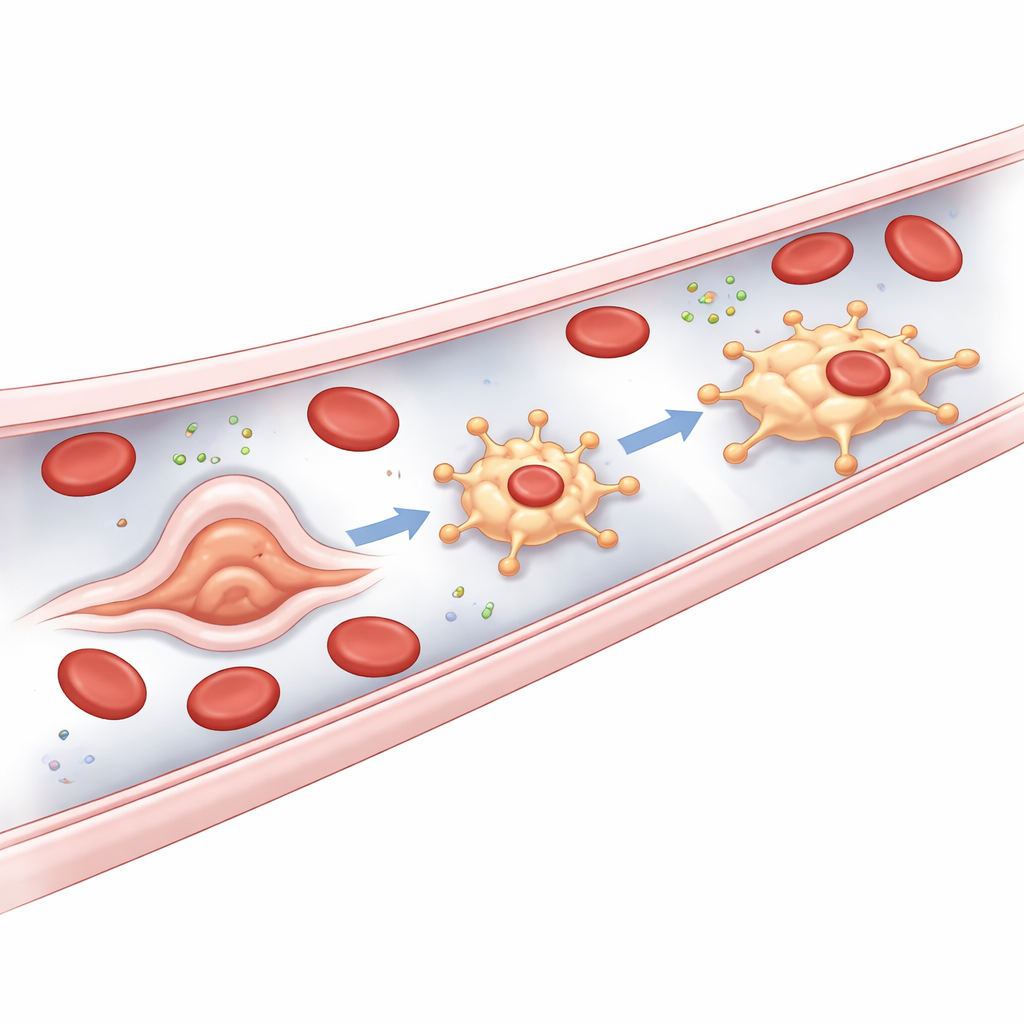
Woher diese Wächter stammen
Eine wichtige Überraschung der Studie ist die Herkunft der bMΦs. Die meisten gewebsansässigen Makrophagen entstehen aus frühen Blutvorläufern oder später aus Knochenmarkszellen. Im Kontrast dazu scheinen bMΦs direkt aus der Gefäßauskleidung zu entspringen. Bei Zebrafischembryonen, kurz nachdem der Blutfluss begonnen hat, verändern sich bestimmte Endothelzellen in den Hauptstammgefäßen und besonders im Schwanzvenenplexus rasch in ihrer Form, wölben sich in das Gefäß hinein und lösen sich dann als frei bewegliche bMΦs ab. Die Autoren bezeichnen diesen ungewöhnlichen Prozess als endothel‑zu‑Makrophagen‑Transition. Er hängt von bekannten Regulatoren der myeloiden Immunlinie ab, erfordert aber auffälligerweise nicht Runx1, einen Schlüsselschalter, der normalerweise für die Umwandlung von Gefäßzellen in blutbildende Stammzellen nötig ist. Das kennzeichnet bMΦs als eine eigenständige, vierte Entwicklungsroute für Makrophagen beim Zebrafisch.
Erhalteneres Merkmal über Arten hinweg und zukünftige Perspektiven
Um zu untersuchen, ob ähnliche Zellen bei Säugetieren existieren, injizierte das Team Pilzpartikel in das Blut von Mäusen und untersuchte, welche Zellen diese aufnahmen. Sie fanden eine seltene Gruppe zirkulierender Zellen, die wie die Zebrafisch‑bMΦs effiziente Fresser waren, eine Mischung aus Immun‑ und gefäßassoziierten Oberflächenmarkern trugen und unter dem Mikroskop tentakelartige Ausstülpungen zeigten. Diese Zellen unterschieden sich von bekannten Monozyten‑ und Neutrophilenpopulationen, was darauf hindeutet, dass bMΦ‑ähnliche Wächter evolutionär konserviert sind. Interessanterweise entwickeln und funktionieren sie selbst dann, wenn ein wichtiger Rezeptor fehlt, der normalerweise für die meisten anderen Makrophagen erforderlich ist, was erklären könnte, warum sie so lange unentdeckt blieben. Insgesamt zeichnen die Ergebnisse ein neues Bild davon, wie Blut und Gefäße überwacht werden, und deuten darauf hin, dass man eines Tages diese ansässigen Patrouillenzellen nutzen oder gezielt erzeugen könnte, um Blutbahninfektionen oder Erkrankungen zu behandeln, die die Gefäßauskleidung schädigen.
Was das für unsere Gesundheit bedeutet
Alltäglich gesprochen zeigt diese Arbeit, dass unsere Blutgefäße eigene eingebaute Sicherheitswächter beherbergen. Diese Wächter entstehen auf überraschende Weise aus der Gefäßwand, setzen sich an der Innenfläche fest und inspizieren kontinuierlich sowohl das Blut als auch die Auskleidung auf Probleme—sie entfernen Keime und defekte Zellen und räumen nach Verletzungen auf. Indem die Studie diese bisher übersehene Schutzschicht sowohl in Fischen als auch in Mäusen sichtbar macht, ebnet sie den Weg für künftige Therapien, die diese Zellen stärken oder nachahmen könnten, um das Blut sauberer und die Gefäße gesünder zu halten, sei es bei Blutbahninfektionen, Gefäßverletzungen oder Herz‑Kreislauf‑Erkrankungen.
Zitation: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Schlüsselwörter: Makrophagen, Blutgefäße, Immunüberwachung, Zebrafisch, Gefäßbiologie