Clear Sky Science · fr
Les macrophages résidents des vaisseaux sanguins préservent l’intégrité du sang et des parois vasculaires chez le poisson zèbre
Gardiens discrets dans notre circulation
Chaque seconde, le sang circule dans un vaste réseau de vaisseaux qui, alignés bout à bout, s’étendraient sur des kilomètres même chez un petit animal. Nous dépendons de cette voie cachée pour transporter l’oxygène, les nutriments et les cellules immunitaires. Pourtant, une question fondamentale est demeurée étonnamment floue : qui contrôle en continu la qualité du sang lui‑même et protège les parois vasculaires délicates ? Cette étude, menée chez des embryons de poisson zèbre transparents puis étendue à la souris, met au jour un type de cellule immunitaire jusqu’ici méconnu qui vit à l’intérieur des vaisseaux sanguins et fait office d’inspecteur et de nettoyeur de la circulation sur place.
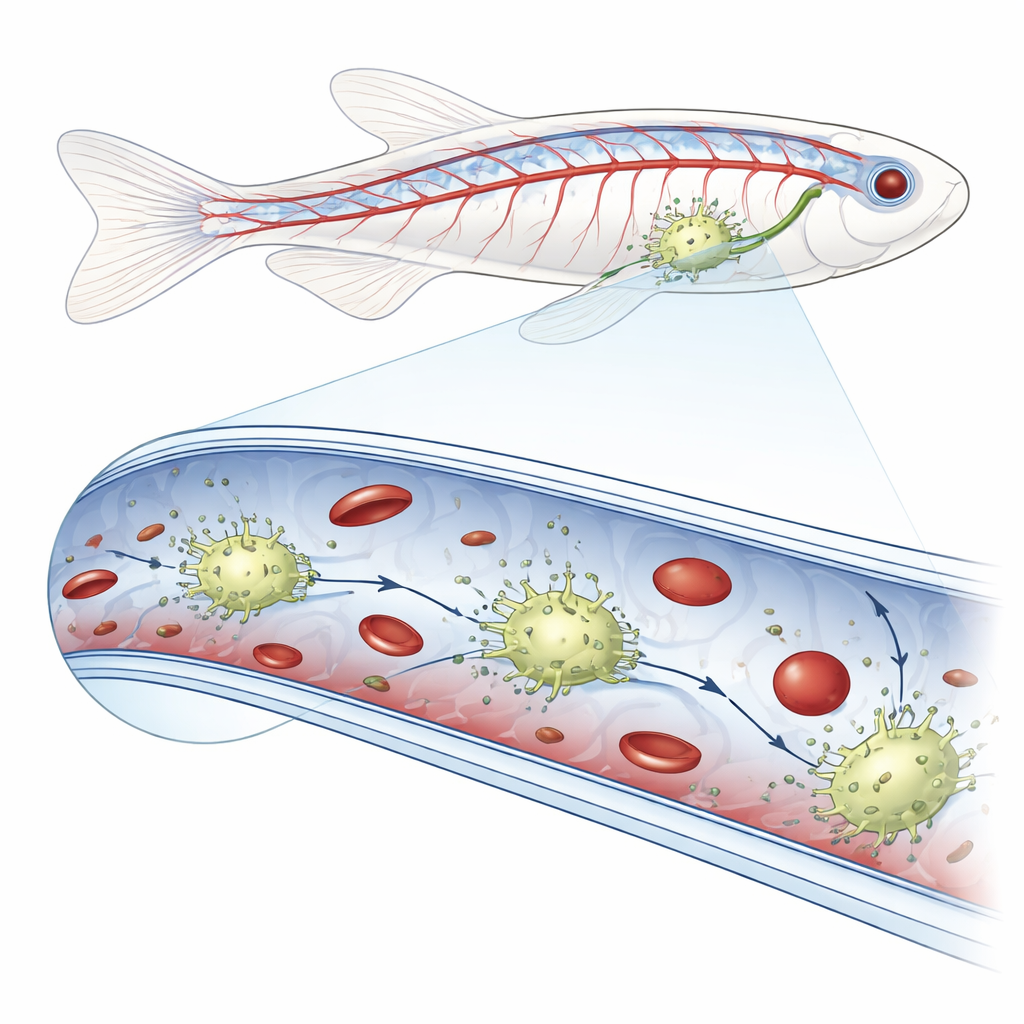
De nouvelles cellules de patrouille à l’intérieur des vaisseaux
Grâce à l’imagerie vive à haute résolution chez l’embryon de poisson zèbre, les chercheurs ont repéré des cellules d’une luminosité inhabituelle qui rampent le long des surfaces internes des veines de la région caudale. Lorsqu’ils ont injecté des bactéries fluorescentes, des particules fongiques, des billes synthétiques ou des globules rouges donneurs dans le courant sanguin, ces cellules intravasculaires ont été les seules à engloutir le matériel étranger. Un marquage génétique précis a montré que ces cellules portaient des caractéristiques à la fois des cellules qui tapissent les vaisseaux et des phagocytes classiques appelés macrophages. Parce qu’elles résident à l’intérieur des vaisseaux et non dans les tissus environnants, l’équipe les a nommées macrophages résidents des vaisseaux sanguins, ou bMΦ.
Comment ces cellules surveillent et nettoient le sang
Des films en chronophotographie rapprochés ont révélé que les bMΦ rampent de façon amiboïde le long de l’endothélium, bloquant parfois brièvement l’écoulement, signe d’une attache forte. Leur surface est hérissée de fines protrusions flexibles qui les aident à s’accrocher à la paroi et à saisir le matériel qui passe. Lorsque l’équipe a perturbé le cytosquelette interne de ces cellules avec un médicament, ces protrusions ont disparu, les bMΦ se sont détachés de la paroi et n’ont plus pu éliminer efficacement les particules injectées, qui ont alors dérivé librement dans la circulation. Ces cellules interagissaient aussi avec les propres cellules sanguines de l’animal : elles saisissaient les globules rouges et les cellules souches et progénitrices hématopoïétiques en passage, les examinaient à la surface puis les relâchaient indemnes ou engloutissaient celles qui semblaient anormalement grandes ou altérées, contribuant ainsi à maintenir la qualité du sang.
Premiers intervenants lors d’une lésion vasculaire
Au‑delà du nettoyage quotidien, les bMΦ jouent aussi le rôle d’intervenants rapides lorsque les vaisseaux sont endommagés. Les chercheurs ont utilisé un outil optogénétique — essentiellement un interrupteur moléculaire activable par la lumière — pour déclencher la mort de quelques cellules endothéliales ciblées, qui forment la paroi du vaisseau. Immédiatement après cette lésion ciblée, les bMΦ ont afflué vers le site et ont éliminé efficacement les débris cellulaires en train de mourir. Les macrophages tissulaires traditionnels et les globules blancs rapides appelés neutrophiles arrivaient moins souvent, restaient moins longtemps sur le lieu du dommage et assuraient peu le nettoyage. Ces observations suggèrent que les bMΦ sont spécialement positionnés et équipés pour détecter les problèmes depuis l’intérieur du vaisseau et préserver la propreté et l’intégrité de l’interface sang–vaisseau.
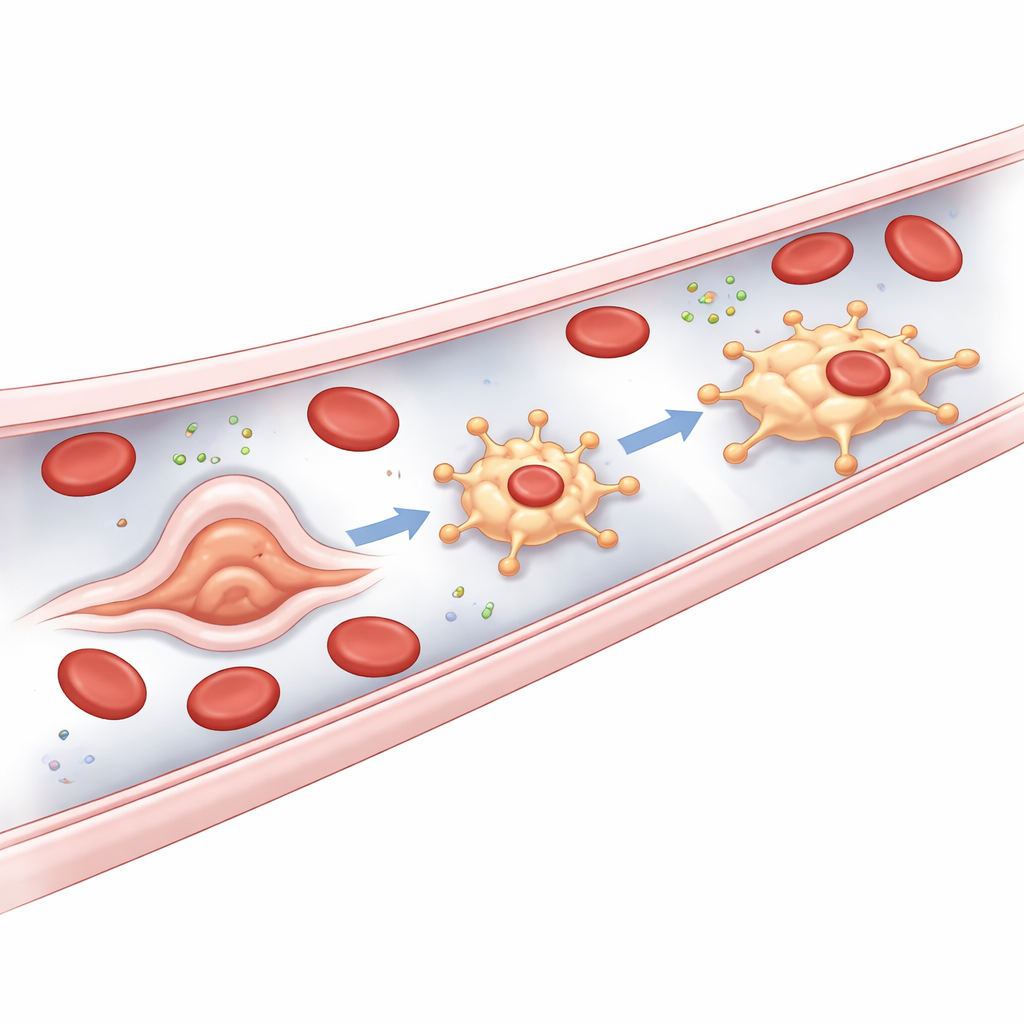
Origine de ces gardiens
Une surprise majeure de l’étude porte sur l’origine des bMΦ. La plupart des macrophages résidents tissulaires proviennent d’ancêtres sanguins précoces ou de cellules médullaires plus tardives. En revanche, il semble que les bMΦ bourgeonnent directement à partir de l’endothélium lui‑même. Chez les embryons de poisson zèbre, peu après le début du flux sanguin, certaines cellules endothéliales des vaisseaux principaux, et particulièrement du plexus veineux caudal, subissent un changement morphologique rapide, faisant saillie dans la lumière du vaisseau puis se détachant pour devenir des bMΦ mobiles. Les auteurs qualifient ce processus inhabituel de transition endothéliale‑vers‑macrophage. Il dépend de régulateurs bien connus de la lignée myéloïde, mais, de façon frappante, ne requiert pas Runx1, un commutateur maître normalement essentiel à la transformation des cellules vasculaires en cellules souches hématopoïétiques. Cela distingue les bMΦ comme une quatrième voie développementale distincte pour les macrophages chez le poisson zèbre.
Rôle conservé entre espèces et perspectives
Pour savoir si des cellules similaires existent chez les mammifères, l’équipe a injecté des particules fongiques dans le sang de souris et examiné quelles cellules les engloutissaient. Ils ont identifié un groupe rare de cellules circulantes qui, comme les bMΦ du poisson zèbre, étaient efficaces pour phagocyter, portaient un mélange de marqueurs de surface associés à l’immunité et aux vaisseaux et montraient au microscope des extensions en forme de tentacules. Ces cellules se distinguaient des populations connues de monocytes et de neutrophiles, suggérant que des gardiens de type bMΦ sont conservés au cours de l’évolution. Fait intrigant, elles se développent et fonctionnent même en l’absence d’un récepteur clé normalement requis par la plupart des autres macrophages, ce qui pourrait expliquer pourquoi elles sont restées longtemps inaperçues. Ensemble, ces résultats redessinent notre vision de la surveillance du sang et des vaisseaux, et laissent entrevoir la possibilité de mobiliser ou d’ingénier ces cellules résidentes de patrouille pour traiter des infections sanguines ou des maladies qui endommagent l’endothélium.
Implications pour notre santé
Concrètement, ce travail montre que nos vaisseaux sanguins abritent leurs propres gardes‑sécurité intégrés. Ces gardiens naissent d’une manière inattendue à partir de la paroi vasculaire, s’installent sur la surface interne et inspectent en continu le sang et l’endothélium à la recherche de signes de trouble — éliminant germes et cellules défectueuses et nettoyant après une lésion. En révélant cette couche de protection négligée chez le poisson et la souris, l’étude ouvre la voie à des thérapies futures visant à renforcer ou à reproduire ces cellules afin de garder le sang plus propre et les vaisseaux en meilleure santé dans des situations allant des infections sanguines aux lésions vasculaires et aux maladies cardiovasculaires.
Citation: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Mots-clés: macrophages, vaisseaux sanguins, surveillance immunitaire, poisson zèbre, biologie vasculaire