Clear Sky Science · it
I macrofagi residenti nei vasi salvaguardano l’integrità del sangue e dei vasi nei pesci zebra
Guardiani nascosti nel nostro flusso sanguigno
Ogni secondo il sangue scorre attraverso un’immensa rete di vasi che, messi uno dopo l’altro, si estenderebbero per chilometri anche in un animale minuscolo. Facciamo affidamento su questa autostrada nascosta per trasportare ossigeno, nutrienti e cellule immunitarie. Eppure una domanda fondamentale è rimasta sorprendentemente poco chiara: chi controlla costantemente la qualità stessa del sangue e protegge le pareti dei vasi, così delicate? Questo studio, condotto in embrioni trasparenti di pesce zebra e esteso ai topi, scopre un tipo di cellula immunitaria finora non riconosciuta che vive all’interno dei vasi sanguigni e agisce come ispettore e pulitore in loco della circolazione.
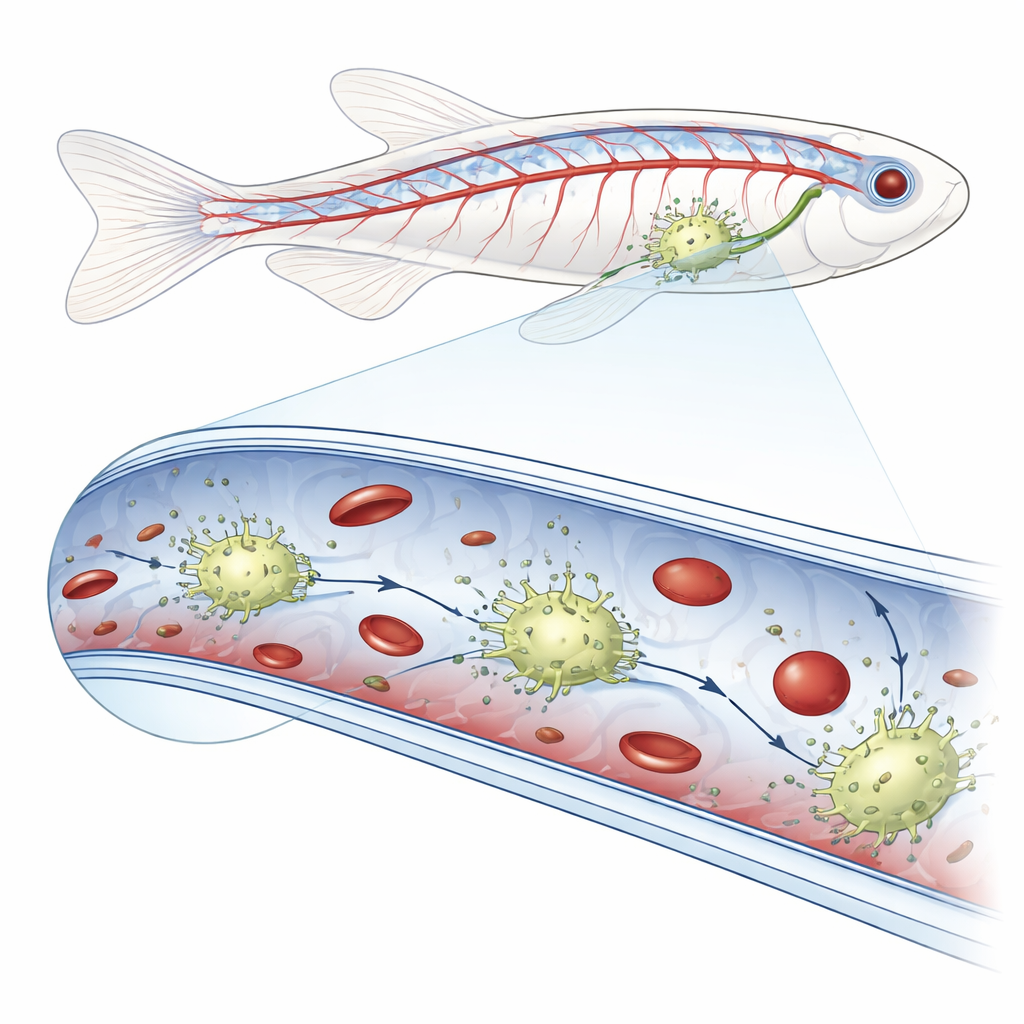
Nuove cellule di pattuglia all’interno dei vasi
Usando immagini live ad alta risoluzione negli embrioni di pesce zebra, i ricercatori hanno notato cellule insolitamente brillanti che si muovevano lungo le superfici interne delle vene nella regione della coda. Quando hanno iniettato batteri fluorescenti, particelle fungine, sfere sintetiche o globuli rossi donatori nella circolazione, queste cellule intravascolari sono state le sole a ingerire il materiale estraneo. Un’attenta marcatura genetica ha mostrato che queste cellule presentavano caratteristiche sia delle cellule che rivestono i vasi sia dei classici mangiatori immunitari noti come macrofagi. Poiché risiedono all’interno dei vasi piuttosto che nei tessuti circostanti, il gruppo le ha chiamate macrofagi residenti nei vasi sanguigni, o bMΦ.
Come queste cellule sorvegliano e puliscono il sangue
Filmati ravvicinati in time‑lapse hanno rivelato che i bMΦ strisciano in modo amoeboide lungo il rivestimento vascolare, talvolta bloccando brevemente il flusso, segno di forte attacco. Le loro superfici sono ricoperte di sottili ed elastiche protrusioni che li aiutano ad aggrapparsi alla parete e afferrare il materiale che passa. Quando il team ha distrutto l’impalcatura interna delle cellule con un farmaco, queste protrusioni sono scomparse, i bMΦ si sono staccati dalla superficie vascolare e non hanno più potuto eliminare efficacemente le particelle iniettate, che così sono rimaste a galleggiare liberamente nella circolazione. Le cellule interagivano anche con le cellule del sangue dell’animale: afferravano i globuli rossi e le cellule staminali e progenitrici ematopoietiche in transito, le esaminavano sulla superficie e poi o le rilasciavano integre o inglobavano quelle che apparivano insolitamente grandi o anormali, contribuendo a mantenere la qualità del sangue.
Primi soccorritori in caso di lesione vascolare
Oltre alla pulizia quotidiana, i bMΦ agiscono anche come primi soccorritori rapidi quando i vasi vengono danneggiati. I ricercatori hanno usato uno strumento optogenetico — sostanzialmente un interruttore molecolare attivato dalla luce — per indurre la morte di alcune cellule endoteliali selezionate, che formano la parete del vaso. Immediatamente dopo questa lesione mirata, i bMΦ si sono precipitati sul posto e hanno rimosso efficacemente i frammenti delle cellule morenti. I macrofagi tessutali tradizionali e i globuli bianchi mobili chiamati neutrofili sono arrivati meno spesso, hanno trascorso meno tempo sul sito del danno e hanno svolto poca pulizia. Queste osservazioni suggeriscono che i bMΦ sono particolarmente posizionati e attrezzati per percepire i problemi dall’interno del vaso e preservare la pulizia e l’integrità dell’interfaccia sangue‑vasi.
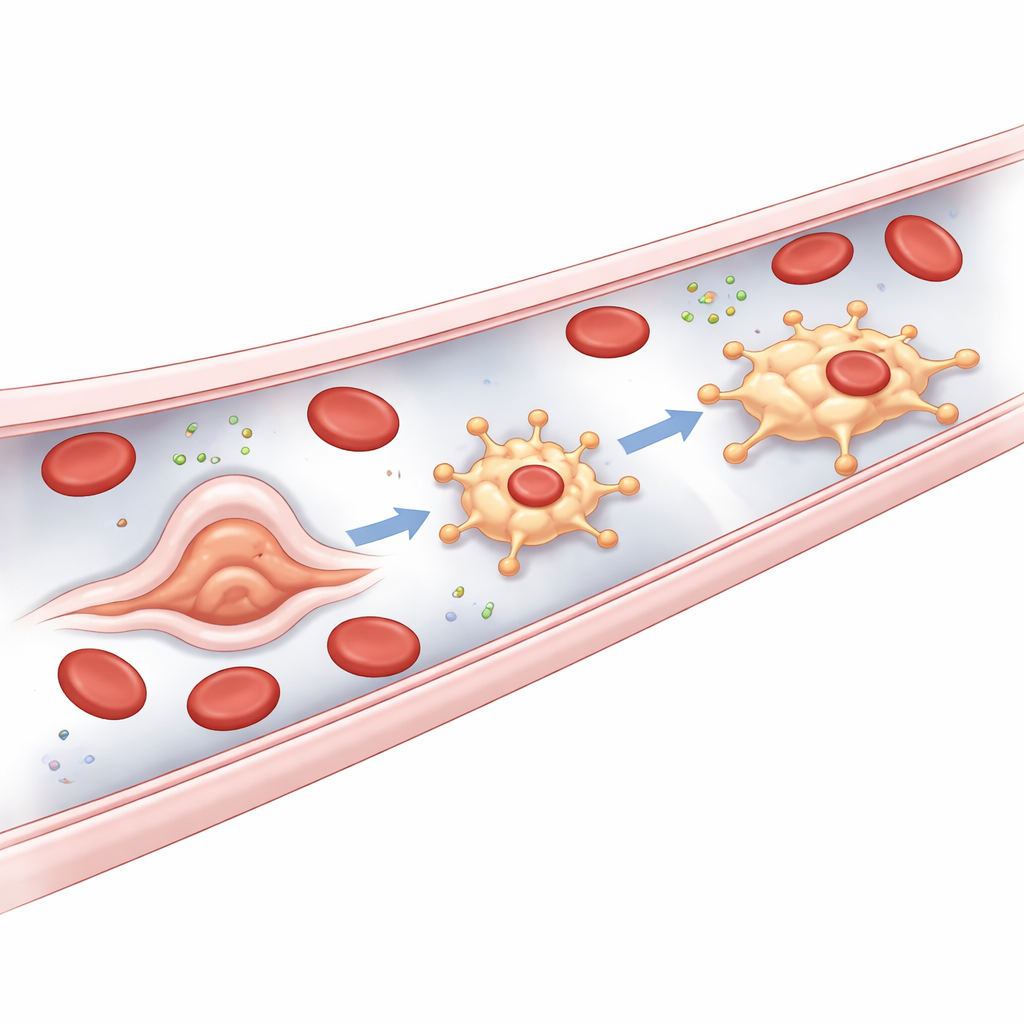
Da dove provengono questi guardiani
Una sorpresa chiave dello studio è l’origine dei bMΦ. La maggior parte dei macrofagi residenti nei tessuti deriva da precursori ematici precoci o da cellule midollari successive. Al contrario, i bMΦ sembrano sbocciare direttamente dal rivestimento vascolare stesso. Negli embrioni di pesce zebra, poco dopo l’inizio del flusso sanguigno, certe cellule endoteliali nei vasi principali del tronco e in particolare nel plesso della vena caudale subiscono un rapido cambiamento di forma, sporgono nel lume vascolare e poi si staccano come bMΦ liberi di muoversi. Gli autori definiscono questo insolito processo transizione endotelio‑verso‑macrofago. Dipende da regolatori ben noti della linea immunitaria mieloide ma, cosa sorprendente, non richiede Runx1, un interruttore maestro normalmente essenziale per trasformare le cellule vascolari in cellule staminali emopoietiche. Questo distingue i bMΦ come una quarta via di sviluppo distinta per i macrofagi nel pesce zebra.
Ruolo conservato tra le specie e prospettive future
Per verificare se cellule simili esistono nei mammiferi, il team ha iniettato particelle fungine nel sangue dei topi ed esaminato quali cellule le hanno ingerite. Hanno trovato un gruppo raro di cellule circolanti che, come i bMΦ del pesce zebra, erano mangiatori efficienti, portavano una miscela di marcatori di superficie immunitari e associati ai vasi e mostravano estensioni simili a tentacoli al microscopio. Queste cellule erano distinte dalle popolazioni note di monociti e neutrofili, suggerendo che guardiani simili ai bMΦ sono conservati evolutivamente. In modo intrigante, si sviluppano e funzionano anche in assenza di un recettore chiave normalmente richiesto per la maggior parte degli altri macrofagi, il che potrebbe spiegare perché sono sfuggiti all’attenzione così a lungo. Nel complesso, i risultati ridisegnano la nostra comprensione di come sangue e vasi sono sorvegliati, suggerendo che un giorno si potrebbe sfruttare o ingegnerizzare queste cellule di pattuglia residenti per trattare infezioni ematiche o malattie che danneggiano il rivestimento vascolare.
Cosa significa per la nostra salute
In termini pratici, questo lavoro mostra che i nostri vasi sanguigni ospitano guardiani di sicurezza integrati. Questi guardiani emergono in modo inatteso dalla parete del vaso, si posano sulla superficie interna e ispezionano continuamente sia il sangue sia il rivestimento alla ricerca di problemi — rimuovendo germi e cellule difettose e ripulendo dopo i danni. Rivelando questo strato di protezione finora trascurato sia nei pesci sia nei topi, lo studio apre la strada a terapie future che potrebbero potenziare o imitare queste cellule per mantenere il sangue più pulito e i vasi più sani in condizioni che vanno dalle infezioni ematiche alle lesioni vascolari e alle malattie cardiovascolari.
Citazione: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Parole chiave: macrofagi, vasi sanguigni, sorveglianza immunitaria, pesce zebra, biologia vascolare