Clear Sky Science · pt
Macrófagos residentes dos vasos sanguíneos protegem a integridade do sangue e dos vasos em zebrafish
Guardas ocultos na nossa corrente sanguínea
A cada segundo, o sangue percorre uma imensa rede de vasos que, colocados ponta a ponta, se estenderiam por quilômetros mesmo em um animal pequeno. Dependemos dessa rodovia oculta para transportar oxigênio, nutrientes e células imunes. Ainda assim, uma pergunta básica permaneceu surpreendentemente obscura: quem verifica constantemente a qualidade do próprio sangue e mantém as delicadas paredes dos vasos seguras? Este estudo, realizado em embriões translúcidos de zebrafish e estendido para camundongos, revela um tipo de célula imune até então não reconhecido que vive dentro dos vasos sanguíneos e atua como um inspetor e agente de limpeza in loco da circulação.
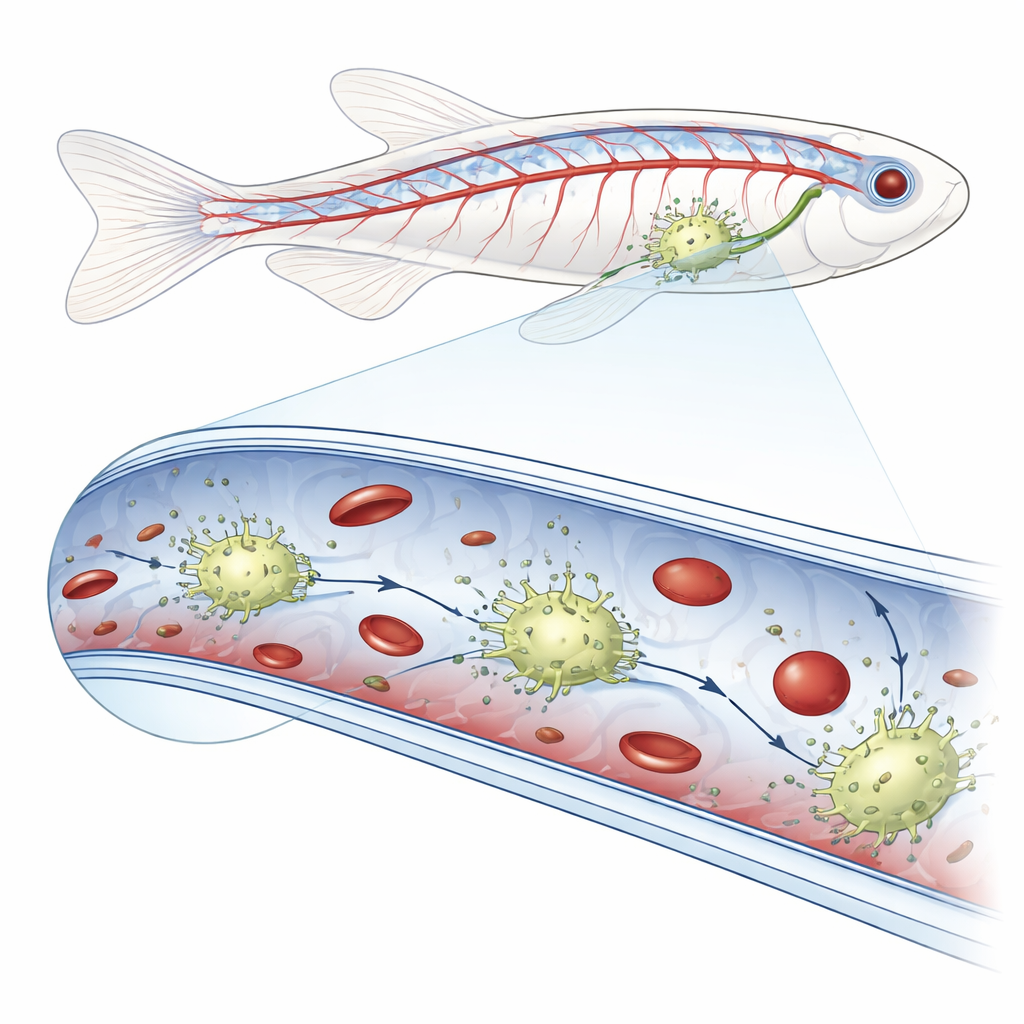
Novas células de patrulha dentro dos vasos sanguíneos
Usando imagem ao vivo de alta resolução em embriões de zebrafish, os pesquisadores notaram células excepcionalmente brilhantes rastejando ao longo das superfícies internas das veias na região da cauda. Quando injetaram bactérias fluorescentes, partículas fúngicas, microesferas sintéticas ou glóbulos vermelhos doadores na corrente sanguínea, essas células intravasculares foram as únicas que engoliram o material estranho. Marcação genética cuidadosa mostrou que essas células exibiam características tanto de células do revestimento vascular quanto de fagócitos clássicos conhecidos como macrófagos. Como residem dentro dos vasos sanguíneos em vez de nos tecidos circundantes, a equipe as batizou de macrófagos residentes dos vasos sanguíneos, ou bMΦs.
Como essas células vigiam e limpam o sangue
Filmes de lapso de tempo em close-up revelaram que os bMΦs rastejam de forma ameboide ao longo do revestimento vascular, às vezes bloqueando brevemente o fluxo—um sinal de forte fixação. Suas superfícies se cobrem de finas e flexíveis protrusões que as ajudam a agarrar a parede e capturar material em passagem. Quando a equipe perturbou o citoesqueleto interno das células com um fármaco, essas protrusões desapareceram, os bMΦs se destacaram da superfície do vaso e não conseguiram mais limpar eficientemente as partículas injetadas, que então derivaram livremente na circulação. As células também interagiam com as próprias células sanguíneas do animal: agarravam glóbulos vermelhos em passagem e células-tronco e progenitoras formadoras de sangue, examinavam-nas na superfície e então ou as liberavam intactas ou fagocitavam aquelas que pareciam incomumente grandes ou anormais, ajudando a manter a qualidade do sangue.
Primeiros a responder a lesões vasculares
Além da limpeza cotidiana, os bMΦs também atuam como respondedores rápidos quando os vasos são danificados. Os pesquisadores usaram uma ferramenta optogenética—essencialmente um interruptor molecular ativado por luz—para desencadear a morte de algumas células endoteliais selecionadas, que formam a parede do vaso. Imediatamente após essa lesão direcionada, os bMΦs correram para o local e removeram eficientemente os fragmentos das células moribundas. Macrófagos teciduais tradicionais e células brancas de ação rápida chamadas neutrófilos chegaram com menos frequência, passaram menos tempo no local do dano e realizaram pouca limpeza. Essas observações sugerem que os bMΦs estão especialmente posicionados e equipados para detectar problemas de dentro do vaso e preservar a limpeza e a integridade da interface sangue–vaso.
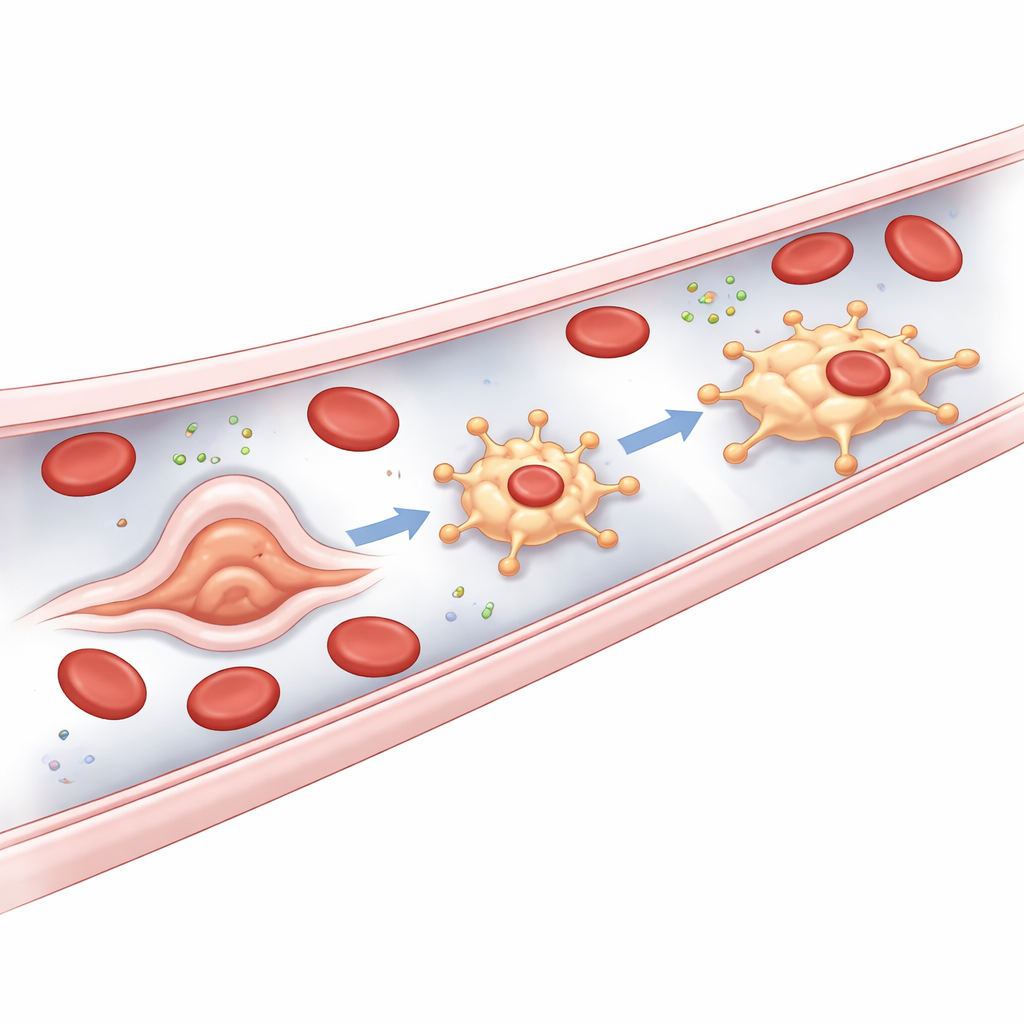
De onde vêm esses guardiões
Uma surpresa central do estudo é a origem dos bMΦs. A maioria dos macrófagos residentes em tecidos surge de precursores sanguíneos precoces ou de células posteriores da medula óssea. Em contraste, os bMΦs parecem brotar diretamente do próprio revestimento vascular. Em embriões de zebrafish, logo após o início do fluxo sanguíneo, certas células endoteliais nos vasos principais do tronco e especialmente no plexo da veia caudal sofrem uma rápida mudança de forma, protuberando para dentro do vaso e depois destacando-se como bMΦs móveis. Os autores chamam esse processo incomum de transição endotélio‑para‑macrófago. Ele depende de reguladores bem conhecidos da linhagem imune mieloide, mas, de forma notável, não requer Runx1, um interruptor mestre normalmente essencial para transformar células vasculares em células-tronco formadoras de sangue. Isso sinaliza os bMΦs como uma quarta via de desenvolvimento distinta para macrófagos em zebrafish.
Papel conservado entre espécies e promessas futuras
Para verificar se células semelhantes existem em mamíferos, a equipe injetou partículas fúngicas no sangue de camundongos e examinou quais células as engoliam. Eles encontraram um grupo raro de células circulantes que, como os bMΦs de zebrafish, eram fagocitárias eficientes, carregavam uma mistura de marcadores superficiais imunes e associados aos vasos e exibiam extensões em forma de tentáculos ao microscópio. Essas células eram distintas das populações conhecidas de monócitos e neutrófilos, sugerindo que guardiões do tipo bMΦ são conservados evolutivamente. Intrigantemente, elas também se desenvolvem e funcionam mesmo quando um receptor-chave normalmente exigido para a maioria dos outros macrófagos está ausente, o que pode explicar por que passaram tanto tempo despercebidas. Em conjunto, os achados redesenham nossa visão de como sangue e vasos são vigiados, insinuando que um dia se poderá aproveitar ou engenheirar essas células de patrulha residentes para tratar infecções que viajam pela corrente sanguínea ou doenças que danificam o revestimento vascular.
O que isso significa para nossa saúde
Em termos práticos, este trabalho mostra que nossos vasos sanguíneos abrigam seus próprios guardas de segurança embutidos. Esses guardas surgem de maneira inesperada a partir da parede do vaso, acomodam‑se na superfície interna e inspecionam continuamente tanto o sangue quanto o revestimento em busca de problemas—removendo germes e células defeituosas e limpando após danos. Ao revelar essa camada de proteção negligenciada em peixes e camundongos, o estudo abre caminho para terapias futuras que possam reforçar ou imitar essas células para manter o sangue mais limpo e os vasos mais saudáveis em condições que vão desde infecções sanguíneas até lesões vasculares e doenças cardiovasculares.
Citação: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Palavras-chave: macrófagos, vasos sanguíneos, vigilância imune, zebrafish, biologia vascular