Clear Sky Science · nl
Bloedvat‑residentie macrofagen beschermen bloed- en vaatintegriteit bij zebravis
Verborgen Wachters in Ons Bloed
Elke seconde stroomt bloed door een enorm netwerk van vaten dat, als men ze achter elkaar zou leggen, zelfs bij een klein dier kilometers lang zou zijn. We vertrouwen op deze verborgen snelweg om zuurstof, voedingsstoffen en immuuncellen te vervoeren. Toch bleef één fundamentele vraag verrassend onduidelijk: wie controleert voortdurend de kwaliteit van het bloed zelf en beschermt de kwetsbare vaatwanden? Deze studie, uitgevoerd in transparante zebravis‑embryo’s en uitgebreid naar muizen, onthult een voorheen onopgemerkte soort immuuncel die binnenin bloedvaten leeft en dienstdoet als on‑site inspecteur en reiniger van de circulatie.
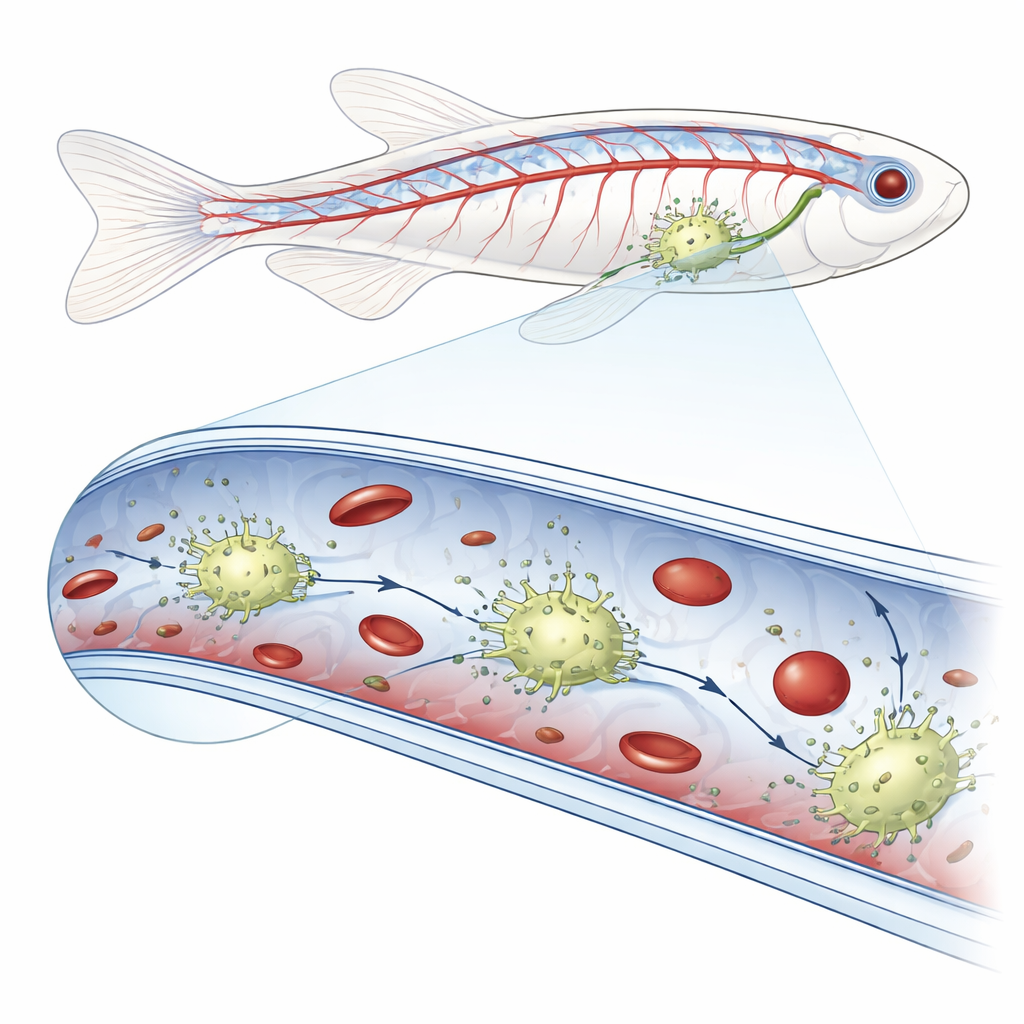
Nieuwe Patrouillecellen Binnen Bloedvaten
Met hoogresolutie live‑imaging in zebravis‑embryo’s zagen de onderzoekers uitzonderlijk heldere cellen kruipen langs de binnenoppervlakken van aders in het staartgebied. Toen ze fluorescerende bacteriën, schimmelpartikels, synthetische bolletjes of donorrede bloedcellen in de bloedbaan injecteerden, waren deze intravasculaire cellen de enigen die vreemd materiaal opslokten. Zorgvuldig genetisch labelen toonde aan dat deze cellen kenmerken van zowel endotheelcellen (vaatwandcellen) als klassieke immuuneters, de macrofagen, droegen. Omdat ze in bloedvaten wonen in plaats van in omliggende weefsels, noemde het team ze bloedvat‑residentie macrofagen, of bMΦs.
Hoe Deze Cellen Het Bloed Bewaken en Reinigen
Close‑up time‑lapse‑opnames lieten zien dat bMΦs amoebe‑achtig langs het vaatendotheel kruipen en soms kort de stroming blokkeren, een teken van sterke hechting. Hun oppervlak zit vol dunne, flexibele uitsteeksels die helpen zich aan de wand vast te klampen en passerend materiaal te vangen. Wanneer het team het interne cytoskelet van de cellen verstoorde met een geneesmiddel, verdwenen deze uitsteeksels, lieten bMΦs los van het vatoppervlak en konden ze geïnjecteerde deeltjes niet langer efficiënt verwijderen, waardoor die vrij in de circulatie dreven. De cellen beïnvloedden ook de eigen bloedcellen van het dier: ze pakten passerende rode bloedcellen en bloedvormende stam‑ en voorlopercellen, onderzochten ze aan het oppervlak en lieten ze vervolgens ongedeerd vrij of omhulden die cellen die ongewoon groot waren of afwijkingen vertoonden, waardoor de bloedkwaliteit behouden bleef.
Eerste Hulp bij Vaatschade
Buiten dagelijkse reiniging fungeren bMΦs ook als snelle eerstehulpverleners bij vaatbeschadiging. De onderzoekers gebruikten een optogenetisch hulpmiddel—een min of meer lichtgestuurde moleculaire schakelaar—om de dood van enkele geselecteerde endotheelcellen te veroorzaken, de cellen die de vaatwand vormen. Direct na deze gerichte schade snelden bMΦs naar de plek en ruimden efficiënt de dode celresten op. Traditionele weefselmacrofagen en snelbewegende witte bloedcellen, neutrofielen genoemd, arriveerden minder vaak, verbleven korter op de schadeplaats en voerden weinig opruimwerk uit. Deze observaties suggereren dat bMΦs speciaal gepositioneerd en uitgerust zijn om problemen van binnenuit het vat te detecteren en de netheid en integriteit van de bloed‑vaatinterface te bewaren.
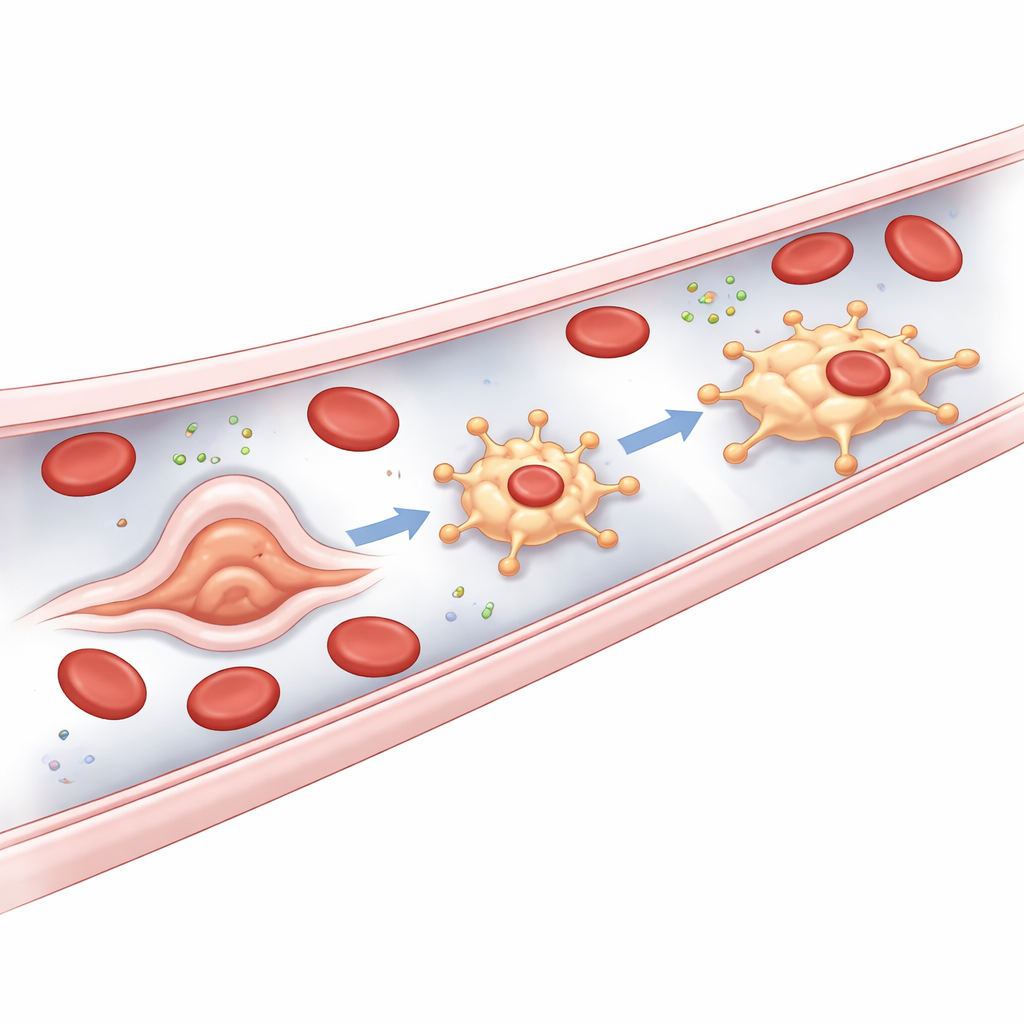
Waar Deze Wachters Vandaan Komen
Een belangrijke verrassing van de studie is de herkomst van bMΦs. De meeste weefselresidentie macrofagen ontstaan uit vroege bloedvoorlopers of later uit beenmergcellen. Daarentegen lijken bMΦs rechtstreeks uit het vaatendotheel te ontspringen. In zebravis‑embryo’s ondergaan bepaalde endotheelcellen in de hoofdtrunkvaten en vooral in het plexus van de staartader kort na het begin van de bloedstroom een snelle vormverandering: ze zwellen uit in het vat en laten zich vervolgens los als vrijbewegende bMΦs. De auteurs noemen dit ongebruikelijke proces een endotheel‑naar‑macrofagetransitie. Het hangt af van bekende regelaars van de myeloïde immuunlijn maar vereist opvallend genoeg geen Runx1, een meesterregulator die normaal essentieel is om vaatcellen om te zetten in bloedvormende stamcellen. Dit plaatst bMΦs als een aparte, vierde ontwikkelingsroute voor macrofagen in zebravissen.
Behouden Rol Over Soorten en Toekomstige Belofte
Om te onderzoeken of vergelijkbare cellen in zoogdieren bestaan, injecteerde het team schimmelpartikels in het bloed van muizen en keek welke cellen ze opnamen. Ze vonden een zeldzame groep circulerende cellen die, net als zebravis‑bMΦs, efficiënte eters waren, een mengeling van immuun‑ en vaatgebonden oppervlakte‑markers droegen en onder de microscoop tentakelachtige uitlopers toonden. Deze cellen verschilden van bekende monocyten‑ en neutrofielpopulaties, wat suggereert dat bMΦ‑achtige wachters evolutionair bewaard zijn. Intrigerend genoeg ontwikkelen en functioneren ze zelfs wanneer een belangrijke receptor die normaal voor de meeste andere macrofagen vereist is, ontbreekt, wat kan verklaren waarom ze zo lang onopgemerkt bleven. Samen herschrijven de bevindingen ons beeld van hoe bloed en vaten worden bewaakt en suggereren ze dat men deze residentie‑patrouillecellen ooit zou kunnen inzetten of ontwerpen om bloedbaaninfecties of aandoeningen die vaatwanden beschadigen te behandelen.
Wat Dit Betekent voor Onze Gezondheid
Concreet toont dit werk aan dat onze bloedvaten hun eigen ingebouwde beveiligers herbergen. Deze wachters ontstaan op onverwachte wijze uit de vaatwand, nestelen zich aan de binnenzijde en inspecteren continu zowel het bloed als het endotheel op problemen—verwijderen ziekteverwekkers en defecte cellen en ruimen schade op. Door deze over het hoofd geziene beschermingslaag aan het licht te brengen in zowel vissen als muizen, opent de studie de deur naar toekomstige therapieën die deze cellen kunnen versterken of nabootsen om het bloed schoner en vaten gezonder te houden bij aandoeningen variërend van bloedbaaninfecties tot vaatschade en hart‑ en vaatziekten.
Bronvermelding: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Trefwoorden: macrofagen, bloedvaten, immuunbewaking, zebravis, vasculaire biologie