Clear Sky Science · es
Macrófagos residentes en vasos sanguíneos protegen la integridad de la sangre y de los vasos en pez cebra
Guardianes ocultos en nuestro torrente sanguíneo
Cada segundo, la sangre circula por una inmensa red de vasos que, puestos uno tras otro, se extenderían kilómetros incluso en un animal pequeño. Confiamos en esta autopista oculta para transportar oxígeno, nutrientes y células inmunitarias. Sin embargo, una pregunta básica ha permanecido sorprendentemente poco clara: ¿quién verifica constantemente la calidad de la propia sangre y protege las delicadas paredes vasculares? Este estudio, realizado en embriones transparentes de pez cebra y ampliado a ratones, descubre un tipo de célula inmunitaria hasta ahora no reconocida que vive dentro de los vasos sanguíneos y actúa como un inspector y limpiador inmediato de la circulación.
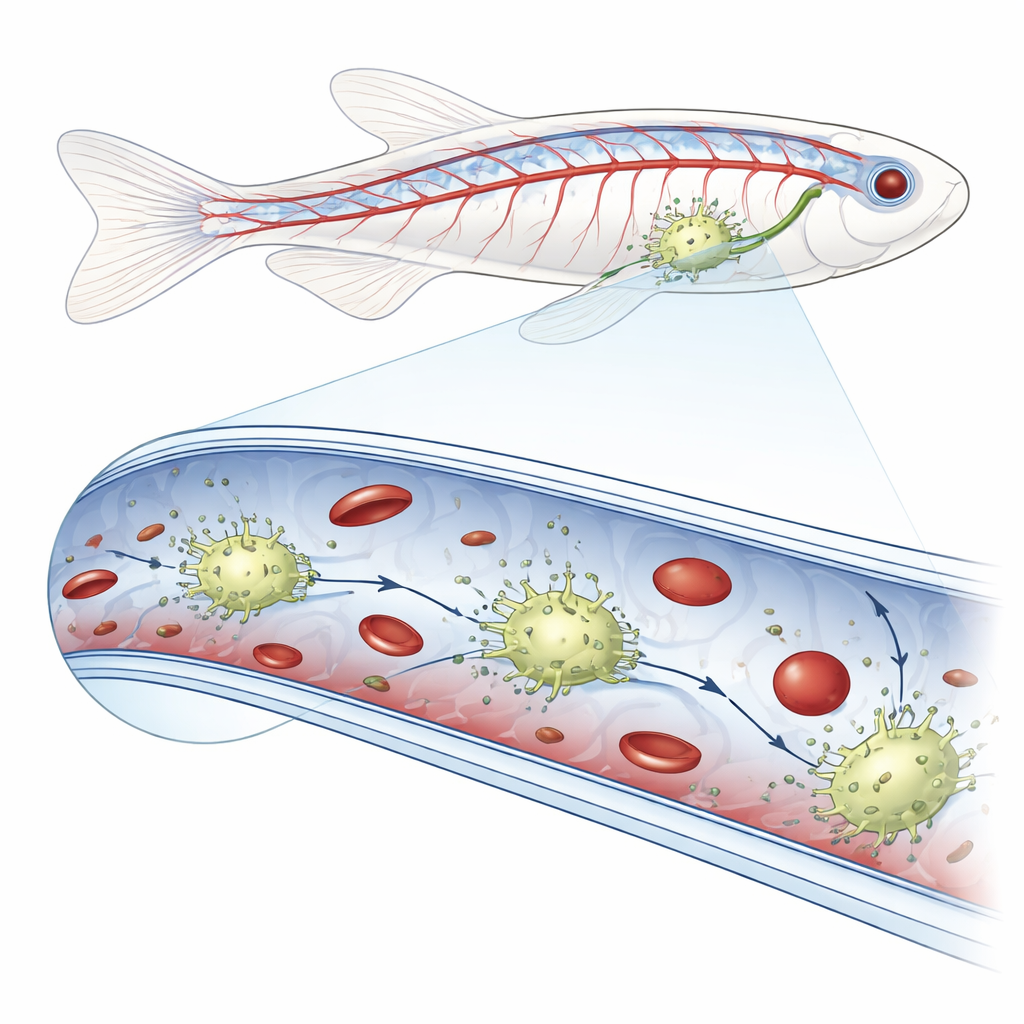
Nuevas células de patrulla dentro de los vasos sanguíneos
Usando imágenes en vivo de alta resolución en embriones de pez cebra, los investigadores observaron células inusualmente brillantes que se desplazaban por las superficies internas de las venas en la región de la cola. Cuando inyectaron bacterias fluorescentes, partículas fúngicas, cuentas sintéticas o hematíes donantes en el torrente sanguíneo, estas células intravasculares fueron las únicas que ingerían el material extraño. Un marcado genético cuidadoso mostró que estas células tenían rasgos tanto de las células que recubren los vasos como de los comedores inmunitarios clásicos conocidos como macrófagos. Debido a que residen dentro de los vasos en lugar de en los tejidos circundantes, el equipo las denominó macrófagos residentes de vasos sanguíneos, o bMΦs.
Cómo estas células vigilan y limpian la sangre
Películas de lapso temporal en primer plano revelaron que los bMΦs se desplazan de forma ameboide a lo largo del revestimiento vascular, a veces bloqueando brevemente el flujo, una señal de fuerte adherencia. Sus superficies están cubiertas de finas y flexibles protrusiones que les ayudan a sujetarse a la pared y atrapar el material que pasa. Cuando el equipo perturbó el armazón interno de estas células con un fármaco, esas protrusiones desaparecieron, los bMΦs se desprendieron de la superficie del vaso y ya no pudieron eliminar eficientemente las partículas inyectadas, que entonces derivaron libremente en la circulación. Las células también interactuaron con las propias células sanguíneas del animal: agarraron hematíes en movimiento y células madre y progenitoras formadoras de sangre, las examinaron en la superficie y luego o bien las liberaron sin daño o bien fagocitaron aquellas que parecían inusualmente grandes o anormales, ayudando así a mantener la calidad de la sangre.
Primeros respondedores ante lesiones vasculares
Más allá de la limpieza cotidiana, los bMΦs también actúan como respondedores rápidos cuando los vasos resultan dañados. Los investigadores emplearon una herramienta optogenética—esencialmente un interruptor molecular activado por luz—para provocar la muerte de algunas células endoteliales seleccionadas, que forman la pared vascular. Inmediatamente después de esta lesión dirigida, los bMΦs acudieron al lugar y eliminaron con eficacia los fragmentos de células moribundas. Los macrófagos tisulares tradicionales y los glóbulos blancos de movimiento rápido llamados neutrófilos llegaron con menos frecuencia, permanecieron menos tiempo en la zona dañada y realizaron poca limpieza. Estas observaciones sugieren que los bMΦs están especialmente situados y equipados para detectar problemas desde el interior del vaso y preservar la limpieza e integridad de la interfaz sangre–vaso.
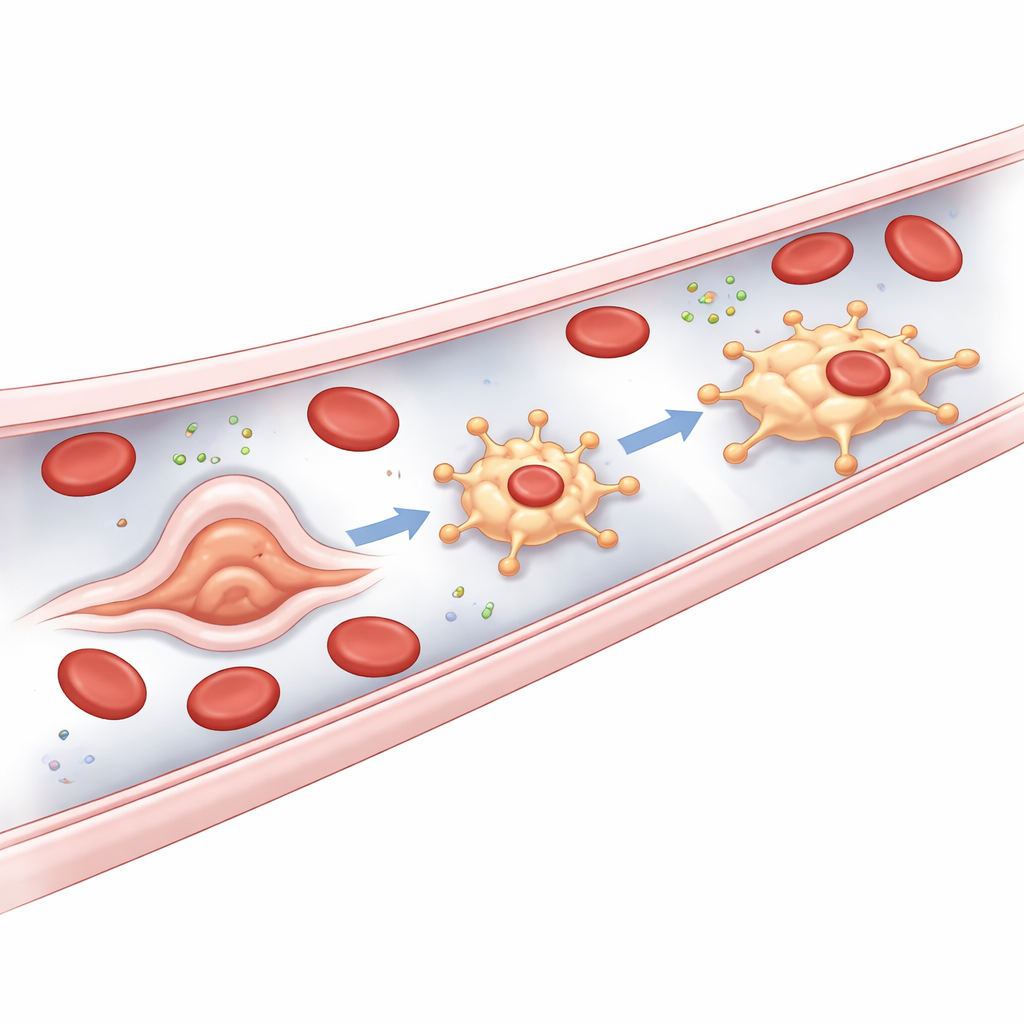
De dónde proceden estos guardianes
Una sorpresa clave del estudio es el origen de los bMΦs. La mayoría de los macrófagos residentes en tejidos provienen de precursores sanguíneos tempranos o de células de la médula ósea en etapas posteriores. En contraste, los bMΦs parecen brotar directamente del propio revestimiento vascular. En embriones de pez cebra, poco después de que comience el flujo sanguíneo, ciertas células endoteliales en los vasos del tronco principal y especialmente en el plexo de la vena caudal sufren un cambio rápido de forma, abultándose hacia el interior del vaso y luego desprendiéndose como bMΦs móviles. Los autores denominan a este inusual proceso una transición endotelio‑a‑macrófago. Depende de reguladores bien conocidos de la línea inmune mieloide pero, de forma destacada, no requiere Runx1, un interruptor maestro normalmente esencial para convertir las células vasculares en células madre formadoras de sangre. Esto sitúa a los bMΦs como una ruta de desarrollo distinta, la cuarta, para macrófagos en pez cebra.
Función conservada entre especies y promesa futura
Para comprobar si existen células similares en mamíferos, el equipo inyectó partículas fúngicas en la sangre de ratones y examinó qué células las engullían. Encontraron un grupo raro de células circulantes que, al igual que los bMΦs de pez cebra, eran comedores eficientes, portaban una mezcla de marcadores de superficie inmunitarios y asociados a vasos, y mostraban extensiones semejantes a tentáculos bajo el microscopio. Estas células eran distintas de las poblaciones conocidas de monocitos y neutrófilos, lo que sugiere que guardianes similares a los bMΦs están conservados evolutivamente. De forma intrigante, también se desarrollan y funcionan incluso cuando falta un receptor clave normalmente requerido para la mayoría de los otros macrófagos, lo que puede explicar por qué pasaron desapercibidos durante tanto tiempo. En conjunto, los hallazgos reconfiguran nuestra imagen de cómo se vigilan la sangre y los vasos, e indican que algún día podría aprovecharse o diseñarse estas células patrulleras residentes para tratar infecciones que viajan por la sangre o enfermedades que dañan el revestimiento vascular.
Qué significa esto para nuestra salud
En términos cotidianos, este trabajo muestra que nuestros vasos sanguíneos alojan sus propios guardianes de seguridad integrados. Estos guardianes surgen de una manera inesperada desde la pared vascular, se asientan en la superficie interna y inspeccionan continuamente tanto la sangre como el revestimiento en busca de problemas: eliminan gérmenes y células defectuosas y limpian los restos tras lesiones. Al revelar esta capa de protección pasada por alto tanto en peces como en ratones, el estudio abre la puerta a futuras terapias que podrían potenciar o imitar estas células para mantener la sangre más limpia y los vasos más saludables en condiciones que van desde infecciones en el torrente sanguíneo hasta lesiones vasculares y enfermedades cardiovasculares.
Cita: Weijts, B., Demmers, J.A.A. & Robin, C. Blood vessel-resident macrophages safeguard blood and vessel integrity in zebrafish. Nat Immunol 27, 975–984 (2026). https://doi.org/10.1038/s41590-026-02481-y
Palabras clave: macrófagos, vasos sanguíneos, vigilancia inmunitaria, pez cebra, biología vascular