Clear Sky Science · zh
基于tRNA脱酰化酶的生物合成通路发现
活细胞中的隐秘化学
当今许多药物——从止痛药到抗生素和抗癌药——最初都来源于微生物或植物为自身用途合成的小分子。然而,即便经过数十年的搜寻,科学家们仍怀疑大部分自然界的化学产物尚未被发现。本研究揭示了一种新方法,用以在微生物DNA中定位构建非常规氨基酸和短肽的难以察觉的通路——这些分子可能成为未来的药物或研究工具。
为何特殊构件重要
氨基酸最为人所知的是作为蛋白质的构件,但细胞也会将它们改造成种类繁多的其他分子。其中一些是含有稀有元素(如氟或砷)或具有非常规氮—氮等键的非常规氨基酸;另一些被缝合进复杂的抗生素、神经调节分子(如裸盖菇素)或胰岛素等肽类激素。由于这些结构高度多样,负责合成它们的基因往往不符合当前基因组搜索工具识别的典型酶家族模式。因此,在如今被测序的大量微生物DNA中,许多相关通路仍然隐匿无形。
质量控制酶作为指示牌
这项新工作的重要洞见在于,某些细胞“校对”酶可以作为指示附近合成非常规氨基酸的通路的灯塔。当细胞生成非常规氨基酸时,这些分子有可能被错误地插入到蛋白质中,从而损害其功能。为避免这种情况,部分微生物携带独立的tRNA脱酰化酶——能够从转运RNA(将构件输送到蛋白合成机器的适配子)上移除错误接上的氨基酸的酶。作者此前已证明,一种此类脱酰化酶能保护细菌免受氟代苏氨酸的误用。这里他们将这一思路扩展:如果一个脱酰化酶基因位于一簇其他代谢基因旁边,它可能是用来防御局部合成的、潜在有害的氨基酸。由此,脱酰化酶成为识别原本隐秘的生物合成基因簇的有用标记。
以新视角挖掘基因组
研究团队聚焦于一类称为AlaX的脱酰化酶,筛查了2.3万多个相关序列。他们构建了一个可视化工具tR3D,用以描绘每个脱酰化酶基因在基因组中周围邻居的分布。大多数AlaX酶与参与常规氨基酸和蛋白质代谢的家务性基因相邻。但约11%出现在更为特殊的环境,靠近运输蛋白、调控因子和典型于次级代谢的异常酶类——次级代谢是微生物用于防御或信号传递的专门化化学反应。这份有前景的基因簇短名单中,仅有一小部分属于已知的天然产物类别,表明许多其余基因簇可能代表此前被忽视的化学新领域。
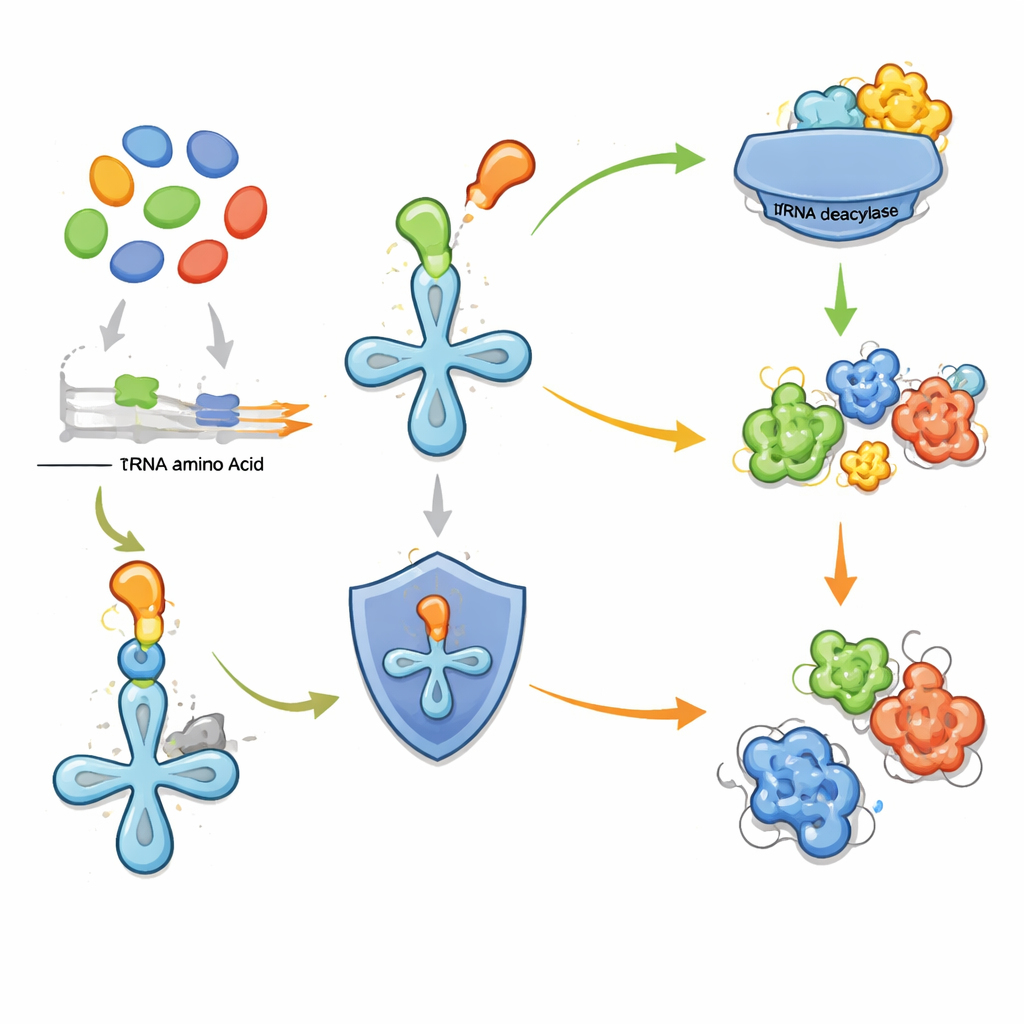
从标记的基因簇中发现新分子
为验证这一策略,研究者对两个由邻近脱酰化酶标记的、性质迥异的基因簇进行了实验鉴定。第一个是一个在一百多种物种中发现的紧凑四基因单元,编码一种将甲硫氨酸(常见氨基酸)羟基化的简单双功能酶,产生一种非常规变体。配套的脱酰化酶选择性地从转运RNA上移除这种修饰的甲硫氨酸,保护细胞免于将其误认为正常构件。第二个来自土壤微生物的基因簇则更为复杂。它将生成活性氮–氮单元的酶与能将三个由氨基酸衍生片段连接起来的酶相结合。通过在实验室细菌中重建该通路并追踪标记的起始底物,团队发现了一种新的肼酰胺键连接的三肽,命名为fuscazine。其主链由精氨酸、丙氨酸和一个环状赖氨酸衍生物构成,以一种此前仅在更复杂体系中见过的不寻常方式连接。
为未来发现开启大门
这些案例研究显示,tRNA脱酰化酶不仅仅是简单的质量控制工具——它们还能指示进化如何将氨基酸化学推向新领域的基因组邻域。通过追随这些指示牌,作者鉴定了数千个候选基因簇,其中许多超出了当前基因组挖掘所用标准类别。他们的tR3D平台也可应用于其他酶家族,帮助研究者聚焦那些可能编码非常规成键反应的基因。对非专业读者而言,结论是:活细胞藏有浩瀚的化学解决方案库,而以脱酰化酶等内建安全阀为导向的聪明基因组解读方法正开始揭示这片库藏。每一个新绘制的通路不仅扩展了我们对生命如何构建分子的基础理解,也为设计药物和生物催化剂提供了新的出发点。
引用: Millar, D.C., Zhou, Y., Marchand, J.A. et al. tRNA-deacylase-directed discovery of biosynthetic pathways. Nat. Chem. 18, 863–871 (2026). https://doi.org/10.1038/s41557-026-02126-5
关键词: 天然产物, 非常规氨基酸, 基因组挖掘, tRNA质量控制, 生物合成基因簇