Clear Sky Science · pt
descoberta de vias biossintéticas guiada por tRNA-deacilase
Química oculta dentro das células vivas
Muitos dos medicamentos atuais, de analgésicos a antibióticos e fármacos contra o câncer, tiveram origem como pequenas moléculas produzidas por microrganismos ou plantas para seus próprios propósitos. Ainda assim, mesmo após décadas de buscas, os cientistas suspeitam que a maior parte dos truques químicos da natureza permanece por descobrir. Este estudo revela uma nova forma de identificar vias difíceis de encontrar no DNA microbiano que constroem aminoácidos incomuns e peptídeos curtos — moléculas que podem se tornar os fármacos ou ferramentas de pesquisa de amanhã.
Por que blocos de construção especiais importam
Os aminoácidos são mais conhecidos como blocos de construção das proteínas, mas as células também os transformam em uma enorme variedade de outras moléculas. Algumas são aminoácidos não padronizados que contêm elementos raros como flúor ou arsênico, ou ligações incomuns entre átomos de nitrogênio. Outras são incorporadas em antibióticos complexos, neuromoduladores como a psilocibina, ou hormônios peptídicos como a insulina. Como essas estruturas são tão diversas, os genes que as produzem frequentemente não se assemelham às famílias clássicas de enzimas que as ferramentas atuais de busca genômica procuram. Como resultado, muitas das vias subjacentes continuam invisíveis nas enormes quantidades de DNA microbiano que vêm sendo sequenciadas.
Enzimas de controle de qualidade como pontos de referência
A ideia central do novo trabalho é que certas enzimas celulares de “revisão” podem agir como faróis para vias vizinhas que produzem aminoácidos estranhos. Quando uma célula produz um aminoácido não padronizado, existe o risco de que ele seja inserido por engano em proteínas, prejudicando sua função. Para evitar isso, alguns micróbios carregam deacilases de tRNA autônomas — enzimas que removem aminoácidos incorretamente ligados ao RNA de transferência, os adaptadores que fornecem os blocos de construção para a maquinaria de produção de proteínas. Os autores já haviam mostrado anteriormente que uma dessas deacilases protege bactérias contra o uso indevido de treonina fluorada. Aqui eles estendem essa ideia: se um gene de deacilase está ao lado de um cluster de outros genes metabólicos, pode estar ali para proteger contra um aminoácido produzido localmente e potencialmente nocivo. Isso torna a deacilase um marcador útil para um cluster gênico biossintético que, de outra forma, seria críptico.
Minerando genomas com uma nova lente
Focando em uma família de deacilases chamada AlaX, a equipe examinou mais de 23.000 sequências relacionadas. Eles construíram uma ferramenta de visualização, tR3D, que mapeia como cada gene de deacilase está rodeado por seus vizinhos no genoma. A maioria das enzimas AlaX apareceu ao lado de genes de manutenção envolvidos no metabolismo rotineiro de aminoácidos e proteínas. Mas cerca de 11% estavam em companhias mais exóticas, próximas a transportadores, reguladores e enzimas incomuns típicas do metabolismo secundário — a química especializada que micróbios usam para defesa ou sinalização. Essa lista curta de clusters promissores incluía apenas uma fração modesta pertencente a classes bem conhecidas de produtos naturais, sugerindo que muitos outros representam química previamente negligenciada.
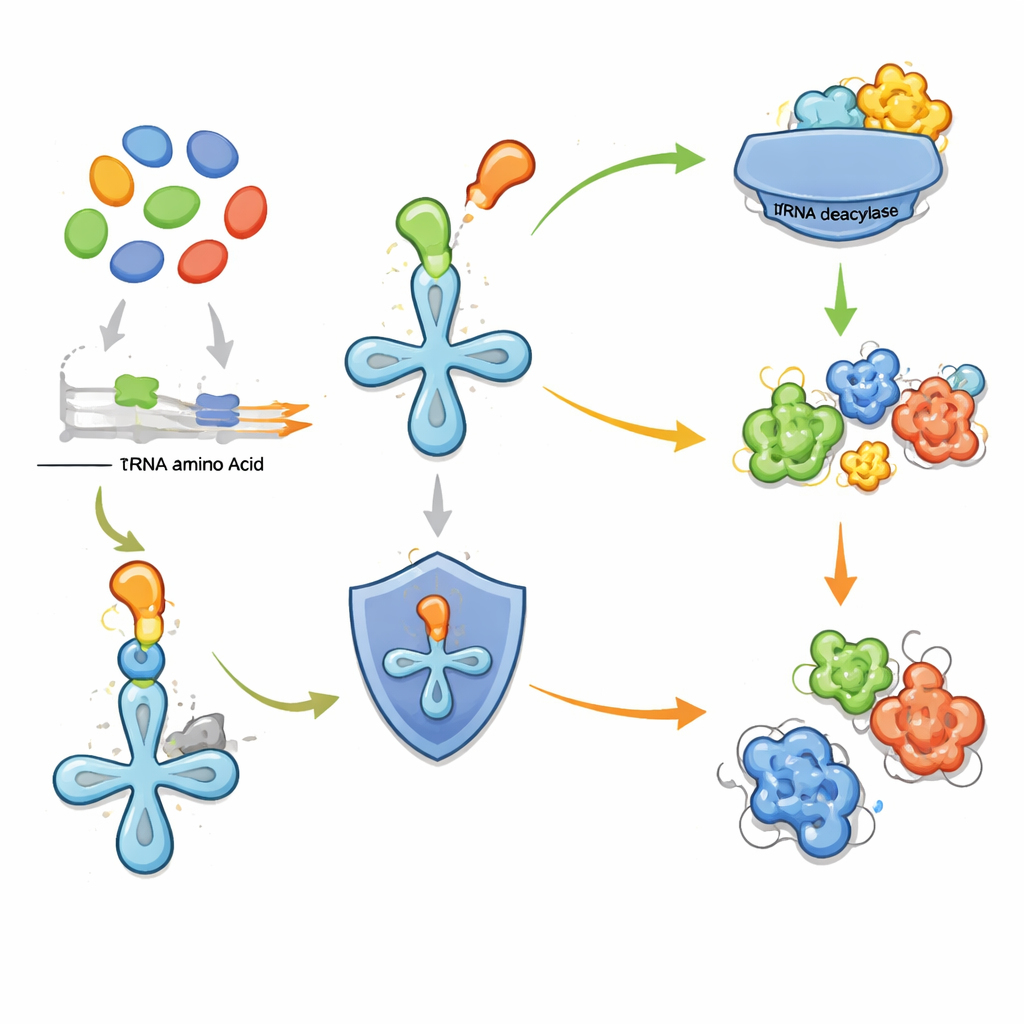
Novas moléculas a partir de clusters marcados
Para testar a estratégia, os pesquisadores sondaram experimentalmente dois clusters gênicos muito diferentes sinalizados por deacilases próximas. O primeiro, uma unidade compacta de quatro genes encontrada em mais de cem espécies, codifica uma enzima simples que adiciona um grupo hidroxila à metionina, um aminoácido comum, criando uma variante não padronizada. A deacilase parceira remove seletivamente essa metionina modificada do RNA de transferência, protegendo a célula de interpretá‑la como o bloco de construção normal. O segundo cluster, de um microrganismo do solo, é mais elaborado. Ele combina enzimas que geram uma unidade reativa nitrogênio–nitrogênio com outras que unem três fragmentos derivados de aminoácidos. Ao reconstituir a via em bactérias de laboratório e rastrear materiais de partida marcados, a equipe descobriu um novo tripeptídeo ligado por hidrazida que chamaram de fuscazina. Sua espinha dorsal é construída a partir de arginina, alanina e um derivado cíclico da lisina, conectados de uma maneira incomum que antes havia sido observada apenas em sistemas mais complexos.
Abrindo portas para descobertas futuras
Esses estudos de caso mostram que deacilases de tRNA são mais do que simples ferramentas de controle de qualidade — elas também destacam bairros de DNA onde a evolução empurrou a química dos aminoácidos para novos territórios. Seguindo esses pontos de referência, os autores identificaram milhares de clusters candidatos, muitos dos quais ficam fora das categorias padrão usadas na mineração genômica atual. A plataforma tR3D pode ser aplicada a outras famílias de enzimas também, ajudando pesquisadores a focalizar genes que provavelmente codificam reações incomuns de formação de ligações. Para não especialistas, a conclusão é que as células vivas escondem uma vasta biblioteca de soluções químicas, e maneiras inteligentes de ler genomas — guiadas por válvulas de segurança embutidas como as deacilases — estão começando a revelá‑la. Cada via recém-mapeada não só expande a compreensão básica de como a vida constrói moléculas, mas também oferece novos pontos de partida para projetar fármacos e biocatalisadores.
Citação: Millar, D.C., Zhou, Y., Marchand, J.A. et al. tRNA-deacylase-directed discovery of biosynthetic pathways. Nat. Chem. 18, 863–871 (2026). https://doi.org/10.1038/s41557-026-02126-5
Palavras-chave: produtos naturais, aminoácidos não canônicos, mineração genômica, controle de qualidade do tRNA, clusters gênicos biossintéticos