Clear Sky Science · pl
Odkrywanie szlaków biosyntezy z wykorzystaniem tRNA-deacylaz
Ukryta chemia wewnątrz żywych komórek
Wiele współczesnych leków — od środków przeciwbólowych po antybiotyki i leki przeciwnowotworowe — zaczynało jako małe cząsteczki wytwarzane przez mikroby lub rośliny dla ich własnych potrzeb. Mimo dekad poszukiwań naukowcy podejrzewają, że większość naturalnych rozwiązań chemicznych pozostaje nieodkryta. Badanie to odsłania nową metodę wyławiania trudnych do wykrycia szlaków w DNA mikroorganizmów, które syntetyzują nietypowe aminokwasy i krótkie peptydy — cząsteczki, które mogą stać się lekami przyszłości lub narzędziami badawczymi.
Dlaczego specjalne „cegiełki” są ważne
Aminokwasy są najbardziej znane jako budulce białek, ale komórki także przekształcają je w ogromną różnorodność innych związków. Niektóre to niestandardowe aminokwasy zawierające rzadkie pierwiastki, jak fluor czy arsen, albo nietypowe wiązania między atomami azotu. Inne włączane są do złożonych antybiotyków, neuromodulatorów takich jak psylocybina czy peptydowych hormonów, np. insuliny. Ponieważ te struktury są tak zróżnicowane, geny je tworzące często nie przypominają klasycznych rodzin enzymatycznych, których poszukują obecne narzędzia do analizy genomów. W rezultacie wiele takich szlaków pozostaje niewidocznych w ogromnych zbiorach DNA mikroorganizmów poddawanych sekwencjonowaniu.
Enzymy kontroli jakości jako drogowskazy
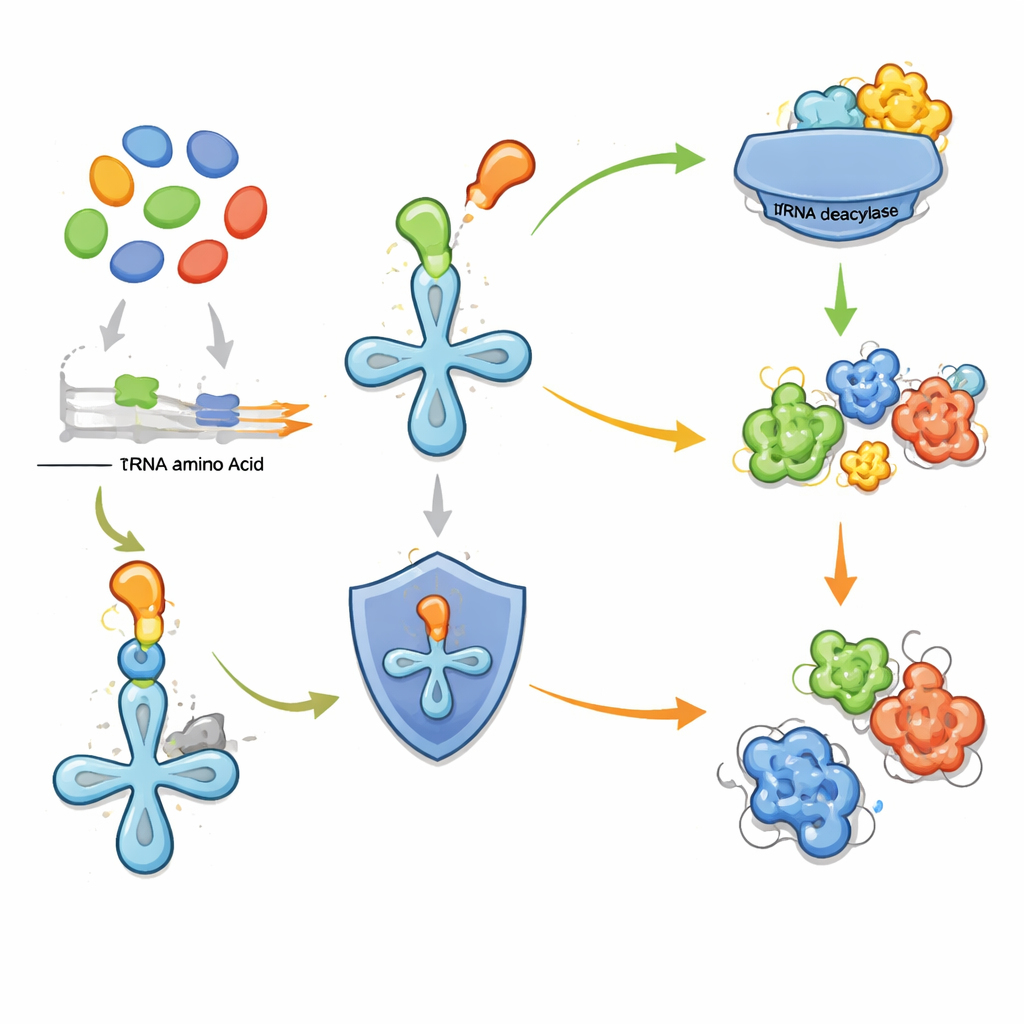
Kluczową obserwacją nowej pracy jest to, że pewne komórkowe enzymy „korygujące błędy” mogą służyć jako latarnie informujące o pobliskich szlakach produkujących dziwne aminokwasy. Gdy komórka wytwarza niestandardowy aminokwas, istnieje ryzyko, że zostanie on omyłkowo wbudowany w białka, co zaburza ich funkcję. Aby temu zapobiec, niektóre mikroby posiadają samodzielne tRNA-deacylazy — enzymy usuwające błędnie przyłączone aminokwasy z tRNA, adaptorów dostarczających składniki do maszynerii syntezy białek. Autorzy wcześniej pokazali, że jedna z takich deacylaz chroni bakterie przed niewłaściwym użyciem sfluorowanej treoniny. W niniejszej pracy rozszerzają tę ideę: jeśli gen deacylazy leży obok klastra genów metabolicznych, może on chronić przed lokalnie wytwarzanym, potencjalnie szkodliwym aminokwasem. Dzięki temu deacylaza staje się wygodnym markerem dla inaczej krypticznego klastra genów biosyntetycznych.
Wydobywanie genomów nową soczewką
Skupiając się na jednej rodzinie deacylaz zwanej AlaX, zespół przeanalizował ponad 23 000 powiązanych sekwencji. Stworzyli narzędzie wizualizacyjne tR3D, które mapuje, jak każdy gen deacylazy jest otoczony przez sąsiednie geny w genomie. Większość enzymów AlaX występowała obok genów „domowych” związanych z rutynowym metabolizmem aminokwasów i białek. Jednak około 11 procent znajdowało się w bardziej egzotycznym towarzystwie — blisko transporterów, regulatorów i nietypowych enzymów charakterystycznych dla metabolizmu wtórnego, czyli wyspecjalizowanej chemii mikroorganizmów używanej do obrony lub sygnalizacji. Ta krótka lista obiecujących klastrów zawierała tylko niewielką część należącą do dobrze znanych klas produktów naturalnych, co sugeruje, że wiele pozostałych reprezentuje dotąd przeoczoną chemię.
Nowe cząsteczki z oznaczonych klastrów
Aby sprawdzić strategię, badacze eksperymentalnie zbadali dwa bardzo różne klastry genów oznaczone przez pobliskie deacylazy. Pierwszy, zwarty czterogenowy układ znaleziony w ponad stu gatunkach, koduje prosty enzym, który dodaje grupę hydroksylową do metioniny — powszechnego aminokwasu — tworząc wariant niestandardowy. Towarzysząca deacylaza selektywnie usuwa zmodyfikowaną metioninę z tRNA, chroniąc komórkę przed błędnym rozpoznaniem jej jako normalnego budulca. Drugi klaster, pochodzący z bakterii glebowej, jest bardziej złożony. Łączy enzymy generujące reaktywną jednostkę azot–azot z innymi, które łączą trzy fragmenty pochodzące z aminokwasów. Odtwarzając ten szlak w laboratoryjnych bakteriach i śledząc znakowane substraty, zespół odkrył nowy tripeptyd powiązany wiązaniem hydrazydowym, który nazwali fuscazyną. Jego szkielet zbudowany jest z argininy, alaniny i pierścieniowego pochodnego lizyny, połączonych w nietypowy sposób widywany wcześniej jedynie w bardziej złożonych systemach.
Otwarcie drzwi do przyszłych odkryć
Przykłady te pokazują, że tRNA-deacylazy to nie tylko narzędzia kontroli jakości — wskazują też fragmenty DNA, gdzie ewolucja przesunęła chemię aminokwasów na nowe terytoria. Podążając za tymi drogowskazami, autorzy zidentyfikowali tysiące kandydackich klastrów, z których wiele nie mieści się w standardowych kategoriach używanych w obecnym poszukiwaniu w genomach. Platformę tR3D można stosować także do innych rodzin enzymów, pomagając badaczom skupić się na genach prawdopodobnie kodujących nietypowe reakcje tworzenia wiązań. Dla osób niebędących ekspertami wniosek jest taki: żywe komórki skrywają ogromną bibliotekę chemicznych rozwiązań, a inteligentne sposoby czytania genomów — kierowane przez wbudowane zawory bezpieczeństwa, takie jak deacylazy — zaczynają ją odsłaniać. Każdy nowo odwzorowany szlak nie tylko poszerza podstawowe rozumienie, jak życie buduje cząsteczki, ale też oferuje nowe punkty wyjścia do projektowania leków i biokatalizatorów.
Cytowanie: Millar, D.C., Zhou, Y., Marchand, J.A. et al. tRNA-deacylase-directed discovery of biosynthetic pathways. Nat. Chem. 18, 863–871 (2026). https://doi.org/10.1038/s41557-026-02126-5
Słowa kluczowe: produkty naturalne, niekanoniczne aminokwasy, poszukiwanie w genomie, kontrola jakości tRNA, klastery genów biosyntetycznych