Clear Sky Science · it
Scoperta di vie biosintetiche guidata dalle tRNA-deacilasi
Chimica nascosta all'interno delle cellule viventi
Molti dei farmaci odierni, dagli antidolorifici agli antibiotici e ai farmaci oncologici, hanno avuto origine come piccole molecole prodotte da microbi o piante per i loro scopi. Eppure, anche dopo decenni di ricerche, gli scienziati sospettano che la maggior parte degli stratagemmi chimici della natura resti ancora da scoprire. Questo studio rivela un nuovo modo per individuare vie difficili da trovare nel DNA microbico che costruiscono amminoacidi e brevi peptidi insoliti—molecole che potrebbero diventare i farmaci o gli strumenti di ricerca di domani.
Perché i blocchi costitutivi speciali contano
Gli amminoacidi sono noti soprattutto come mattoni delle proteine, ma le cellule li trasformano anche in una vasta gamma di altri composti. Alcuni sono amminoacidi non standard che contengono elementi rari come il fluoro o l'arsenico, o legami insoliti tra atomi di azoto. Altri vengono cuciti in antibiotici complessi, neuromodulatori come la psilocibina o ormoni peptidici come l'insulina. Poiché queste strutture sono così diverse, i geni che le producono spesso non assomigliano alle famiglie enzimatiche classiche che gli strumenti attuali di ricerca genomica cercano. Di conseguenza, molte delle vie sottostanti rimangono invisibili nelle enormi quantità di DNA microbico che vengono sequenziate oggi.
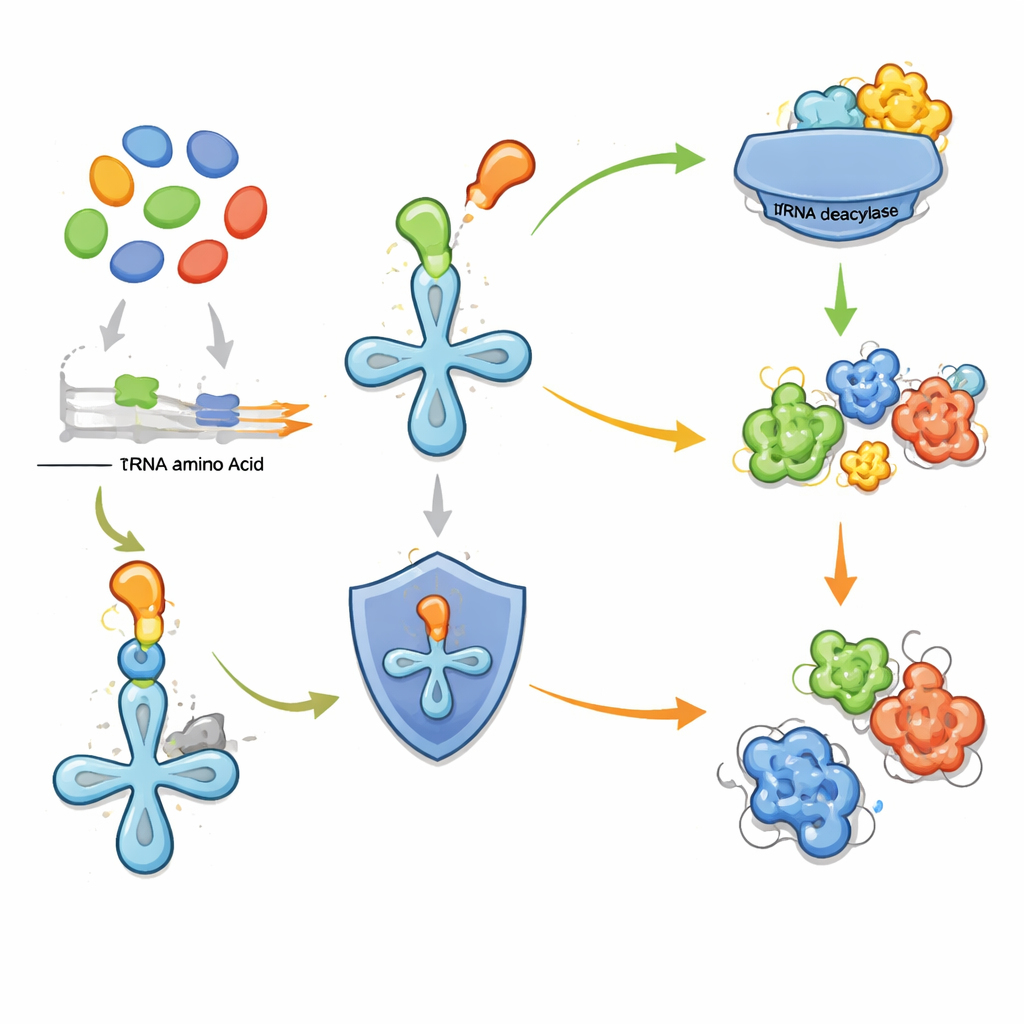
Enzimi di controllo qualità come segnali
L'intuizione chiave del nuovo lavoro è che certi enzimi cellulari di "revisione" possono funzionare da fari per vie vicine che producono amminoacidi strani. Quando una cellula produce un amminoacido non standard, c'è il rischio che venga inserito per errore nelle proteine, compromettendone la funzione. Per evitarlo, alcuni microbi possiedono deacilasi del tRNA autonome—enzimi che rimuovono amminoacidi attaccati in modo scorretto al transfer RNA, gli adattatori che forniscono i mattoni alla macchina proteica. Gli autori avevano precedentemente dimostrato che una di queste deacilasi protegge i batteri dall'uso improprio di una treonina fluorurata. Qui estendono quell'idea: se un gene per una deacilasi si trova accanto a un cluster di altri geni metabolici, potrebbe esserci per difendere dalla presenza locale di un amminoacido potenzialmente dannoso. Questo rende la deacilasi un utile marcatore per un cluster genico biosintetico altrimenti criptico.
Esplorare i genomi con una nuova lente
Concentrandosi su una famiglia di deacilasi chiamata AlaX, il team ha setacciato più di 23.000 sequenze correlate. Hanno costruito uno strumento di visualizzazione, tR3D, che mappa come ogni gene deacilasi è circondato dai suoi vicini nel genoma. La maggior parte degli enzimi AlaX appariva accanto a geni di manutenzione coinvolti nel metabolismo routinario di amminoacidi e proteine. Ma circa l'11 percento si trovava in compagnia più esotica, vicino a trasportatori, regolatori ed enzimi insoliti tipici del metabolismo secondario—la chimica specializzata che i microbi usano per difesa o segnalazione. Questa breve lista di cluster promettenti includeva solo una frazione modesta appartenente a classi di prodotti naturali già note, suggerendo che molti altri rappresentano chimica finora trascurata.
Nuove molecole da cluster segnalati
Per mettere alla prova la strategia, i ricercatori hanno investigato sperimentalmente due cluster genici molto diversi individuati dalle deacilasi vicine. Il primo, un'unità compatta di quattro geni presente in oltre cento specie, codifica per un enzima semplice che aggiunge un gruppo ossidrile alla metionina, un amminoacido comune, creando una variante non standard. La deacilasi partner rimuove selettivamente questa metionina modificata dal transfer RNA, proteggendo la cellula dall'interpretarla come il normale mattone costitutivo. Il secondo cluster, proveniente da un microbo del suolo, è più elaborato. Combina enzimi che generano un'unità reattiva azoto–azoto con altri che uniscono tre frammenti derivati da amminoacidi. Ricostruendo la via in batteri da laboratorio e tracciando materiali di partenza etichettati, il team ha scoperto un nuovo tripeptide legato tramite idrazide che hanno chiamato fuscazine. La sua spina dorsale è costruita da arginina, alanina e un derivato ciclico della lisina, collegati in un modo insolito che era stato osservato precedentemente solo in sistemi più complessi.
Aprire porte a scoperte future
Questi casi di studio mostrano che le deacilasi del tRNA sono più di semplici strumenti di controllo qualità—mettono anche in evidenza quartieri di DNA dove l'evoluzione ha spinto la chimica degli amminoacidi verso nuovi territori. Seguendo questi segnali, gli autori hanno identificato migliaia di cluster candidati, molti dei quali cadono al di fuori delle categorie standard usate nell'attuale genome mining. La loro piattaforma tR3D può essere applicata anche ad altre famiglie enzimatiche, aiutando i ricercatori a focalizzarsi su geni che probabilmente codificano reazioni di formazione di legami insolite. Per i non esperti, il messaggio è che le cellule viventi nascondono una vasta biblioteca di soluzioni chimiche, e modi intelligenti di leggere i genomi—guidati da valvole di sicurezza incorporate come le deacilasi—stanno iniziando a rivelarla. Ogni via mappata di recente non solo amplia la comprensione di base su come la vita costruisce molecole, ma offre anche nuovi punti di partenza per progettare farmaci e biocatalizzatori.
Citazione: Millar, D.C., Zhou, Y., Marchand, J.A. et al. tRNA-deacylase-directed discovery of biosynthetic pathways. Nat. Chem. 18, 863–871 (2026). https://doi.org/10.1038/s41557-026-02126-5
Parole chiave: prodotti naturali, amminoacidi non canonici, mining del genoma, controllo qualità del tRNA, cluster genici biosintetici