Clear Sky Science · zh
层粱病性扩张型心肌病中的端粒缩短
为何心肌细胞的衰老很重要
许多患有遗传性心肌病的人在相对较年轻时就出现严重问题,如心律失常、心力衰竭,甚至需要进行心脏移植。本研究提出了一个看似简单但重要的问题:这些患者的心肌细胞在最基本的DNA层面是否更快地老化?研究者通过仔细观察称为端粒的微小结构——染色体末端的保护帽——来探讨细胞核关键支架蛋白缺陷如何加速心脏细胞的损耗与老化。
DNA末端的保护帽
我们细胞中的每条染色体末端都有一段重复的DNA,类似鞋带的塑料帽,防止磨损和分裂。端粒通常随着年龄缓慢缩短,极短的端粒被视为细胞衰老的标志。在心脏中,大多数心肌细胞在出生后不久就停止分裂,因此其端粒长度预期会相对稳定。该团队此前的工作显示,某些遗传性心脏病打破了这一规律,端粒意外变短。本研究聚焦一类罕见疾病——层粱病(laminopathies),由LMNA基因突变引起,该基因构建细胞核的内壳,帮助维持核的形状和刚性。
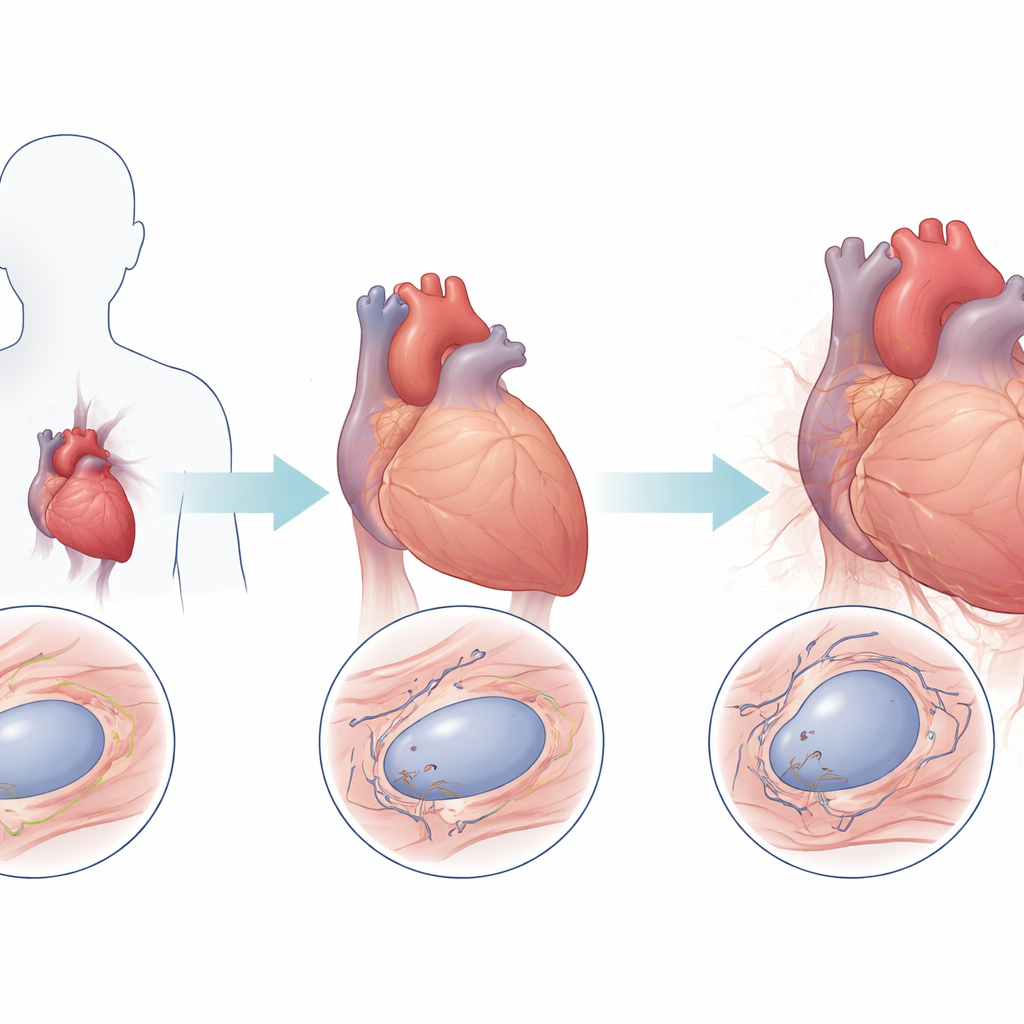
看起来比实际更老的心脏组织
研究小组首先检查了接受心脏移植的不同层粱病患者的心肌活检样本,并将其与无心脏疾病者的心脏进行比较。使用一种荧光技术在单个心肌细胞核中测量端粒信号,他们发现层粱病心脏的端粒平均比对照组低38%。这一模式在数个临床亚型中均有体现,且一种称为LGMD1B的疾病亚型随年龄表现出特别快速的端粒丧失。相比之下,健康心脏的端粒水平随时间保持相当稳定,进一步支持LMNA突变促使心肌细胞端粒异常加速缩短的观点。
在培养皿中模拟病变心肌细胞
为探明因果关系,研究者从携带框移LMNA突变的患者制备了诱导多能干细胞,然后用基因编辑工具生成了配对的细胞系:具有两个正常拷贝、一个突变拷贝或没有功能性LMNA拷贝。在干细胞状态下,补回一个正常的LMNA拷贝会增加端粒长度,而完全丧失LMNA仅产生有限的端粒增加,凸显了核结构与端粒维持之间的微妙平衡。当这些干细胞在实验室中被分化为有节律收缩的心肌细胞时,情况发生变化:缺乏或几乎没有正常LMNA的细胞系表现出明显的端粒丧失,支持这样一个观点:重复收缩的机械应力使核完整性对保持心肌端粒尤为重要。
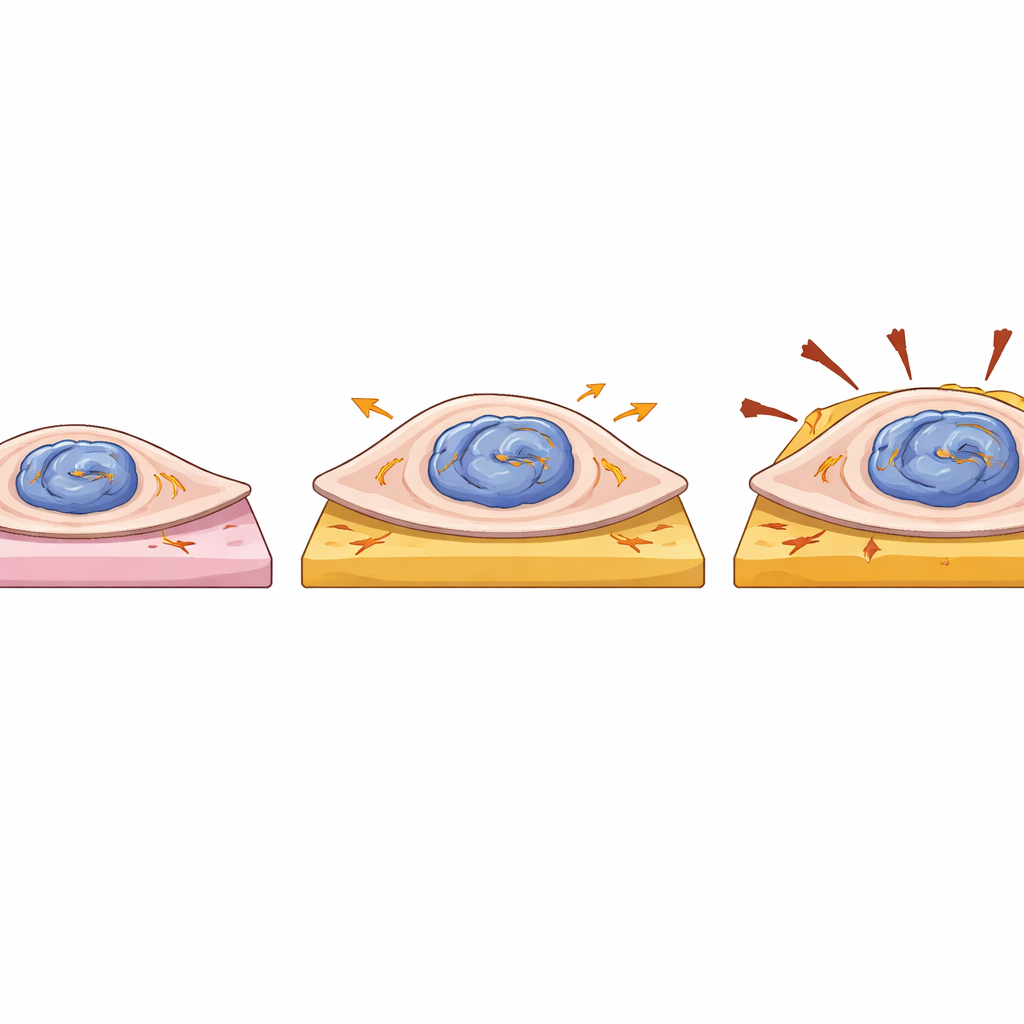
更强但更脆弱的心肌细胞
团队还探讨了该突变如何影响单个心肌细胞的物理行为。他们将来源于患者和已纠正细胞的单个细胞放置在模拟健康或瘢痕化心脏组织的软或硬小凝胶垫上,测量每个细胞收缩时的牵引力。携带一个突变LMNA拷贝的细胞在面积上更大,产生的总体拉力和应变能也高于已纠正的细胞,尤其是在较软的凝胶上。然而,这种增加的力并不伴随更快的收缩,这些细胞显示出节律的小幅不规则,暗示内部信号存在扰动。由于各组间凝胶表面的平均位移相似,额外的力主要来自细胞体积的增大,而非更高效的机械装置。连同细胞核的形变,这提示突变LMNA使心肌细胞更笨重且机械敏感,同时削弱其端粒的保护。
来自人源化小鼠模型的证据
为了检验这些发现是否在整体生物体中成立,研究者使用了工程化携带会产生促衰老蛋白progerin的人源LMNA突变的小鼠。这些小鼠出现了扩张型心肌病的早期迹象,心脏泵血功能降低。它们的心肌细胞端粒明显更短,并且每次收缩时的缩短减少,表明收缩功能受损。这些动物实验结果与人类组织和细胞培养的数据相互呼应,加强了LMNA突变、端粒丧失与心肌衰竭之间的联系。
对未来治疗的意义
简而言之,这项工作表明,细胞核支架的某些遗传缺陷可以使心肌细胞既更加负荷工作又更快衰老——这一点可通过染色体末端保护帽的丧失看到。端粒缩短的程度随具体的LMNA突变和细胞类型而异,这或许有助于解释为什么携带相似基因变化的患者疾病严重程度不同。通过确立端粒侵蚀是层粱病相关心脏病的一致特征,该研究指向端粒保护和核支持作为潜在的新治疗靶点,旨在减缓或预防这类患者的心力衰竭。
引用: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
关键词: 层粱病, 端粒, 扩张型心肌病, 心肌细胞, 细胞衰老