Clear Sky Science · fr
Raccourcissement des télomères dans la cardiomyopathie dilatée laminopathique
Pourquoi le vieillissement des cellules cardiaques compte
De nombreuses personnes atteintes de maladies héréditaires du muscle cardiaque développent des complications sévères — arythmies, insuffisance cardiaque et besoin de greffes — à des âges relativement jeunes. Cette étude pose une question simple mais cruciale : les cellules cardiaques de ces patients vieillissent-elles plus vite au niveau le plus fondamental de leur ADN ? En examinant de près de minuscules structures appelées télomères — des coiffe protectrices aux extrémités des chromosomes — les chercheurs explorent comment une anomalie dans une protéine structurale clé du noyau cellulaire pourrait accélérer l’usure cellulaire dans le cœur.
Des coques protectrices aux extrémités de notre ADN
Chaque chromosome de nos cellules se termine par une série de répétitions d’ADN qui agissent comme l’embout en plastique d’un lacet, empêchant l’effilochage. Ces télomères se raccourcissent normalement lentement avec l’âge, et des télomères très courts sont considérés comme un marqueur du vieillissement cellulaire. Dans le cœur, la plupart des cellules musculaires cessent de se diviser peu après la naissance, si bien que la longueur des télomères devrait rester assez stable. Des travaux antérieurs du groupe ont montré que certaines maladies cardiaques génétiques enfreignent cette règle, avec des télomères devenant anormalement courts. Ici, l’attention se porte sur une famille de troubles rares appelés laminopathies, causés par des mutations du gène LMNA, qui construit l’enveloppe interne du noyau cellulaire et contribue à maintenir sa forme et sa rigidité.
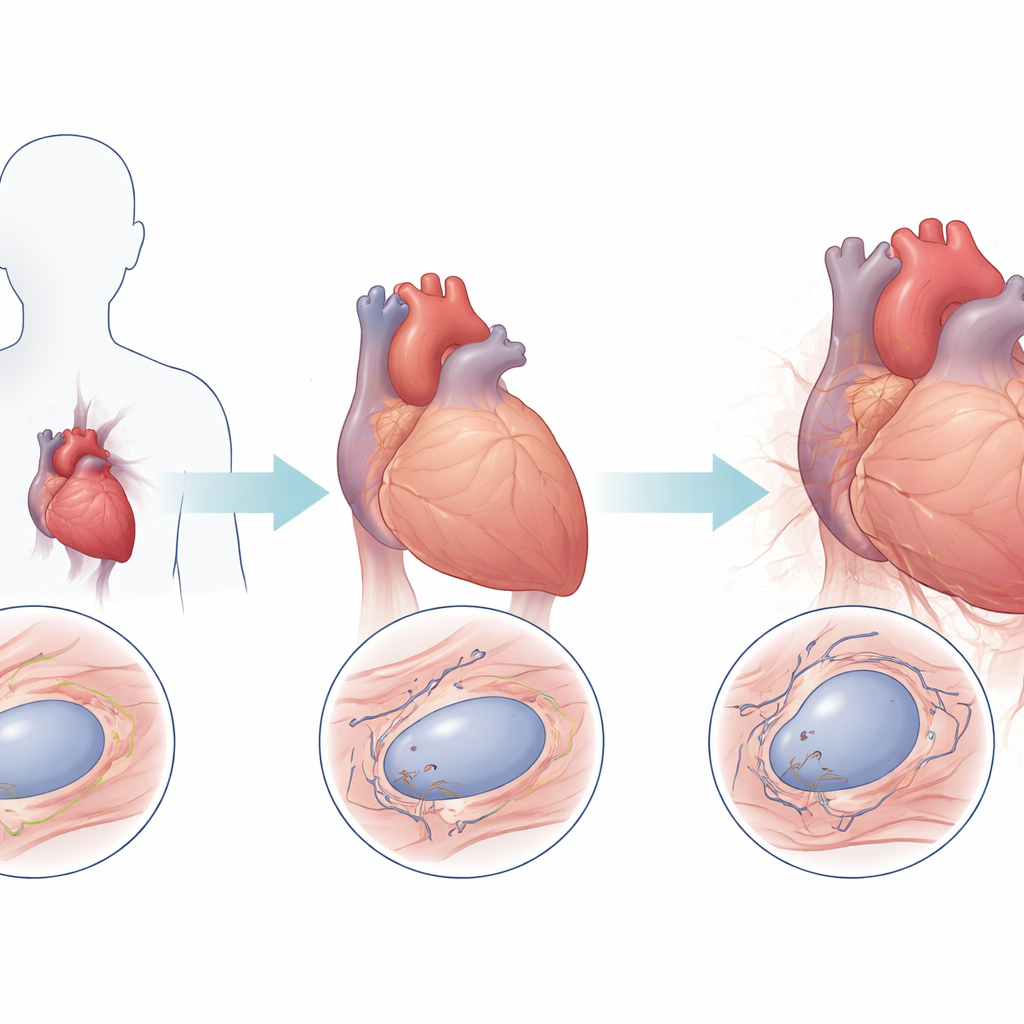
Un tissu cardiaque qui paraît plus âgé qu’il ne devrait
L’équipe a d’abord examiné des échantillons de biopsies cardiaques prélevés chez des patients atteints de différentes formes de laminopathie ayant subi une transplantation cardiaque, et les a comparés à des cœurs de personnes sans maladie cardiaque. En utilisant une technique fluorescente qui mesure les signaux télomériques dans les noyaux des cellules myocardiques individuelles, ils ont constaté que les cœurs laminopathiques présentaient en moyenne 38 % de signal télomérique en moins que les témoins. Ce schéma se retrouvait dans plusieurs sous-types cliniques, et les patients atteints d’une forme de la maladie appelée LGMD1B montraient une perte de télomères particulièrement rapide avec l’âge. En revanche, les niveaux de télomères dans les cœurs sains restaient remarquablement stables au fil du temps, renforçant l’idée que les mutations de LMNA entraînent une accélération anormale du raccourcissement des télomères dans les cellules cardiaques.
Modéliser des cellules cardiaques malades en laboratoire
Pour étudier la relation de cause à effet, les chercheurs ont créé des cellules souches pluripotentes induites à partir d’un patient porteur d’une mutation décalant le cadre de lecture du LMNA, puis ont utilisé des outils d’édition génétique pour générer des lignées cellulaires appariées contenant deux copies normales, une copie mutée ou aucune copie fonctionnelle de LMNA. À l’état de cellules souches, la réintroduction d’une copie normale de LMNA augmentait la longueur des télomères, tandis que la perte complète de LMNA produisait seulement de modestes gains télomériques, soulignant un équilibre délicat entre la structure nucléaire et l’entretien des télomères. Lorsque ces cellules souches ont été différenciées en cellules cardiaques battantes en laboratoire, le tableau a changé : les lignées avec peu ou pas de LMNA normale montraient une perte télomérique marquée, soutenant l’idée que le stress mécanique lié aux contractions répétées rend l’intégrité nucléaire particulièrement importante pour préserver les télomères dans le muscle cardiaque.
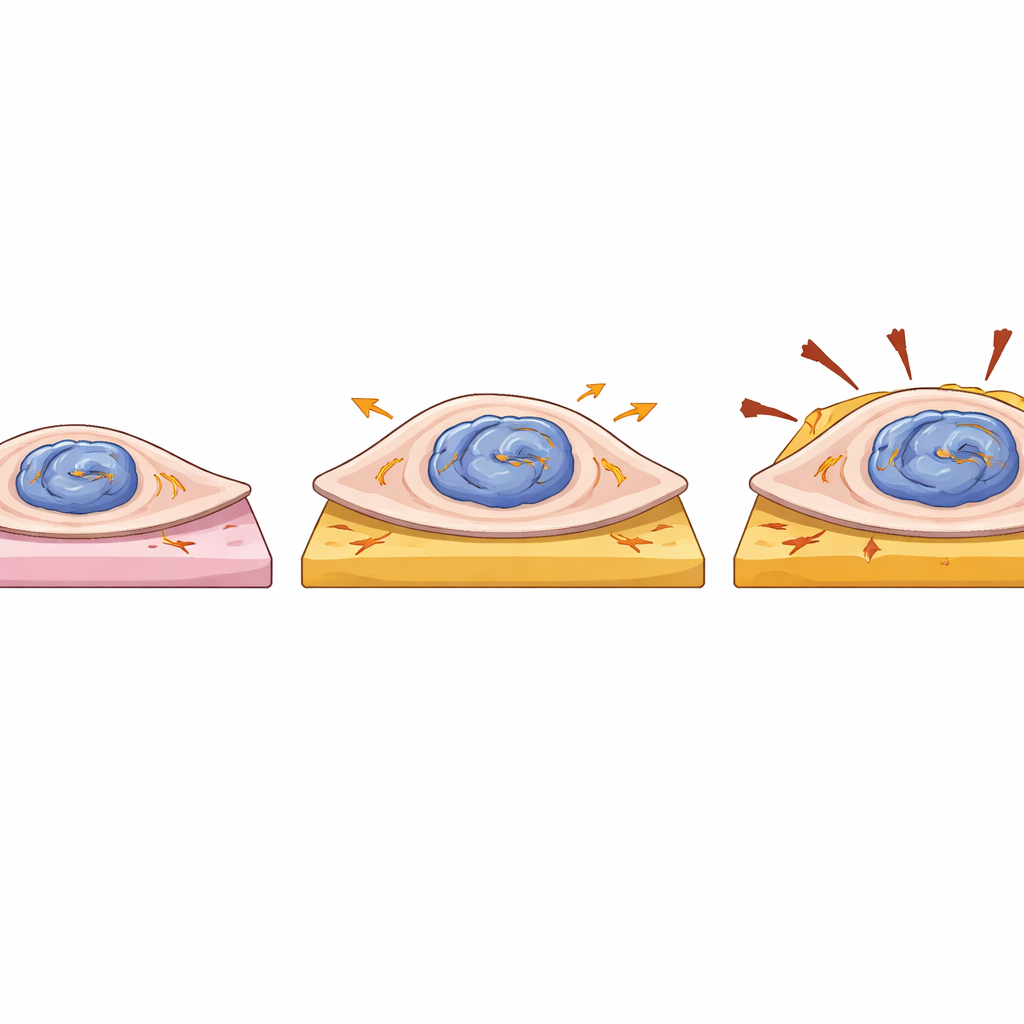
Des cellules cardiaques plus puissantes mais plus fragiles
L’équipe a aussi étudié comment la mutation affecte le comportement physique de cellules cardiaques isolées. Ils ont placé des cellules individuelles dérivées du patient et des cellules corrigées sur de petites pastilles de gel moulées, souples ou rigides, imitant respectivement un tissu cardiaque sain ou cicatriciel, et ont mesuré la force exercée par chaque cellule lors de la contraction. Les cellules portant une copie mutante de LMNA étaient plus étendues en surface et généraient une force globale et une énergie de déformation supérieures à celles des cellules corrigées, en particulier sur les gels mous. Cependant, cette force accrue n’était pas accompagnée d’une contraction plus rapide, et ces cellules présentaient de subtiles irrégularités de fréquence de battement, suggérant des perturbations du signal interne. Comme le déplacement moyen de la surface du gel était similaire entre les groupes, la force supplémentaire semble provenir principalement d’une augmentation de la taille cellulaire, et non d’une machinerie plus efficace. Avec la déformation nucléaire observée, cela suggère que LMNA mutant rend les cellules cardiaques plus volumineuses et plus sensible mécaniquement, tout en érodant leur protection télomérique.
Preuves issues d’un modèle murin humanisé
Pour vérifier si ces observations se maintiennent dans un organisme entier, les chercheurs ont utilisé des souris ingénéées pour porter une mutation humaine de LMNA qui produit la progerine, la protéine altérée responsable d’un syndrome de vieillissement prématuré. Ces souris ont développé des signes précoces de cardiomyopathie dilatée, avec une performance de pompage réduite. Leurs cellules musculaires cardiaques présentaient également des télomères significativement plus courts et montraient une réduction de l’abaissement lors de chaque battement, indiquant un défaut de la fonction contractile. Ces résultats animaux reflètent les données issues des tissus humains et des cultures cellulaires, renforçant le lien entre mutation de LMNA, perte de télomères et défaillance du muscle cardiaque.
Ce que cela implique pour les soins futurs
En termes simples, ce travail montre que certains défauts héréditaires de l’armature du noyau cellulaire peuvent amener les cellules du muscle cardiaque à travailler davantage et à vieillir plus vite, comme le révèle la perte de leurs coques chromosomiques. L’importance du raccourcissement télomérique varie selon la mutation spécifique de LMNA et le type cellulaire, ce qui peut contribuer à expliquer pourquoi des patients portant des altérations génétiques semblables présentent des sévérités de maladie différentes. En établissant que l’érosion des télomères est une caractéristique cohérente de la cardiopathie liée aux laminopathies, l’étude pointe vers la protection des télomères et le soutien nucléaire comme cibles potentielles pour des thérapies visant à ralentir ou prévenir l’insuffisance cardiaque chez ces patients.
Citation: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Mots-clés: laminopathie, télomères, cardiomyopathie dilatée, cellules du muscle cardiaque, vieillissement cellulaire