Clear Sky Science · pl
Skracanie telomerów w laminopatycznym kardiomiopatii rozstrzeniowej
Dlaczego starzenie komórek serca ma znaczenie
Wiele osób z dziedzicznymi chorobami mięśnia sercowego rozwija poważne problemy, takie jak zaburzenia rytmu, niewydolność serca i konieczność przeszczepu, w stosunkowo młodym wieku. W tym badaniu zadano proste, ale istotne pytanie: czy komórki serca u tych pacjentów starzeją się szybciej na najpodstawniejszym poziomie ich DNA? Poprzez szczegółową analizę drobnych struktur zwanych telomerami — ochronnymi nasadkami na chromosomach — badacze badają, jak wada w kluczowym białku rusztowania jądra komórkowego może przyspieszać zużycie komórek serca.
Ochronne nasadki na końcach naszego DNA
Każdy chromosom w naszych komórkach kończy się odcinkiem powtarzalnego DNA, który działa jak plastikowy kołnierzyk sznurowadła, zapobiegając strzępieniu. Telomery skracają się zwykle powoli wraz z wiekiem, a bardzo krótkie telomery są uważane za znak starzenia komórkowego. W sercu większość komórek mięśniowych przestaje się dzielić wkrótce po urodzeniu, więc spodziewa się, że długość telomerów pozostaje stosunkowo stała. Wcześniejsze prace tej grupy wykazały jednak, że niektóre genetyczne choroby serca łamią tę zasadę, a telomery stają się niespodziewanie krótkie. Tutaj skupiono się na rodzinie rzadkich schorzeń zwanych laminopatiami, wywołanych mutacjami w genie LMNA, który buduje wewnętrzną powłokę jądra komórkowego i pomaga utrzymać jego kształt oraz sztywność.
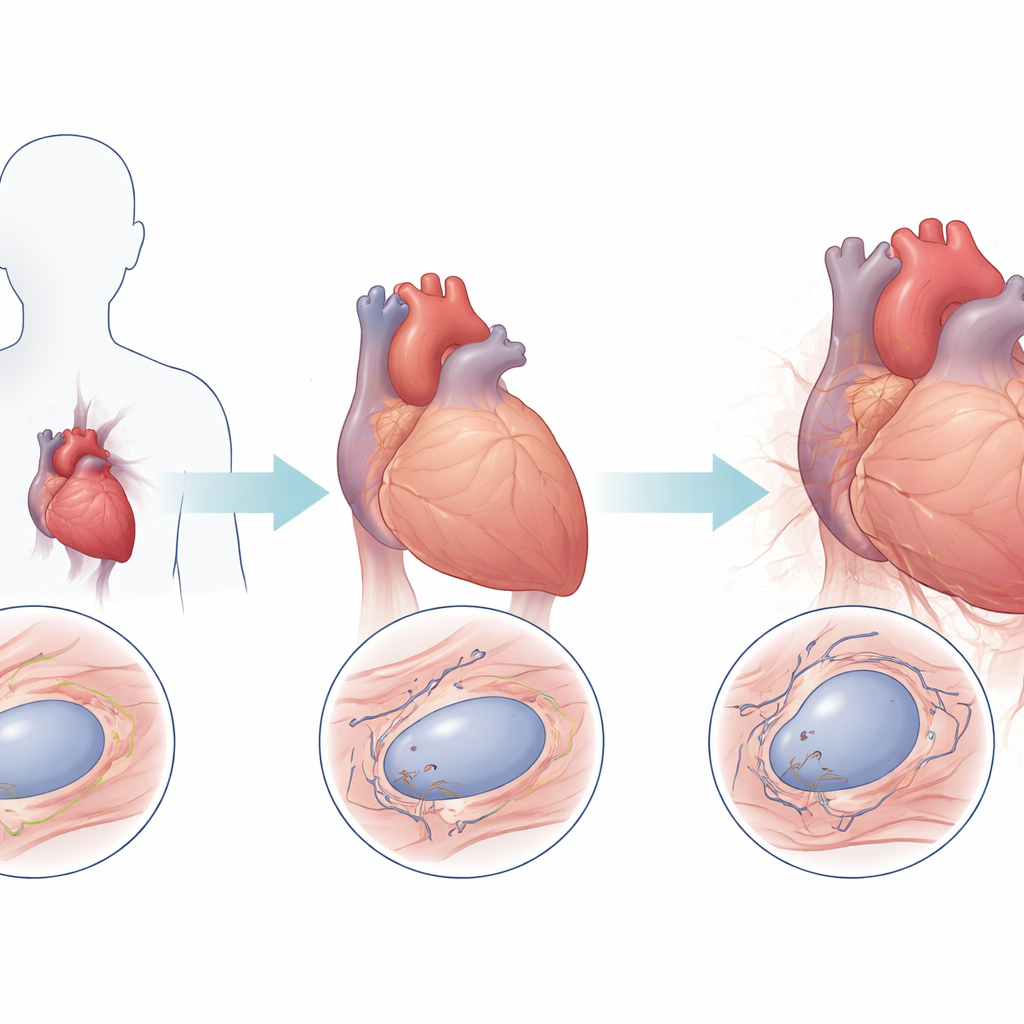
Tkanka serca wyglądająca na starszą niż powinna
Zespół najpierw przeanalizował próbki bioptatów serca od pacjentów z różnymi postaciami laminopatii, którzy przeszli przeszczep serca, i porównał je z sercami osób bez chorób serca. Za pomocą techniki fluorescencyjnej mierzącej sygnały telomerowe w pojedynczych jądrach komórek mięśnia sercowego stwierdzono, że serca z laminopatią miały średnio o 38 procent niższy poziom telomerów niż grupy kontrolne. Wzór ten utrzymywał się w różnych podtypach klinicznych, a pacjenci z jedną postacią choroby, nazwaną LGMD1B, wykazywali szczególnie szybkie skracanie telomerów wraz z wiekiem. W przeciwieństwie do tego, poziomy telomerów w zdrowych sercach były zadziwiająco stabilne w czasie, co wzmacnia ideę, że mutacje LMNA napędzają nieprawidłowe przyspieszenie skracania telomerów w komórkach serca.
Modelowanie chorych komórek serca na szalce laboratoryjnej
Aby zbadać związek przyczynowo-skutkowy, badacze stworzyli indukowane komórki macierzyste pluripotentne od pacjenta z mutacją ramkową w genie LMNA, a następnie użyli narzędzi do edycji genów, by wygenerować dopasowane linie komórkowe z dwiema normalnymi kopiami, jedną zmutowaną kopią lub bez funkcjonalnych kopii LMNA. W stanie komórek macierzystych przywrócenie normalnej kopii LMNA zwiększało długość telomerów, podczas gdy całkowita utrata LMNA dawała jedynie skromne przyrosty telomerów, podkreślając delikatną równowagę między strukturą jądra a utrzymaniem telomerów. Gdy te komórki macierzyste przekształcono w bijące komórki serca w laboratorium, obraz się zmienił: linie z małą liczbą lub brakiem normalnego LMNA wykazywały wyraźne ubytki telomerów, co wspiera koncepcję, że mechaniczny stres powtarzających się skurczów czyni integralność jądra szczególnie ważną dla zachowania telomerów w mięśniu sercowym.
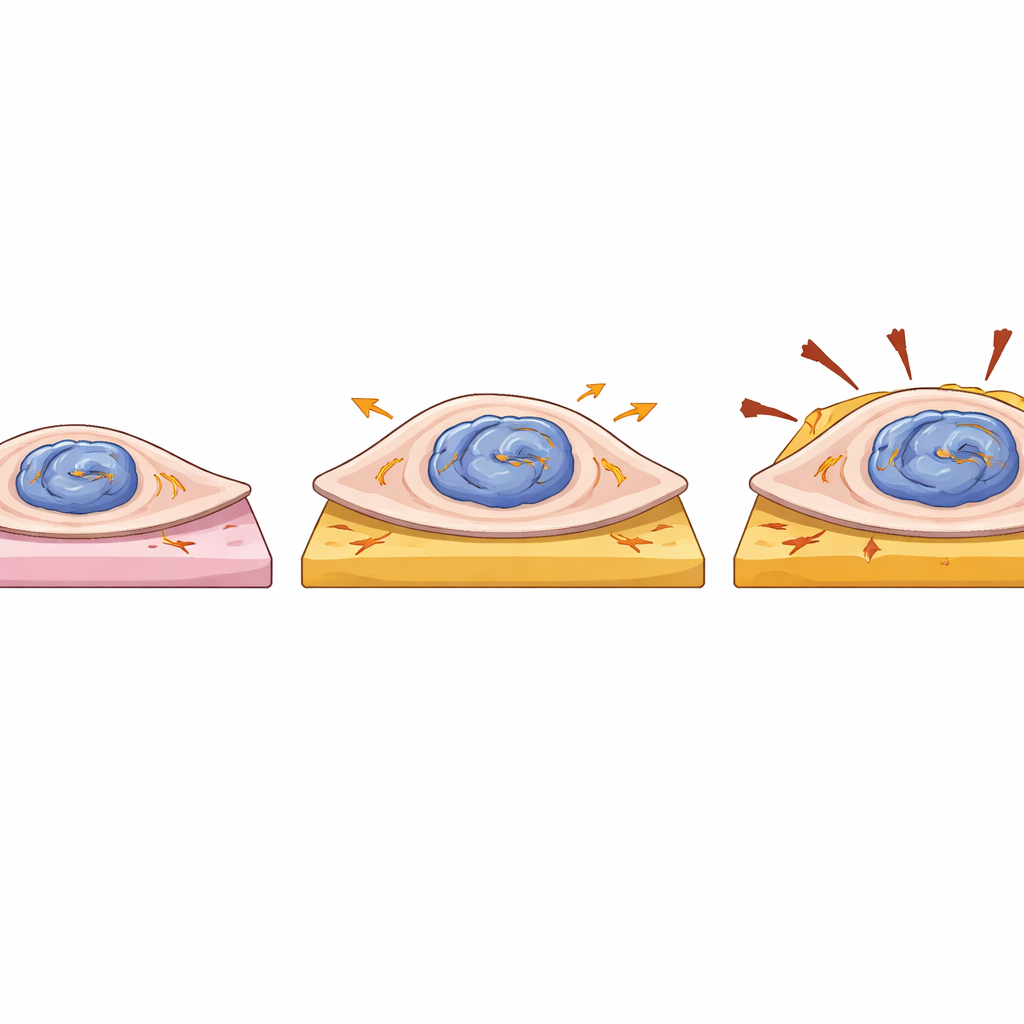
Mocniejsze, lecz bardziej kruche komórki serca
Zespół zapytał także, jak mutacja wpływa na zachowanie fizyczne pojedynczych komórek serca. Umieścili pojedyncze komórki pochodzące od pacjenta oraz skorygowane komórki na małych, miękkich lub twardych podkładach żelowych naśladujących zdrową i zbliznowaciałą tkankę serca i zmierzyli, jak mocno każda komórka ciągnie podczas skurczu. Komórki niosące jedną zmutowaną kopię LMNA miały większą powierzchnię i generowały większą całkowitą siłę oraz energię odkształcenia niż ich skorygowane odpowiedniki, szczególnie na miększych żelach. Jednak zwiększona siła nie szła w parze z szybszym skurczem, a te komórki wykazywały subtelne nieregularności w rytmie bicia, sugerując zaburzenia wewnętrznego sygnalizowania. Ponieważ średnie przemieszczenie powierzchni żelu było podobne między grupami, dodatkowa siła wydaje się wynikać głównie ze zwiększonego rozmiaru komórki, a nie bardziej wydajnego mechanizmu. W połączeniu z deformacją jądra sugeruje to, że zmutowane LMNA sprawia, iż komórki serca stają się masywniejsze i bardziej mechanicznie wrażliwe, jednocześnie osłabiając ochronę ich telomerów.
Dane z humanizowanego modelu mysiego
Aby sprawdzić, czy te odkrycia utrzymują się w całym organizmie, badacze sięgnęli po myszy zaprojektowane tak, by nosić ludzką mutację LMNA prowadzącą do produkcji progeryny — zmienionego białka odpowiedzialnego za zespół przedwczesnego starzenia. Te myszy rozwinęły wczesne objawy kardiomiopatii rozstrzeniowej z obniżoną wydolnością skurczową. Komórki mięśnia sercowego miały także znacząco krótsze telomery i wykazywały zmniejszone skracanie podczas każdego skurczu, co wskazuje na upośledzoną funkcję kurczliwą. Wyniki u zwierząt odzwierciedlają dane z tkanek ludzkich i hodowli komórkowych, wzmacniając związek między mutacją LMNA, utratą telomerów i niewydolnością mięśnia sercowego.
Co to oznacza dla przyszłej opieki
Mówiąc prosto, praca ta pokazuje, że niektóre wrodzone defekty rusztowania jądra komórkowego mogą sprawić, że komórki mięśnia sercowego będą zarówno pracować ciężej, jak i starzeć się szybciej, co widać po utracie ich nasadek chromosomowych. Stopień skracania telomerów zależy od konkretnej mutacji LMNA i typu komórki, co może pomóc wyjaśnić, dlaczego pacjenci z podobnymi zmianami genetycznymi mogą mieć różne nasilenie choroby. Ustanowienie, że erozja telomerów jest spójną cechą związanej z laminopatią choroby serca, wskazuje na ochronę telomerów i wsparcie jądra jako potencjalne nowe cele terapeutyczne ukierunkowane na spowolnienie lub zapobieganie niewydolności serca u tych pacjentów.
Cytowanie: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Słowa kluczowe: laminopatia, telomery, kardiomiopatia rozstrzeniowa, komórki mięśnia sercowego, starzenie komórkowe