Clear Sky Science · pt
Encurtamento de telômeros na cardiomiopatia dilatada laminopática
Por que o envelhecimento das células cardíacas importa
Muitas pessoas com doenças hereditárias do músculo cardíaco desenvolvem problemas graves, como ritmos cardíacos irregulares, insuficiência cardíaca e a necessidade de transplante, em idades relativamente precoces. Este estudo faz uma pergunta simples, porém importante: as células do coração desses pacientes envelhecem mais rápido no nível mais básico do DNA? Ao investigar de perto estruturas minúsculas chamadas telômeros — tampas protetoras nos cromossomos — os pesquisadores exploram como uma falha em uma proteína chave da “armação” do núcleo celular pode acelerar o desgaste celular no coração.
Tampas protetoras nas extremidades do nosso DNA
Cada cromossomo nas nossas células termina com um trecho de DNA repetido que age como a ponta plástica de um cadarço, evitando que ele desfie. Esses telômeros normalmente encurtam lentamente conforme envelhecemos, e telômeros muito curtos são considerados uma marca do envelhecimento celular. No coração, a maioria das células musculares para de se dividir logo após o nascimento, de modo que o comprimento dos telômeros tende a permanecer relativamente estável. Trabalhos anteriores desse grupo mostraram que certas doenças cardíacas genéticas violam essa regra, com telômeros ficando inesperadamente curtos. Aqui, o foco é numa família de doenças raras chamadas laminopatias, causadas por mutações no gene LMNA, que constrói a “casca” interna do núcleo celular e ajuda a manter sua forma e rigidez.
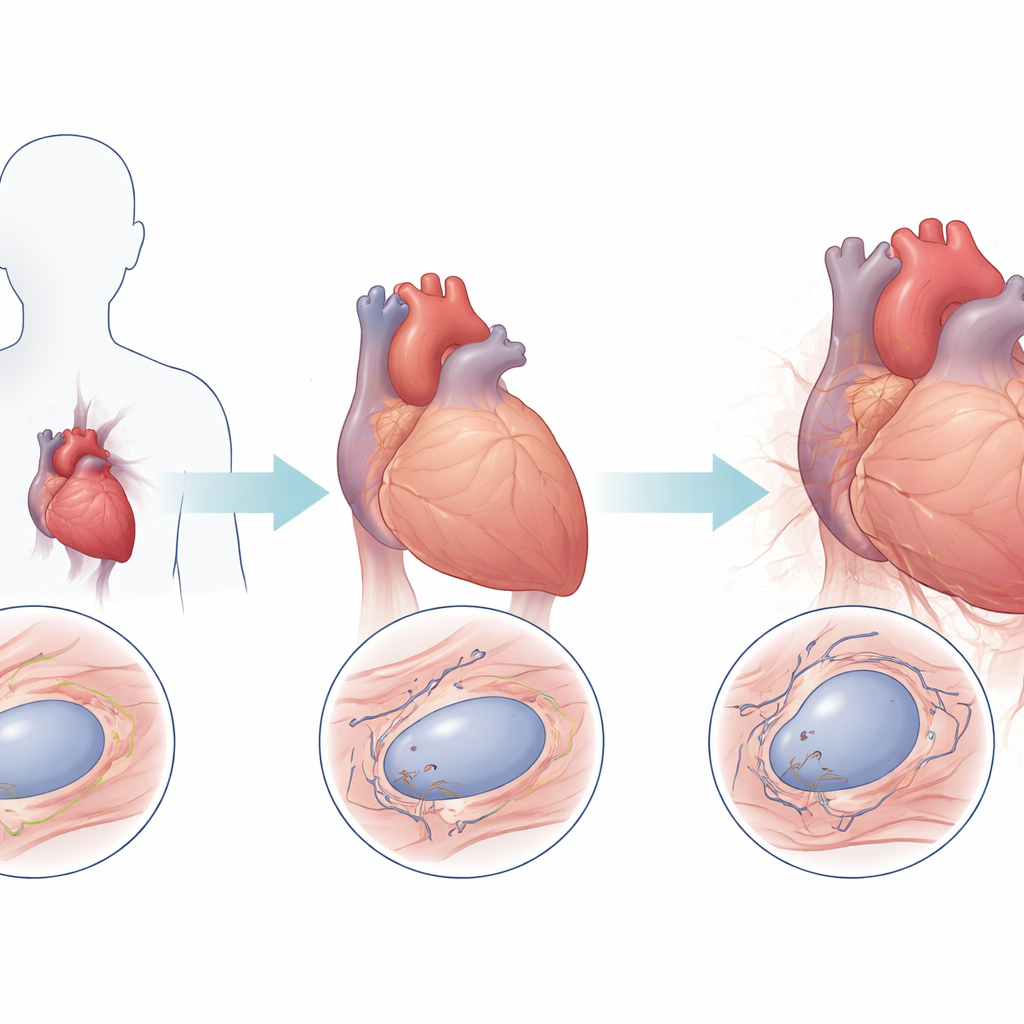
Tecido cardíaco que parece mais velho do que deveria
O grupo primeiro examinou amostras de biópsia cardíaca de pacientes com diferentes formas de laminopatia que haviam passado por transplante de coração e as comparou com corações de pessoas sem doença cardíaca. Usando uma técnica fluorescente que mede sinais de telômero nos núcleos de células musculares cardíacas individuais, eles descobriram que os corações com laminopatia tinham, em média, níveis de telômero 38% menores do que os controles. Esse padrão se manteve em vários subtipos clínicos, e pacientes com uma forma da doença, chamada LGMD1B, apresentaram perda de telômeros especialmente rápida com a idade. Em contraste, os níveis de telômero em corações saudáveis foram notavelmente estáveis ao longo do tempo, reforçando a ideia de que mutações em LMNA promovem uma aceleração anormal do encurtamento de telômeros nas células do coração.
Modelando células cardíacas doentes em cultura
Para investigar causa e efeito, os pesquisadores criaram células-tronco pluripotentes induzidas a partir de um paciente portador de uma mutação frameshift em LMNA e, em seguida, usaram ferramentas de edição genética para gerar linhagens celulares pareadas com duas cópias normais, uma cópia mutada ou nenhuma cópia funcional de LMNA. No estado de célula-tronco, adicionar de volta uma cópia normal de LMNA aumentou o comprimento dos telômeros, enquanto a perda completa de LMNA produziu apenas ganhos modestos, destacando um equilíbrio delicado entre a estrutura nuclear e a manutenção dos telômeros. Quando essas células-tronco foram transformadas em células cardíacas pulsantes no laboratório, o quadro mudou: linhagens com pouca ou nenhuma LMNA normal exibiram perda pronunciada de telômeros, apoiando a ideia de que o estresse mecânico da contração repetida torna a integridade nuclear especialmente importante para preservar telômeros no músculo cardíaco.
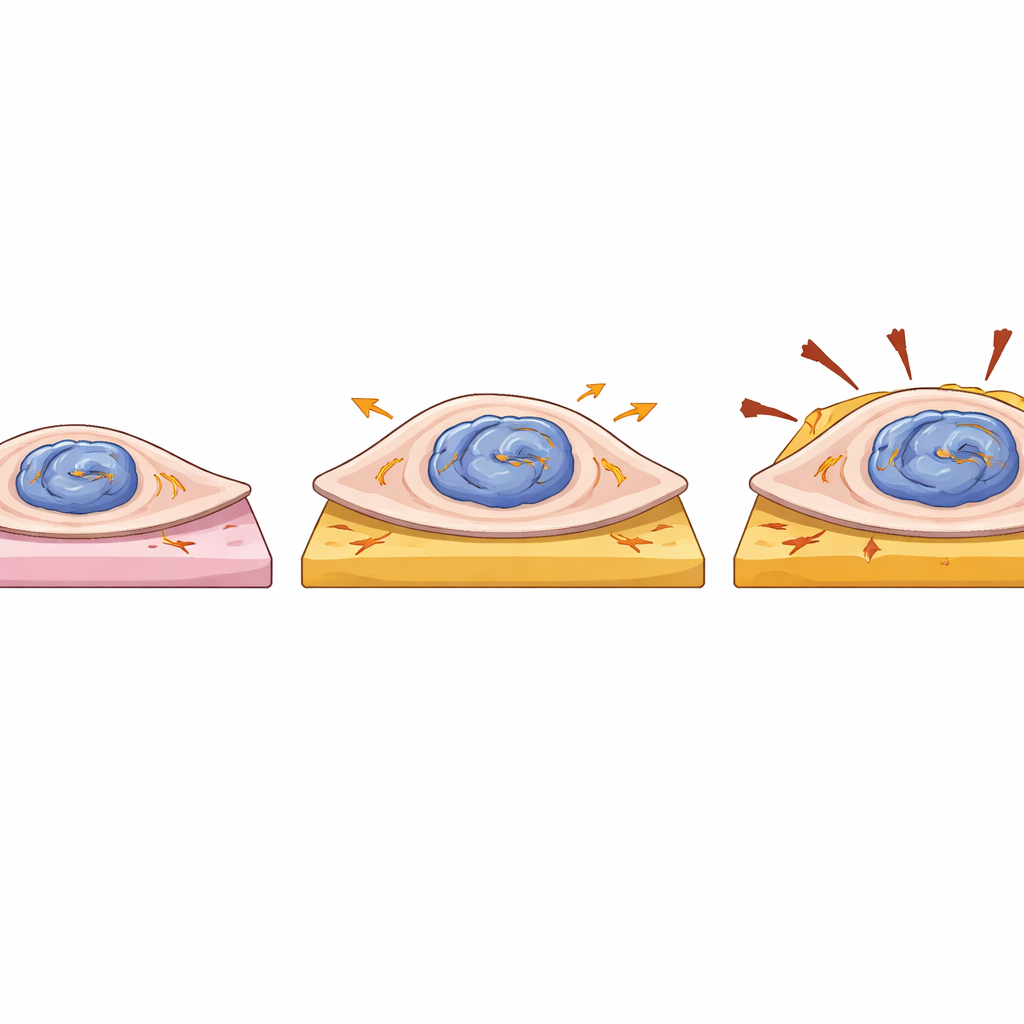
Células cardíacas mais fortes, porém mais frágeis
Os pesquisadores também investigaram como a mutação afeta o comportamento físico de células cardíacas individuais. Eles colocaram células derivadas do paciente e células corrigidas sobre pequenos tapetes de gel macios ou rígidos que imitam tecido cardíaco saudável e cicatrizado, e mediram com que força cada célula puxava ao contrair. Células que carregavam uma cópia mutante de LMNA eram maiores em área e geravam maior força total e energia de deformação do que suas contrapartes corrigidas, particularmente em géis mais macios. No entanto, esse aumento de força não veio com contrações mais rápidas, e essas células mostraram sutis irregularidades na frequência de batimento, sugerindo alteração na sinalização interna. Como o movimento médio da superfície do gel foi semelhante entre os grupos, a força extra parece derivar principalmente do aumento do tamanho celular, não de uma maquinaria mais eficiente. Junto com a deformação do núcleo, isso sugere que a LMNA mutante torna as células cardíacas mais volumosas e mecanicamente sensíveis, ao mesmo tempo em que corrói sua proteção telomérica.
Evidência de um modelo murino humanizado
Para verificar se essas descobertas se mantêm em um organismo inteiro, os pesquisadores recorreram a camundongos geneticamente modificados para carregar uma mutação humana em LMNA que produz progerina, a proteína alterada responsável por uma síndrome de envelhecimento precoce. Esses camundongos desenvolveram sinais precoces de cardiomiopatia dilatada, com desempenho de bombeamento reduzido. As células do músculo cardíaco deles também apresentaram telômeros significativamente mais curtos e mostraram encurtamento reduzido a cada batida, apontando para função contrátil prejudicada. Esses resultados em animais espelham os dados de tecido humano e cultura celular, fortalecendo a ligação entre mutação em LMNA, perda de telômeros e falha do músculo cardíaco.
O que isso significa para cuidados futuros
Em termos simples, este trabalho mostra que certos defeitos herdados na “armação” do núcleo celular podem fazer com que as células do músculo cardíaco trabalhem mais e envelheçam mais depressa, como evidenciado pela perda das tampas nas extremidades dos cromossomos. O grau de encurtamento dos telômeros varia com a mutação específica em LMNA e o tipo de célula, o que pode ajudar a explicar por que pacientes com alterações genéticas semelhantes apresentam gravidades diferentes da doença. Ao estabelecer que a erosão dos telômeros é uma característica consistente da doença cardíaca relacionada à laminopatia, o estudo aponta a proteção dos telômeros e o suporte nuclear como potenciais novos alvos terapêuticos para desacelerar ou prevenir a insuficiência cardíaca nesses pacientes.
Citação: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Palavras-chave: laminopatia, telômeros, cardiomiopatia dilatada, células do músculo cardíaco, envelhecimento celular