Clear Sky Science · sv
Telomerförkortning vid laminopatisk dilaterad kardiomyopati
Varför hjärtmuskelcellers åldrande spelar roll
Många personer med ärftliga hjärtmuskelsjukdomar utvecklar tidigt allvarliga problem som oregelbundna hjärtrytmer, hjärtsvikt och behov av transplantation. Denna studie ställer en enkel men viktig fråga: åldras hjärtmuskelcellerna hos dessa patienter snabbare på den mest grundläggande DNA-nivån? Genom att noggrant undersöka små strukturer kallade telomerer — skyddande mössor på kromosomerna — utforskar forskarna hur en defekt i ett nyckelprotein i cellkärnans stomme kan påskynda cellulärt slitage i hjärtat.
Skyddande mössor i slutet av vårt DNA
Varje kromosom i våra celler slutar i en sträcka av upprepade DNA-sekvenser som fungerar som plastspetsen på en skosnöre och hindrar att den fransar upp sig. Dessa telomerer förkortas normalt långsamt när vi åldras, och mycket korta telomerer betraktas som ett kännetecken för cellulärt åldrande. I hjärtat slutar de flesta muskelceller dela sig strax efter födseln, så deras telomerlängd förväntas förbli relativt stabil. Tidigare arbete från denna grupp visade att vissa ärftliga hjärtsjukdomar bryter mot denna regel och att telomererna blir oväntat korta. Här ligger fokus på en familj sällsynta sjukdomar som kallas laminopatier, orsakade av mutationer i LMNA-genen, vilken bygger upp cellkärnans inre skal och hjälper till att bevara dess form och styvhet.
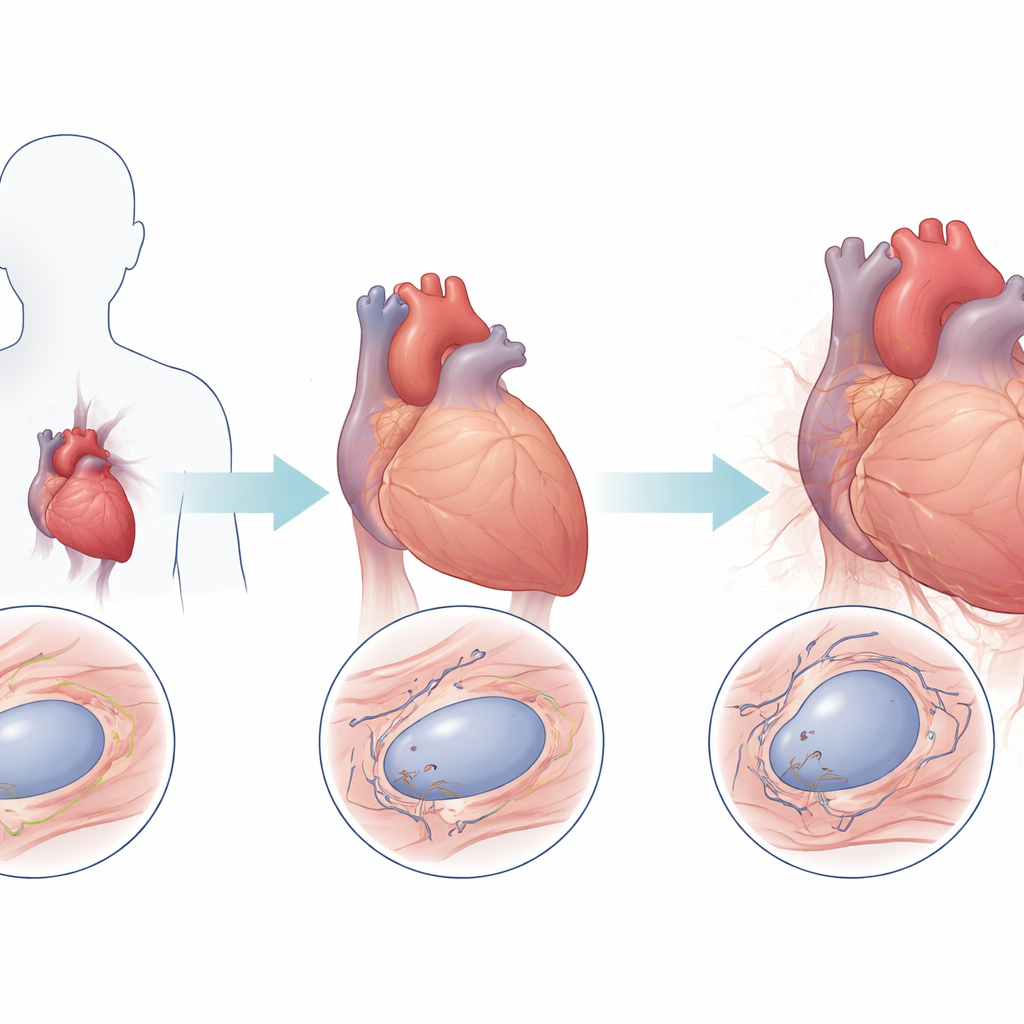
Hjärtvävnad som ser äldre ut än den borde
Forskargruppen undersökte först hjärtbiopsier från patienter med olika former av laminopati som genomgått hjärttransplantation och jämförde dem med hjärtan från personer utan hjärtsjukdom. Med en fluorescerande teknik som mäter telomersignaler i enskilda hjärtmuskelkärnor fann de att laminopati-hjärtan i genomsnitt hade 38 procent lägre telomernivåer än kontroller. Detta mönster höll i flera kliniska undertyper, och patienter med en form av sjukdomen kallad LGMD1B visade särskilt snabb telomerförlust med åldern. Däremot var telomernivåerna i friska hjärtan anmärkningsvärt stabila över tid, vilket stärker idén att LMNA-mutationer driver en onormal acceleration av telomerförkortning i hjärtmuskelceller.
Att modellera sjuka hjärtceller i skålar
För att undersöka orsak och verkan skapade forskarna inducerade pluripotenta stamceller från en patient med en frameshift-mutation i LMNA, och använde sedan genredigering för att generera matchade cellinjer med två normala kopior, en muterad kopia eller inga funktionella kopior av LMNA. I stamcellstillståndet ökade återinförd normal LMNA telomerlängden, medan komplett förlust av LMNA bara gav måttliga telomerökningar — vilket visar på en känslig balans mellan kärnstruktur och telomerunderhåll. När dessa stamceller differentierades till pulserande hjärtceller i labbet ändrades bilden: linjer med lite eller ingen normal LMNA visade uttalad telomerförlust, vilket stöder hypotesen att det mekaniska slitage som följer av upprepad kontraktion gör kärnans integritet särskilt viktig för att bevara telomerer i hjärtmuskel.
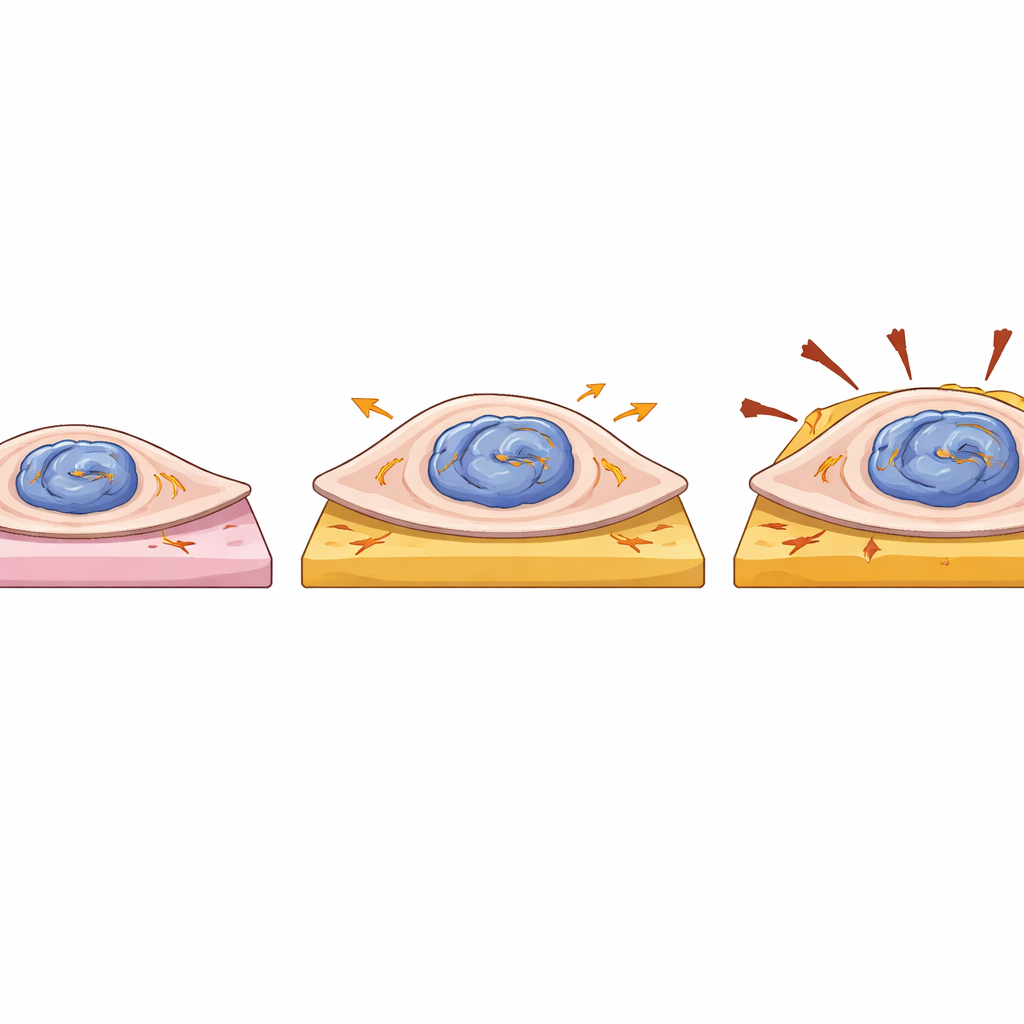
Starkare men mer sköra hjärtceller
Teamet undersökte också hur mutationen påverkar den fysiska beteendet hos enskilda hjärtceller. De placerade individuella patientavledda och korrigerade celler på små, mjuka eller styva gelplattor som efterliknar frisk respektive ärrad hjärtvävnad, och mätte hur hårt varje cell drog när den kontraherade. Celler med en muterad LMNA-kopia var större i yta och genererade större total kraft och mer energi i deformation än sina korrigerade motsvarigheter, särskilt på mjukare geler. Denna ökade kraft förenades dock inte med snabbare kontraktion, och dessa celler visade subtila oregelbundenheter i slagfrekvens, vilket antyder rubbningar i intern signalering. Eftersom den genomsnittliga förflyttningen av gelens yta var likartad mellan grupperna verkar den extra kraften huvudsakligen bero på ökad cellstorlek snarare än effektivare maskineri. Tillsammans med kärnans deformation tyder detta på att muterat LMNA gör hjärtcellerna grövre och mer mekaniskt känsliga, samtidigt som deras telomerskydd eroderas.
Bevis från en humaniserad musmodell
För att se om dessa fynd gäller i en hel organism använde forskarna möss konstruerade att bära en mänsklig LMNA-mutation som producerar progerin, det förändrade proteinet som ligger bakom ett förtidigt åldrande-syndrom. Dessa möss utvecklade tidiga tecken på dilaterad kardiomyopati med nedsatt pumpfunktion. Deras hjärtmuskelceller hade också avsevärt kortare telomerer och visade minskad förkortning under varje slag, vilket pekar på nedsatt kontraktil funktion. Dessa djurdata speglar fynden i mänsklig vävnad och cellodling och stärker sambandet mellan LMNA-mutation, telomerförlust och sviktande hjärtmuskel.
Vad detta innebär för framtida vård
Kort sagt visar detta arbete att vissa ärftliga defekter i cellkärnans stomme kan göra att hjärtmuskelceller både arbetar hårdare och åldras snabbare, mätt som förlust av deras kromosomändmössor. Graden av telomerförkortning varierar med den specifika LMNA-mutation och celltyp, vilket kan hjälpa förklara varför patienter med liknande genförändringar kan få olika sjukdomsbild. Genom att etablera att telomererosion är ett konsekvent inslag i laminopati-relaterad hjärtsjukdom pekar studien mot telomerskydd och kärnstöd som potentiella nya mål för terapier som syftar till att bromsa eller förebygga hjärtsvikt hos dessa patienter.
Citering: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Nyckelord: laminopati, telomerer, dilaterad kardiomyopati, hjärtmuskelceller, cellulär åldrande