Clear Sky Science · nl
Telomeerverkorting bij laminopathische gedilateerde cardiomyopathie
Waarom veroudering van hartcellen ertoe doet
Veel mensen met erfelijke hartspieraandoeningen ontwikkelen op relatief jonge leeftijd ernstige problemen zoals hartritmestoornissen, hartfalen en de noodzaak van transplantatie. Deze studie stelt een eenvoudige maar belangrijke vraag: verouderen de hartcellen van deze patiënten sneller op het meest fundamentele DNA-niveau? Door nauwkeurig te kijken naar kleine structuren die telomeren worden genoemd — beschermende doppen op chromosomen — onderzoeken de onderzoekers hoe een fout in een belangrijk skeleteiwit van de kern van de cel het verslijten van cellen in het hart kan versnellen.
Beschermende doppen aan het einde van ons DNA
Elk chromosoom in onze cellen eindigt in een reeks herhaalde DNA-sequenties die functioneren als het plastic uiteinde van een veter en voorkomen dat deze rafelt. Deze telomeren worden normaal gesproken geleidelijk korter naarmate we ouder worden, en zeer korte telomeren worden gezien als een kenmerk van cellulaire veroudering. In het hart stoppen de meeste spiercellen kort na de geboorte met delen, dus wordt verwacht dat hun telomeerlengte redelijk stabiel blijft. Eerder werk van deze groep toonde aan dat bepaalde erfelijke hartaandoeningen deze regel doorbreken, waarbij telomeren onverwacht kort worden. Hier ligt de focus op een familie van zeldzame aandoeningen genaamd laminopathieën, veroorzaakt door mutaties in het LMNA-gen, dat de interne schaal van de celkern vormt en helpt de vorm en stijfheid te behouden.
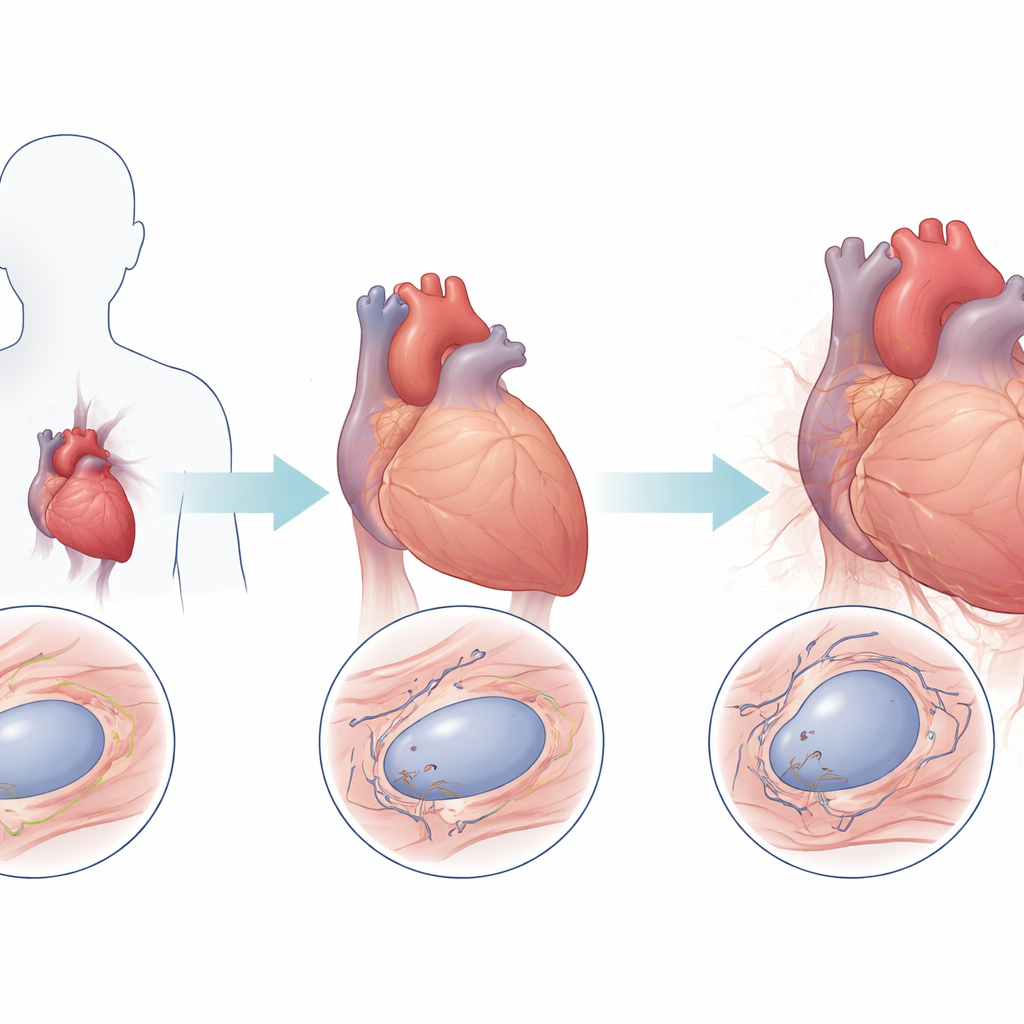
Hartweefsel dat ouder lijkt dan het zou moeten
Het team onderzocht eerst hartbiopsieën van patiënten met verschillende vormen van laminopathie die een harttransplantatie hadden ondergaan en vergeleek deze met harten van mensen zonder hartziekte. Met een fluorescentietechniek die telomeersignalen in individuele kernen van hartspiercellen meet, vonden ze dat laminopathie-harten gemiddeld 38 procent lagere telomeerniveaus hadden dan controles. Dit patroon trad op in verschillende klinische subtypes, en patiënten met één vorm van de ziekte, LGMD1B genoemd, vertoonden bijzonder snelle telomeerverlies met de leeftijd. Daarentegen bleven telomeerniveaus in gezonde harten opmerkelijk stabiel in de tijd, wat het idee versterkt dat LMNA-mutaties een abnormale versnelling van telomeerverkorting in hartcellen veroorzaken.
Zieke hartcellen nabootsen in het laboratorium
Om oorzaak en gevolg te onderzoeken, maakten de onderzoekers geïnduceerde pluripotente stamcellen van een patiënt met een frameshiftmutatie in LMNA en gebruikten vervolgens genetische bewerkingstools om vergelijkbare cellijnen te genereren met twee normale kopieën, één gemuteerde kopie of geen functionele kopieën van LMNA. In de stamceltoestand leidde het terugplaatsen van een normale LMNA-kopie tot langere telomeren, terwijl het volledige verlies van LMNA slechts bescheiden telomeerverbeteringen gaf, wat wijst op een kwetsbare balans tussen kernstructuur en telomeeronderhoud. Wanneer deze stamcellen werden omgezet in kloppende hartcellen in het laboratorium, veranderde het beeld: lijnen met weinig of geen normale LMNA vertoonden uitgesproken telomeerverlies, wat de gedachte ondersteunt dat de mechanische stress van herhaalde contractie de kernintegriteit bijzonder belangrijk maakt voor het behoud van telomeren in hartspiercellen.
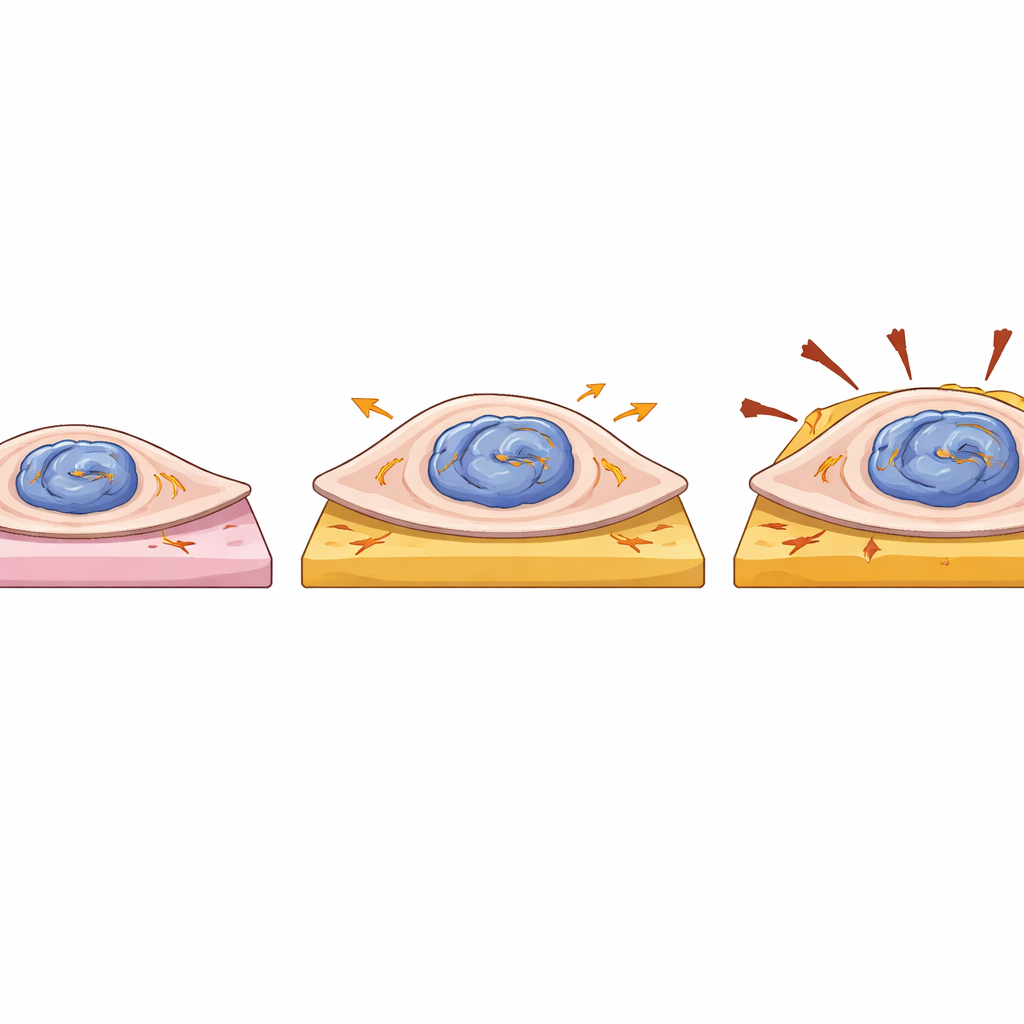
Krachtiger maar fragielere hartcellen
Het team onderzocht ook hoe de mutatie het fysieke gedrag van individuele hartcellen beïnvloedt. Ze plaatsten individuele patiënt-afgeleide en gecorrigeerde cellen op kleine, zachte of stijve gelpads die gezond respectievelijk beschadigd hartweefsel nabootsen, en maten hoe hard elke cel trok tijdens contractie. Cellen met één gemuteerde LMNA-kopie waren groter in oppervlakte en leverden meer totale kracht en rekenergie dan hun gecorrigeerde tegenhangers, vooral op zachtere gels. Deze toegenomen kracht ging echter niet gepaard met snellere contractie, en deze cellen vertoonden subtiele onregelmatigheden in de slaafrequentie, wat wijst op verstoorde interne signalering. Omdat de gemiddelde verplaatsing van het oppervlak van de gel vergelijkbaar was tussen de groepen, lijkt de extra kracht voornamelijk voort te komen uit toegenomen cellulaire omvang, niet uit efficiëntere machinerie. Samen met vervorming van de kern suggereert dit dat gemuteerd LMNA hartcellen omvangrijker en mechanisch gevoeliger maakt, terwijl tegelijkertijd hun telomeerbescherming wordt aangetast.
Bewijs uit een gehumaniseerd muismodel
Om te bekijken of deze bevindingen in een compleet organisme gelden, gebruikten de onderzoekers muizen die waren aangepast om een menselijke LMNA-mutatie te dragen die progerine produceert, het veranderde eiwit dat verantwoordelijk is voor een voortijdig verouderingssyndroom. Deze muizen ontwikkelden vroege tekenen van gedilateerde cardiomyopathie met verminderde pompfunctie. Hun hartspiercellen hadden ook significant kortere telomeren en vertoonden verminderde verkorting tijdens elke hartslag, wat wijst op verminderde contractiele functie. Deze dierresultaten weerspiegelen de gegevens uit menselijk weefsel en cellulaire kweek en versterken de koppeling tussen LMNA-mutatie, telomeerverlies en falend hartweefsel.
Wat dit betekent voor toekomstige zorg
Simpele gezegd laat dit werk zien dat bepaalde erfelijke defecten in het skelet van de celkern hartspiercellen zowel zwaarder kunnen laten werken als sneller kunnen laten verouderen, zoals blijkt uit het verlies van hun chromosoomuiteinden. De mate van telomeerverkorting varieert met de specifieke LMNA-mutatie en het celtype, wat kan helpen verklaren waarom patiënten met vergelijkbare genetische veranderingen verschillende ziektebeelden hebben. Door aan te tonen dat telomeererosie een consistent kenmerk is van laminopathie-gerelateerde hartziekte, wijst de studie op telomeerbescherming en kernondersteuning als potentiële nieuwe doelen voor therapieën die gericht zijn op het vertragen of voorkomen van hartfalen bij deze patiënten.
Bronvermelding: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Trefwoorden: laminopathie, telomeren, gedilateerde cardiomyopathie, hartspiercellen, cellulair verouderen