Clear Sky Science · it
Accorciamento dei telomeri nella cardiomiopatia dilatativa laminopatica
Perché l’invecchiamento delle cellule cardiache conta
Molte persone con malattie ereditarie del muscolo cardiaco sviluppano problemi gravi come aritmie, insufficienza cardiaca e la necessità di trapianto a età relativamente giovani. Questo studio pone una domanda semplice ma cruciale: le cellule cardiache di questi pazienti invecchiano più velocemente al livello più fondamentale del loro DNA? Osservando da vicino piccole strutture chiamate telomeri — cappucci protettivi sui cromosomi — i ricercatori esplorano come un difetto in una proteina fondamentale della struttura del nucleo cellulare possa accelerare l’usura cellulare nel cuore.
Cappucci protettivi alle estremità del nostro DNA
Ogni cromosoma nelle nostre cellule termina con una porzione di DNA ripetuto che funziona come la punta plastica di un laccio, impedendo lo sfilacciamento. Questi telomeri si accorciano normalmente in modo lento con l’età, e telomeri molto corti sono considerati un segno distintivo dell’invecchiamento cellulare. Nel cuore, la maggior parte delle cellule muscolari cessa di dividersi poco dopo la nascita, quindi la lunghezza dei loro telomeri dovrebbe rimanere relativamente stabile. Lavori precedenti del gruppo avevano mostrato che alcune malattie genetiche cardiache infrangono questa regola, con telomeri diventati inaspettatamente corti. Qui l’attenzione è su una famiglia di disturbi rari chiamati laminopatie, causati da mutazioni nel gene LMNA, che costruisce l’involucro interno del nucleo e contribuisce a mantenere la sua forma e rigidità.
Tessuto cardiaco che appare più vecchio del dovuto
Il team ha prima esaminato campioni bioptici di cuore di pazienti con diverse forme di laminopatia sottoposti a trapianto cardiaco, confrontandoli con cuori di persone senza malattie cardiache. Utilizzando una tecnica fluorescente che misura i segnali dei telomeri nei singoli nuclei delle cellule muscolari cardiache, hanno rilevato che i cuori laminopatici avevano in media livelli di telomeri inferiori del 38 percento rispetto ai controlli. Questo schema si è mantenuto attraverso diversi sottotipi clinici, e i pazienti con una forma della malattia chiamata LGMD1B hanno mostrato una perdita di telomeri particolarmente rapida con l’età. Al contrario, nei cuori sani i livelli di telomeri risultavano sorprendentemente stabili nel tempo, rafforzando l’idea che le mutazioni LMNA promuovano un’accelerazione anomala dell’accorciamento dei telomeri nelle cellule cardiache.
Modellare le cellule cardiache malate in coltura
Per sondare causa ed effetto, i ricercatori hanno creato cellule staminali pluripotenti indotte da un paziente portatore di una mutazione frameshift in LMNA, poi hanno usato strumenti di editing genetico per ottenere linee cellulari abbinate con due copie normali, una copia mutata o nessuna copia funzionale di LMNA. Nello stato di cellule staminali, reintrodurre una copia normale di LMNA aumentava la lunghezza dei telomeri, mentre la perdita completa di LMNA produceva solo modesti guadagni di telomeri, evidenziando un equilibrio delicato tra struttura nucleare e mantenimento dei telomeri. Quando queste staminali sono state trasformate in cellule cardiache battenti in laboratorio, il quadro è cambiato: le linee con poca o nessuna LMNA normale mostravano una marcata perdita di telomeri, a sostegno dell’idea che lo stress meccanico delle contrazioni ripetute renda l’integrità nucleare particolarmente importante per preservare i telomeri nelle cellule del muscolo cardiaco.
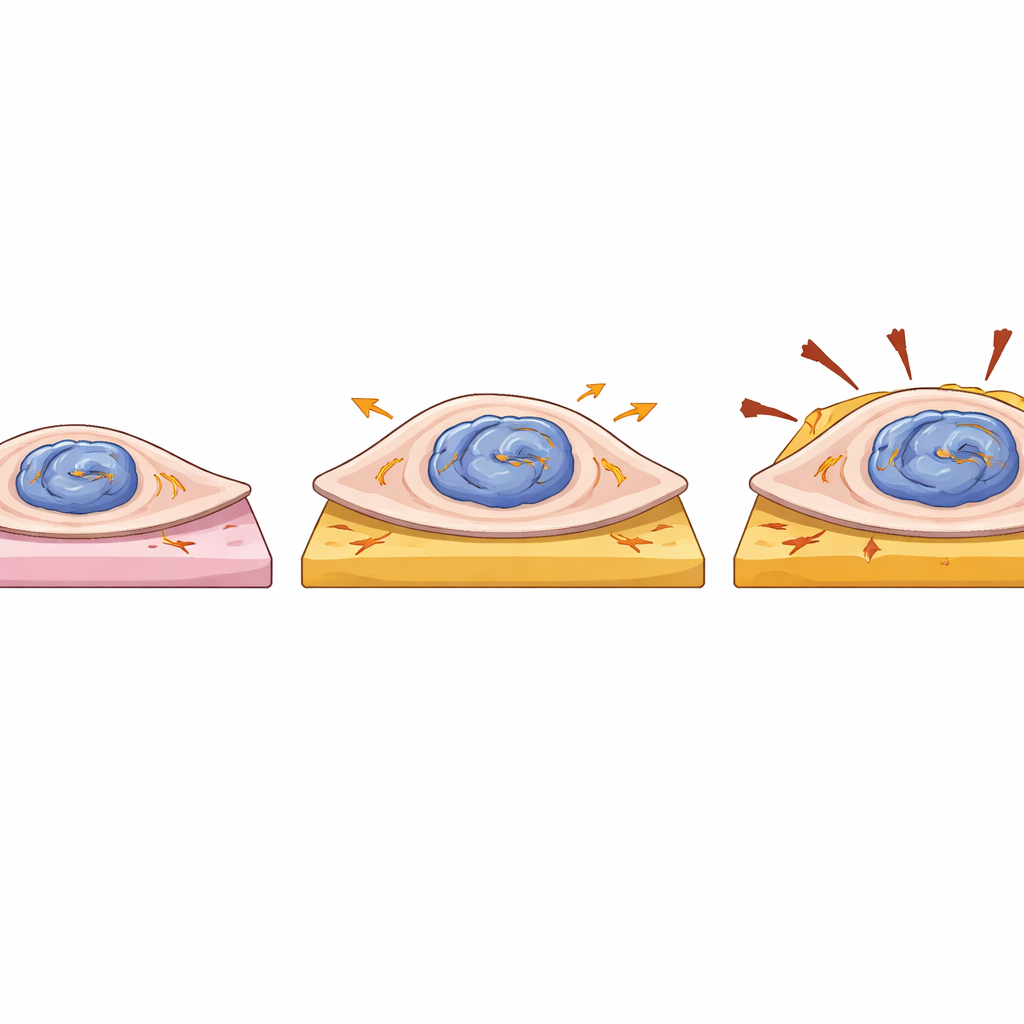
Cellule cardiache più forti ma più fragili
Il gruppo ha anche indagato come la mutazione influisca sul comportamento fisico delle singole cellule cardiache. Hanno posizionato cellule derivate dal paziente e cellule corrette su piccoli cuscinetti di gel morbidi o rigidi che imitano tessuto cardiaco sano o cicatriziale, e hanno misurato quanto ogni cellula tirasse durante la contrazione. Le cellule con una copia mutante di LMNA avevano un’area maggiore e generavano una forza complessiva e un’energia di deformazione superiori rispetto alle controparti corrette, in particolare sui gel più morbidi. Tuttavia, questa forza aumentata non si accompagnava a contrazioni più rapide, e queste cellule mostravano lievi irregolarità nella frequenza del battito, suggerendo segnali interni disturbati. Poiché lo spostamento medio della superficie del gel era simile tra i gruppi, la forza extra sembra derivare principalmente dall’aumento delle dimensioni cellulari, non da una macchina contrattile più efficiente. Insieme alla deformazione del nucleo, ciò suggerisce che la LMNA mutata renda le cellule cardiache più ingombranti e meccanicamente sensibili, pur erodendo la protezione dei loro telomeri.
Prove da un modello murino umanizzato
Per verificare se questi risultati si mantengono in un organismo intero, i ricercatori hanno utilizzato topi ingegnerizzati per portare una mutazione umana di LMNA che produce progerina, la proteina alterata responsabile di una sindrome da invecchiamento precoce. Questi topi hanno sviluppato segni precoci di cardiomiopatia dilatativa, con prestazioni di pompaggio ridotte. Le loro cellule del muscolo cardiaco presentavano inoltre telomeri significativamente più corti e mostravano una ridotta accorciamento durante ogni battito, indicando una funzione contrattile compromessa. Questi risultati animali rispecchiano i dati umani e di colture cellulari, rafforzando il legame tra mutazione di LMNA, perdita di telomeri e deterioramento del muscolo cardiaco.
Cosa significa per la cura futura
In termini chiari, questo lavoro mostra che alcuni difetti ereditari nell’impalcatura del nucleo cellulare possono rendere le cellule del muscolo cardiaco sia più sollecitate che più rapide nell’invecchiamento, come evidenziato dalla perdita dei loro cappucci cromosomici. Il grado di accorciamento dei telomeri varia a seconda della specifica mutazione LMNA e del tipo cellulare, il che può aiutare a spiegare perché pazienti con cambiamenti genetici simili presentino gravità della malattia diversa. Stabilendo che l’erosione dei telomeri è una caratteristica costante della malattia cardiaca legata alle laminopatie, lo studio indica la protezione dei telomeri e il supporto nucleare come possibili nuovi bersagli terapeutici per rallentare o prevenire l’insufficienza cardiaca in questi pazienti.
Citazione: Chang, A.C.Y., Pardon, G., Chang, A.C.H. et al. Telomere shortening in laminopathic dilated cardiomyopathy. npj Regen Med 11, 16 (2026). https://doi.org/10.1038/s41536-026-00462-1
Parole chiave: laminopatia, telomeri, cardiomiopatia dilatativa, cellule del muscolo cardiaco, invecchiamento cellulare