Clear Sky Science · zh
抗病毒固有免疫在神经元中诱导α-突触核蛋白在丝氨酸129位的磷酸化,与聚集无关
为何病毒与帕金森病可能有关联
许多从严重病毒感染中康复的人随后会出现记忆、运动或情绪方面的问题。与此同时,诸如帕金森病等脑部疾病的特征是在神经细胞内出现一种称为α-突触核蛋白的异常团块。本研究针对患者和家庭提出了一个紧迫的问题:当大脑抵御病毒时,这种免疫反应是否会推动α-突触核蛋白发生那类可能在多年后为帕金森样疾病奠定基础的改变?
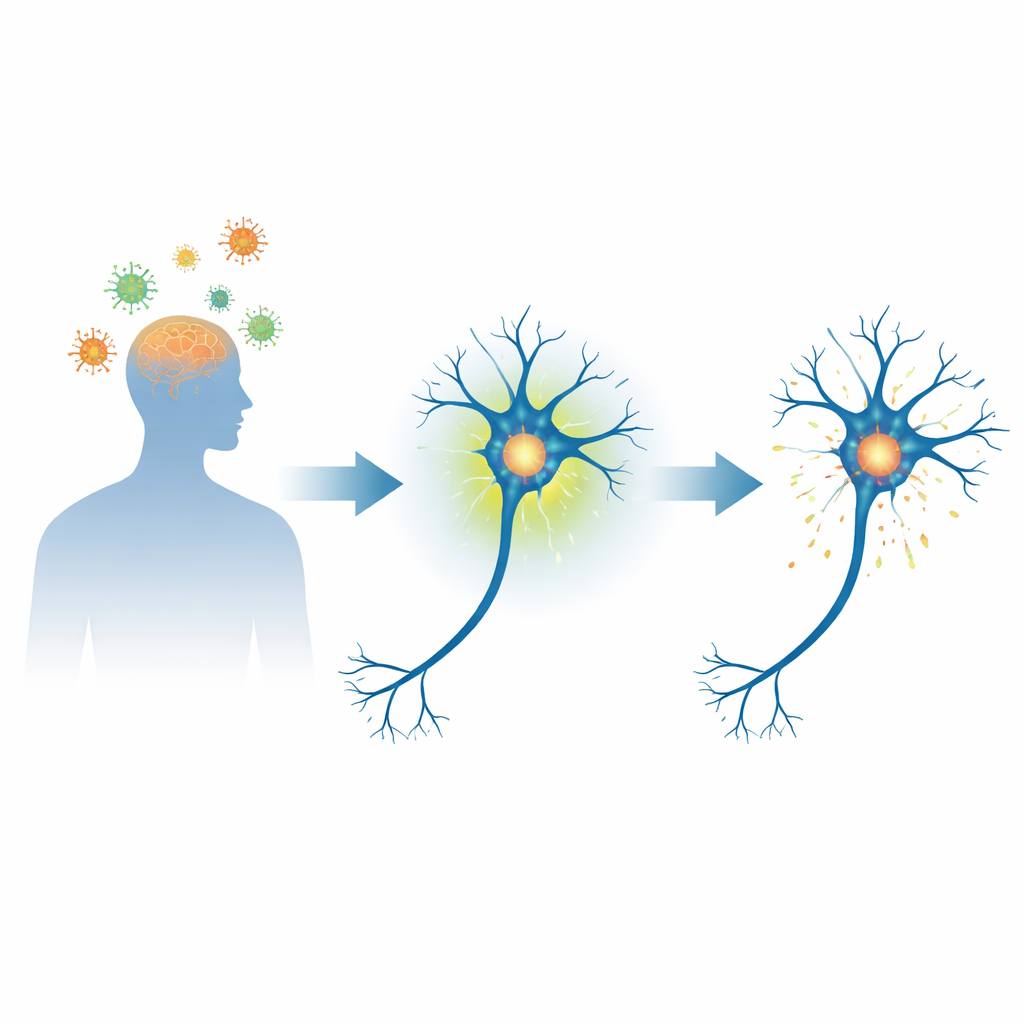
位于脑病中心的神经细胞蛋白
α-突触核蛋白是一种小而灵活的蛋白,广泛存在于神经细胞中,参与调节细胞间信号的传递。在帕金森病及相关疾病中,该蛋白可能错误折叠并堆积成被称为路易体的致密沉积物,这与神经细胞的死亡密切相关。该蛋白上的一个关键化学标签——位于特定位点的磷酸化(丝氨酸129)——在这些沉积物中的大部分α-突触核蛋白上都能检测到。这促使科学家思考,这一标签是单纯的损伤标志,还是通向疾病的早期步骤。
来自患脑部感染的人与动物的线索
研究人员首先检查了死于严重西尼罗病毒脑部感染的人的脑组织。与对照脑相比,感染脑在神经元内显示出更多携带丝氨酸129磷酸化标签的α-突触核蛋白,尤其在与运动相关的重要区域,这些相同的细胞还显示出活跃的抗病毒信号。为了检验因果关系,研究团队随后建立了一个小鼠模型,在该模型中西尼罗病毒沿嗅觉通路从鼻子进入大脑。随着病毒的传播,动物体重下降,启动了强烈的抗病毒基因表达,且——关键在于——在嗅球中出现了标记的α-突触核蛋白激增,尽管该蛋白尚未形成不溶性团块。
病毒触发但无持久团块
为了观察这是否为一种普遍反应,科学家们研究了其他病毒。一种在猴子中引起带状疱疹样疾病的DNA病毒,以及小鼠中的单纯疱疹病毒,也都在服务皮肤和面部的神经团簇中提升了被标记的α-突触核蛋白。在培养的鼠脑细胞中,西尼罗病毒感染在数小时内迅速提高了被标记的α-突触核蛋白水平,但这些水平随后回落,灵敏检测未发现新的聚集体。即使用合成分子模拟病毒的遗传物质,而不使用真实病毒,也足以在神经元中暂时增加被标记的蛋白形式,仍然没有形成团块。
干扰素:开启这种标签的信使
将所有这些观察联系起来的是大脑的前线警报系统:I型干扰素,这是一类当神经细胞感知到病毒遗传物质时释放的蛋白。在培养的神经元中,真实感染与病毒模拟物都促使细胞分泌这类干扰素,而单独用干扰素处理也在30分钟内迅速使被标记的α-突触核蛋白水平翻倍。此类峰值短暂出现,且仍未伴随聚集体。值得注意的是,当团队在缺失干扰素受体基因的神经元中重复实验时,病毒和RNA模拟物都无法提高被标记的α-突触核蛋白。这表明该化学标签是在干扰素信号下游被添加的,而非由病毒直接造成。
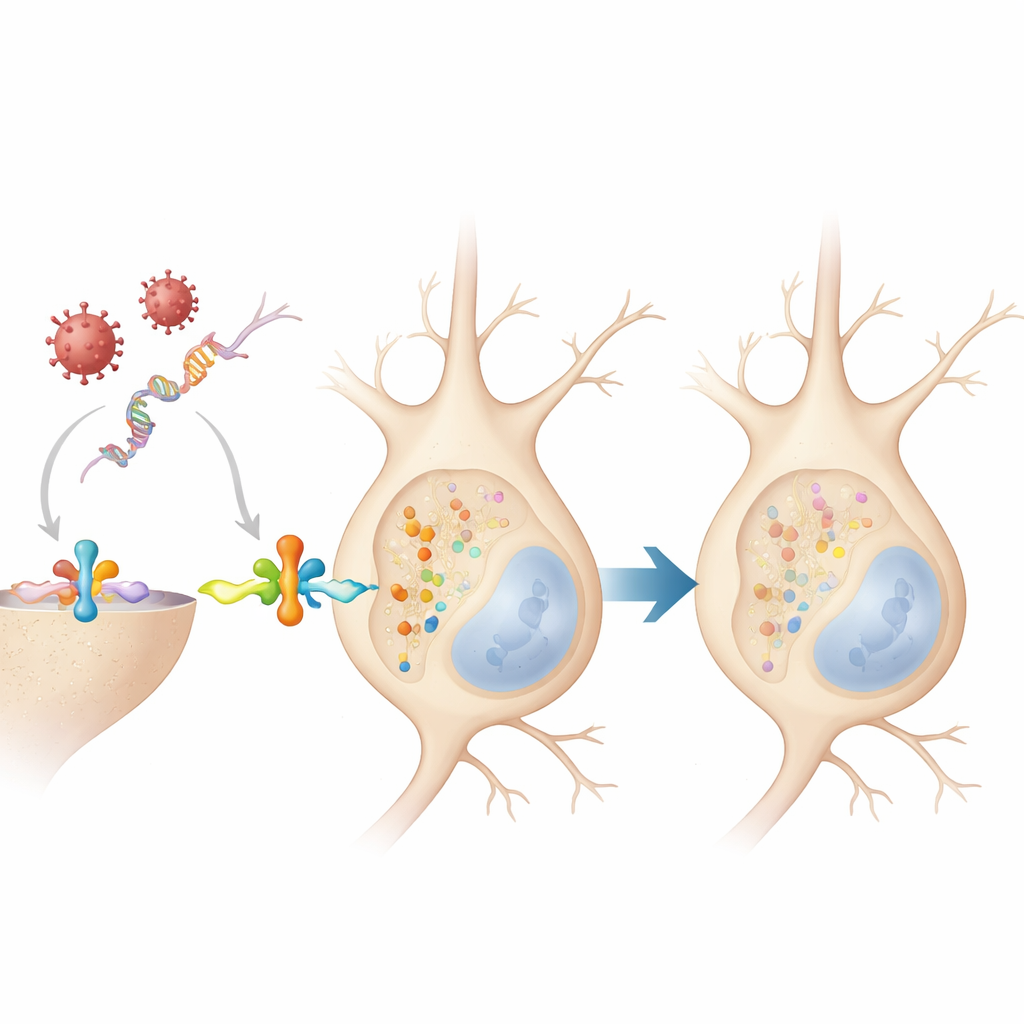
这对长期脑健康的意义
综合来看,这项工作表明,当神经元发动抗病毒防御时,会短暂性地修饰α-突触核蛋白,这种修饰通常是可逆的,并不会立即产生有毒的团块。然而,由于这种反应在不同物种和多种病毒中都能观察到,重复感染或终生慢性炎症可能会反复触发这一分子开关。如果随着年龄增长,通常负责清除被标记α-突触核蛋白的系统变得不堪重负或失效,这些无害且短暂的变化可能开始累积,推动该蛋白朝向帕金森病及相关疾病中观察到的聚集体发展。在这种观点下,α-突触核蛋白的标记不仅仅是损伤的标志,而是大脑对感染的早期反应——在不利条件下,这一反应可能会从保护性逐渐转为有害。
引用: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
关键词: 帕金森病, α-突触核蛋白, 病毒感染, 干扰素, 神经炎症