Clear Sky Science · it
L’immunità innata antivirale induce la fosforilazione della alfa-sinucleina in serina129 nei neuroni indipendentemente dall’aggregazione
Perché virus e Parkinson potrebbero essere collegati
Molte persone che si riprendono da infezioni virali gravi sviluppano in seguito problemi di memoria, movimento o umore. Allo stesso tempo, le malattie cerebrali come il Parkinson sono caratterizzate da ammassi anomali di una proteina chiamata alfa-sinucleina all’interno dei neuroni. Questo studio pone una domanda urgente per pazienti e famiglie: quando il cervello combatte un virus, quella stessa risposta immunitaria spinge l’alfa-sinucleina verso cambiamenti che, nel corso degli anni, possono predisporre a disturbi simili al Parkinson?
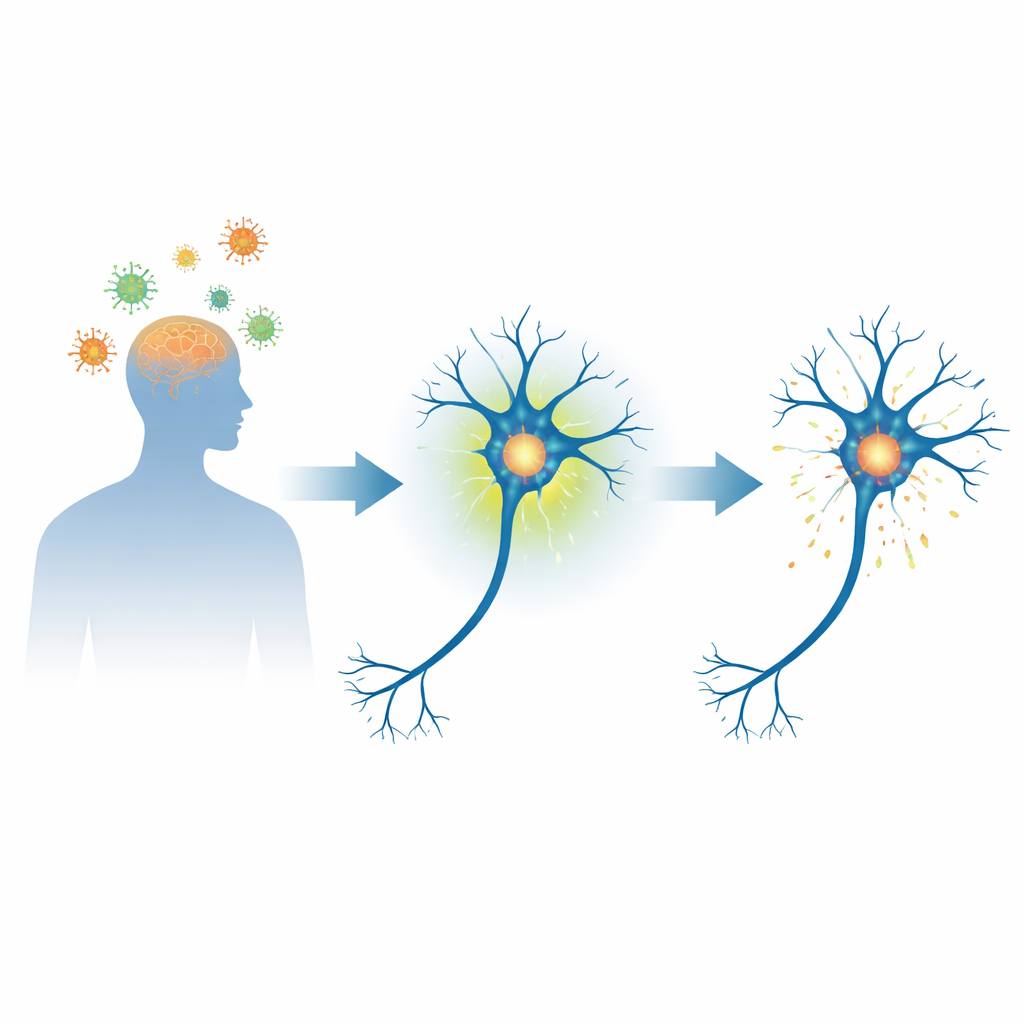
Una proteina neuronale al centro delle malattie cerebrali
L’alfa-sinucleina è una piccola proteina flessibile, abbondante nei neuroni, che contribuisce a regolare il passaggio dei segnali tra le cellule nervose. Nella malattia di Parkinson e in condizioni correlate, questa proteina può malripiegarsi e accumularsi in depositi densi noti come corpi di Lewy, strettamente associati alla morte neuronale. Un marcatore chimico chiave su questa proteina, la fosforilazione in uno specifico sito (serina 129), è presente nella maggior parte dell’alfa-sinucleina all’interno di questi depositi. Ciò ha spinto gli scienziati a chiedersi se questo marchio sia solo un indicatore di danno o un passo iniziale verso la malattia.
Indizi da persone e animali con infezioni cerebrali
I ricercatori hanno prima esaminato tessuto cerebrale di persone decedute per una grave infezione cerebrale da virus West Nile. Rispetto ai cervelli di controllo, quelli infetti mostravano più alfa-sinucleina con la fosforilazione in serina-129 all’interno dei neuroni, specialmente nelle aree importanti per il movimento, e le stesse cellule presentavano segnali di attivazione antivirale. Per testare causa ed effetto, il gruppo ha quindi sviluppato un modello murino in cui il virus West Nile viaggia dal naso al cervello lungo le vie olfattive. Con la diffusione del virus, gli animali perdevano peso, attivavano forti geni antivirali e — elemento cruciale — mostravo un’ondata di alfa-sinucleina fosforilata nei bulbi olfattivi, nonostante la proteina non avesse ancora formato aggregati insolubili.
Scatenanti virali senza aggregati persistenti
Per verificare se si trattasse di una risposta generale, gli scienziati hanno osservato altri virus. Un virus a DNA che provoca una malattia simile al fuoco di Sant’Antonio nelle scimmie, e l’herpes simplex nei topi, aumentavano anch’essi l’alfa-sinucleina fosforilata nei gruppi neuronali che servono la pelle e il volto. In colture di cellule cerebrali murine, l’infezione da West Nile innalzava rapidamente i livelli di alfa-sinucleina fosforilata in poche ore, ma questi livelli poi ricadevano e test sensibili non rilevavano nuovi aggregati. Anche l’imitazione del materiale genetico virale con una molecola sintetica, senza usare il virus reale, era sufficiente ad aumentare temporaneamente la forma fosforilata della proteina nei neuroni, di nuovo senza generare ammassi.
Interferone: il messaggero che attiva il marchio
Ciò che collegava tutte queste osservazioni era il sistema d’allarme in prima linea del cervello: l’interferone di tipo I, una famiglia di proteine che i neuroni rilasciano quando percepiscono materiale genetico virale. Nei neuroni in coltura, sia l’infezione vera sia il mimetico virale inducevano le cellule a secernere questo tipo di interferone, e il trattamento diretto con interferone da solo raddoppiava rapidamente i livelli di alfa-sinucleina fosforilata entro 30 minuti. Questo picco era di breve durata e non era accompagnato da aggregati. Notevolmente, quando il gruppo ripeté gli esperimenti in neuroni privi geneticamente del recettore per l’interferone, né il virus né il mimetico RNA riuscivano ad aumentare l’alfa-sinucleina fosforilata. Ciò dimostra che il marchio chimico viene aggiunto a valle della segnalazione dell’interferone, non direttamente dal virus.
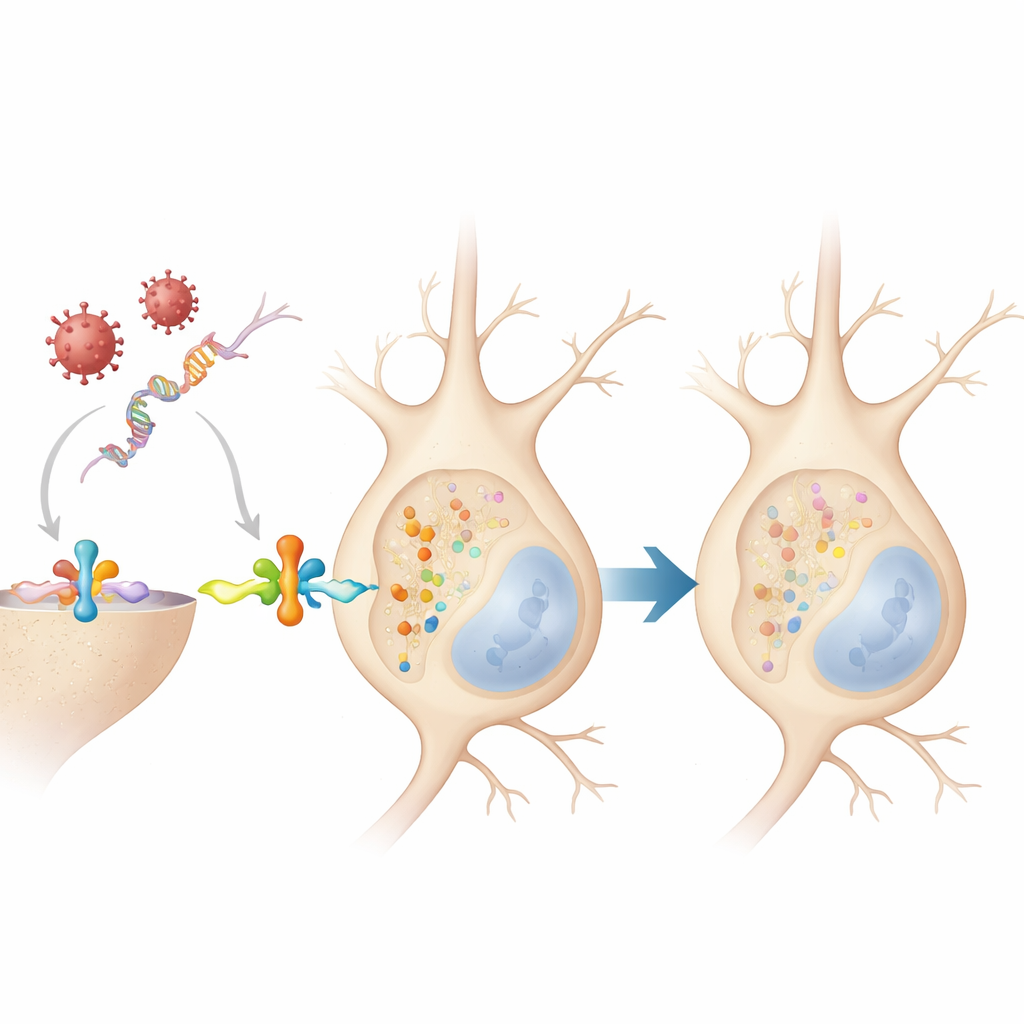
Cosa significa per la salute cerebrale a lungo termine
Nel complesso, il lavoro suggerisce che quando i neuroni attivano una difesa antivirale, modificano brevemente l’alfa-sinucleina in modo normalmente reversibile e che non crea immediatamente aggregati tossici. Tuttavia, poiché questa risposta appare in più specie e con virus diversi, infezioni ripetute o infiammazione cronica nel corso della vita potrebbero attivare ripetutamente questo interruttore molecolare. Se i sistemi che normalmente eliminano l’alfa-sinucleina fosforilata si sovraccaricano o falliscono con l’età, questi cambiamenti innocui e transitori potrebbero accumularsi, spingendo la proteina verso gli aggregati osservati nel Parkinson e in malattie correlate. In questa prospettiva, la fosforilazione dell’alfa-sinucleina non è solo un segno di danno ma parte della risposta precoce del cervello all’infezione — una risposta che, in condizioni sfavorevoli, può gradualmente passare da protettiva a dannosa.
Citazione: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Parole chiave: Morbo di Parkinson, alfa-sinucleina, infezione virale, interferone, neuroinfiammazione