Clear Sky Science · nl
Antivirale aangeboren immuniteit veroorzaakt fosforylering van alfa‑synucleïne op serine129 in neuronen onafhankelijk van aggregatie
Waarom virussen en Parkinson met elkaar verbonden zouden kunnen zijn
Veel mensen die herstellen van ernstige virusinfecties ontwikkelen later problemen met geheugen, beweging of stemming. Tegelijkertijd worden hersenaandoeningen zoals de ziekte van Parkinson gekenmerkt door abnormale ophopingen van een eiwit dat alfa‑synucleïne heet in zenuwcellen. Deze studie behandelt een prangende vraag voor patiënten en families: wanneer de hersenen een virus bestrijden, duwt die immuunreactie alfa‑synucleïne dan richting veranderingen die, over jaren, de weg kunnen banen naar Parkinson‑achtige stoornissen?
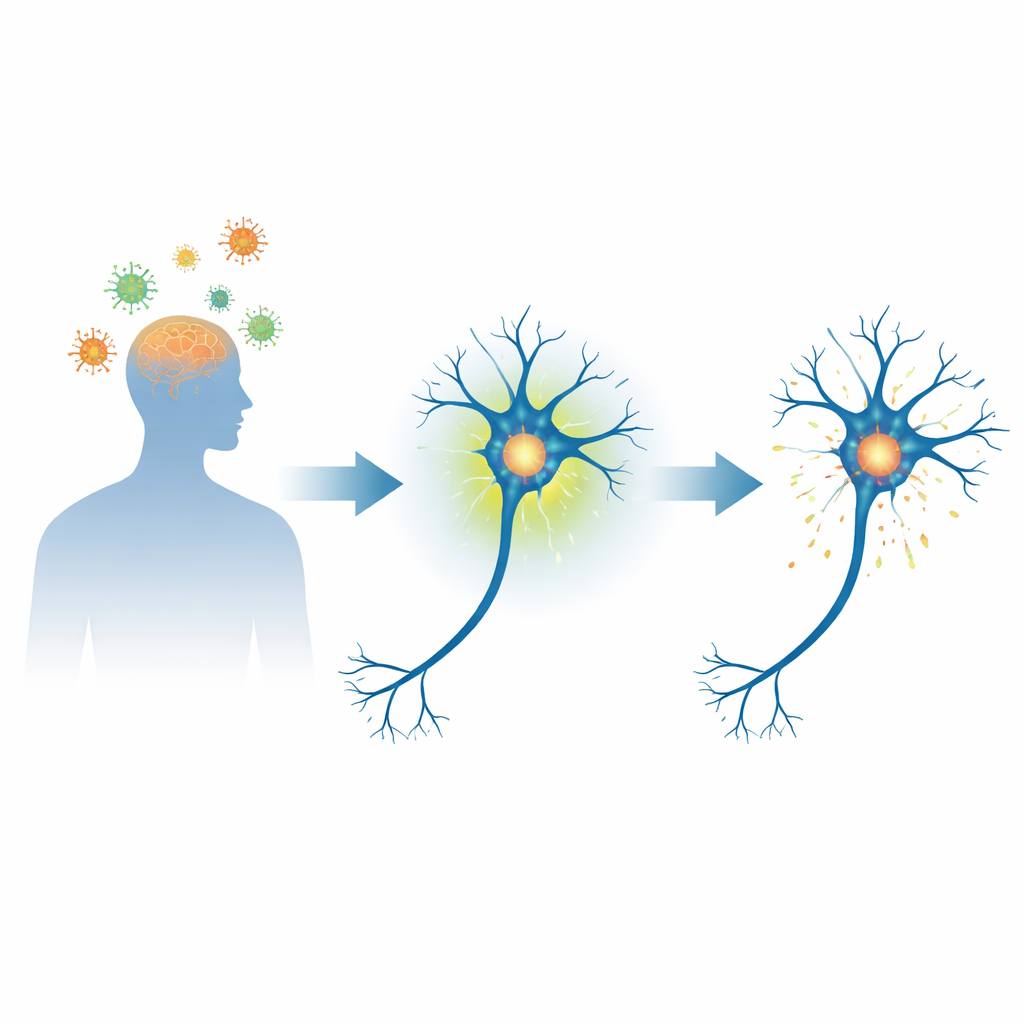
Een zenuwceleiwit centraal in hersenziekte
Alfa‑synucleïne is een klein, flexibel eiwit dat in overvloed aanwezig is in zenuwcellen en helpt reguleren hoe signalen tussen die cellen worden doorgegeven. Bij de ziekte van Parkinson en aanverwante aandoeningen kan dit eiwit verkeerd vouwen en zich ophopen in dichte afzettingen die Lewy‑lichaampjes worden genoemd, en die nauw zijn verbonden met het afsterven van zenuwcellen. Een belangrijk chemisch merkteken op dit eiwit, fosforylering op een specifieke plek (serine 129), wordt aangetroffen op het merendeel van het alfa‑synucleïne in deze afzettingen. Dat heeft wetenschappers doen afvragen of dit merkteken louter een schade‑indicator is of een vroege stap op weg naar ziekte.
Aanwijzingen van mensen en dieren met herseninfecties
De onderzoekers bestudeerden eerst hersenweefsel van mensen die waren overleden aan een ernstige West‑Nijlvirus‑infectie van de hersenen. Vergeleken met controlehersenen vertoonden de geïnfecteerde hersenen meer alfa‑synucleïne met het serine‑129‑merkteken binnen neuronen, vooral in gebieden die belangrijk zijn voor beweging, en diezelfde cellen toonden tekenen van actieve antivirale signalering. Om oorzaak en gevolg te testen ontwikkelde het team vervolgens een muismodel waarin het West‑Nijlvirus vanuit de neus via de reukbanen de hersenen binnenkomt. Terwijl het virus zich verspreidde, verloren de dieren gewicht, zetten ze krachtige antivirale genen aan en—cruciaal—toonden ze een piek van gemerkt alfa‑synucleïne in de reukbollen, hoewel het eiwit nog geen onoplosbare klonten had gevormd.
Virale triggers zonder blijvende klonten
Om te onderzoeken of dit een algemene reactie is, keken de wetenschappers naar andere virussen. Een DNA‑virus dat bij apen een gordelroosachtige ziekte veroorzaakt, en herpes simplex‑virus in muizen, verhoogden eveneens het gehalte aan gemerkt alfa‑synucleïne in zenuwknoopjes die huid en gezicht bedienen. In kweekschalen met muizenhersencellen verhoogde een West‑Nijlvirus‑infectie binnen enkele uren snel het niveau van gemerkt alfa‑synucleïne, maar deze niveaus daalden daarna weer en gevoelige tests vonden geen nieuwe aggregaten. Zelfs het nabootsen van viraal genetisch materiaal met een synthetische molecule, zonder echt virus te gebruiken, was voldoende om de gemerkte vorm van het eiwit tijdelijk in neuronen te verhogen, opnieuw zonder klonten te creëren.
Interferon: de boodschapper die het merkteken activeert
Wat al deze observaties verbond, was het frontale alarmsysteem van de hersenen: type I‑interferon, een familie van eiwitten die zenuwcellen uitscheiden wanneer zij viraal genetisch materiaal detecteren. In gekweekte neuronen veroorzaakten zowel daadwerkelijke infectie als het virale nabootsingsmiddel dat de cellen dit soort interferon uitscheiden, en directe behandeling met interferon alleen verdubbelde snel binnen 30 minuten de niveaus van gemerkt alfa‑synucleïne. Deze piek was van korte duur en ging nog steeds niet gepaard met aggregaten. Opmerkelijk genoeg, wanneer het team de experimenten herhaalde in neuronen die genetisch het interferonreceptor misten, konden noch het virus noch het RNA‑nabootsingsmiddel het gehalte aan gemerkt alfa‑synucleïne verhogen. Dat toont aan dat het chemische merkteken wordt toegevoegd stroomafwaarts van interferonsignalering, niet door het virus zelf.
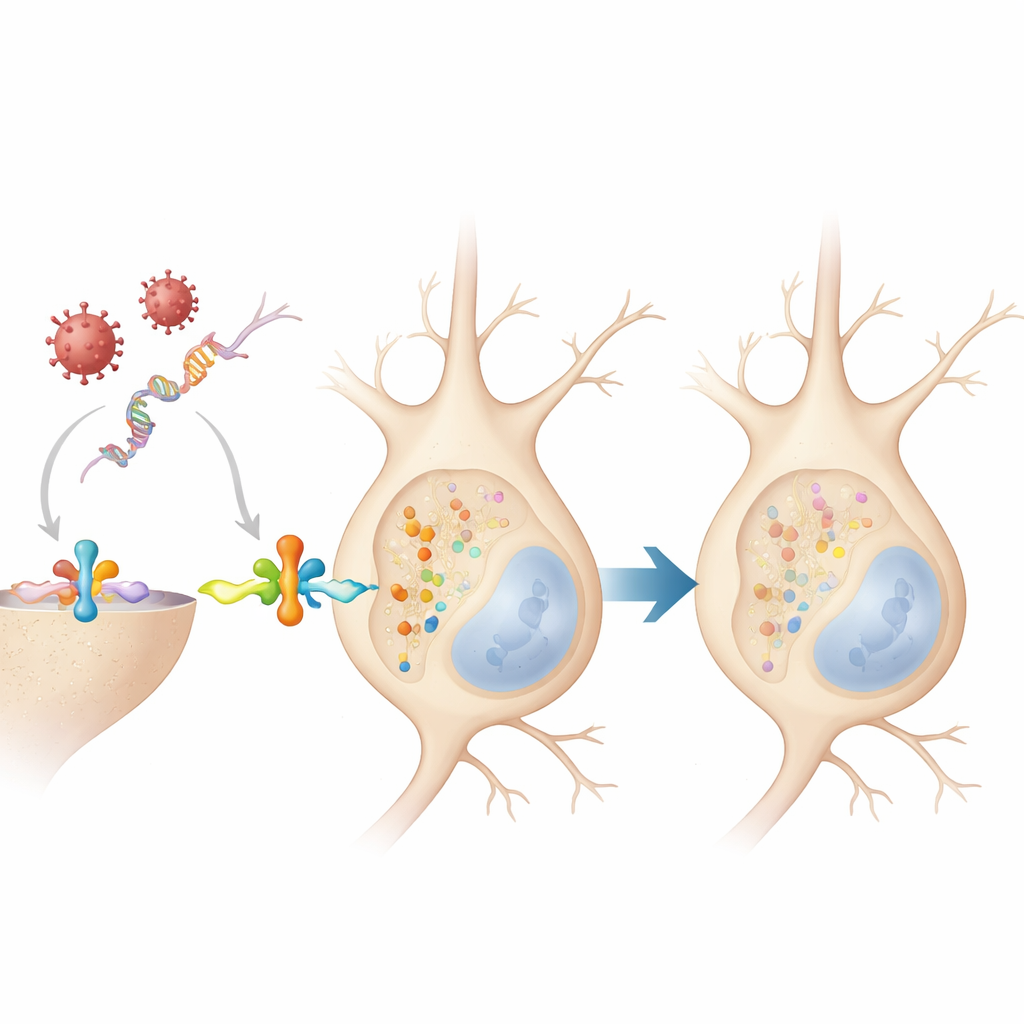
Wat dit betekent voor de langetermijngezondheid van de hersenen
Gezamenlijk suggereert het werk dat wanneer neuronen een antivirale verdediging opzetten, ze alfa‑synucleïne kortstondig zodanig wijzigen dat dit normaal omkeerbaar is en niet onmiddellijk toxische klonten creëert. Omdat deze reactie echter voorkomt bij verschillende soorten en uiteenlopende virussen, zou herhaalde infectie of chronische ontsteking gedurende een leven deze moleculaire schakel herhaaldelijk kunnen omzetten. Als de systemen die normaal gesproken gemerkt alfa‑synucleïne opruimen overbelast raken of met de leeftijd falen, zouden deze onschadelijke, vluchtige veranderingen kunnen beginnen op te hopen en het eiwit richting de aggregaten te duwen die bij Parkinson en aanverwante ziekten worden gezien. In dit licht is het taggen van alfa‑synucleïne niet slechts een teken van schade, maar onderdeel van de vroege reactie van de hersenen op infectie—een reactie die, onder ongunstige omstandigheden, geleidelijk van beschermend naar schadelijk kan omslaan.
Bronvermelding: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Trefwoorden: Ziekte van Parkinson, alfa-synucleïne, virusinfectie, interferon, neuroinflammatie