Clear Sky Science · fr
L’immunité innée antivirale induit la phosphorylation de l’alpha-synucléine en sérine129 dans les neurones indépendamment de l’agrégation
Pourquoi les virus et la maladie de Parkinson pourraient être liés
De nombreuses personnes qui se remettent d’infections virales sévères développent ensuite des troubles de la mémoire, du mouvement ou de l’humeur. Parallèlement, des maladies cérébrales comme la maladie de Parkinson se caractérisent par des amas anormaux d’une protéine appelée alpha‑synucléine à l’intérieur des cellules nerveuses. Cette étude aborde une question cruciale pour les patients et leurs familles : lorsque le cerveau lutte contre un virus, cette réponse immunitaire favorise‑t‑elle des modifications de l’alpha‑synucléine susceptibles, au fil des années, de préparer le terrain à des troubles de type Parkinson ?
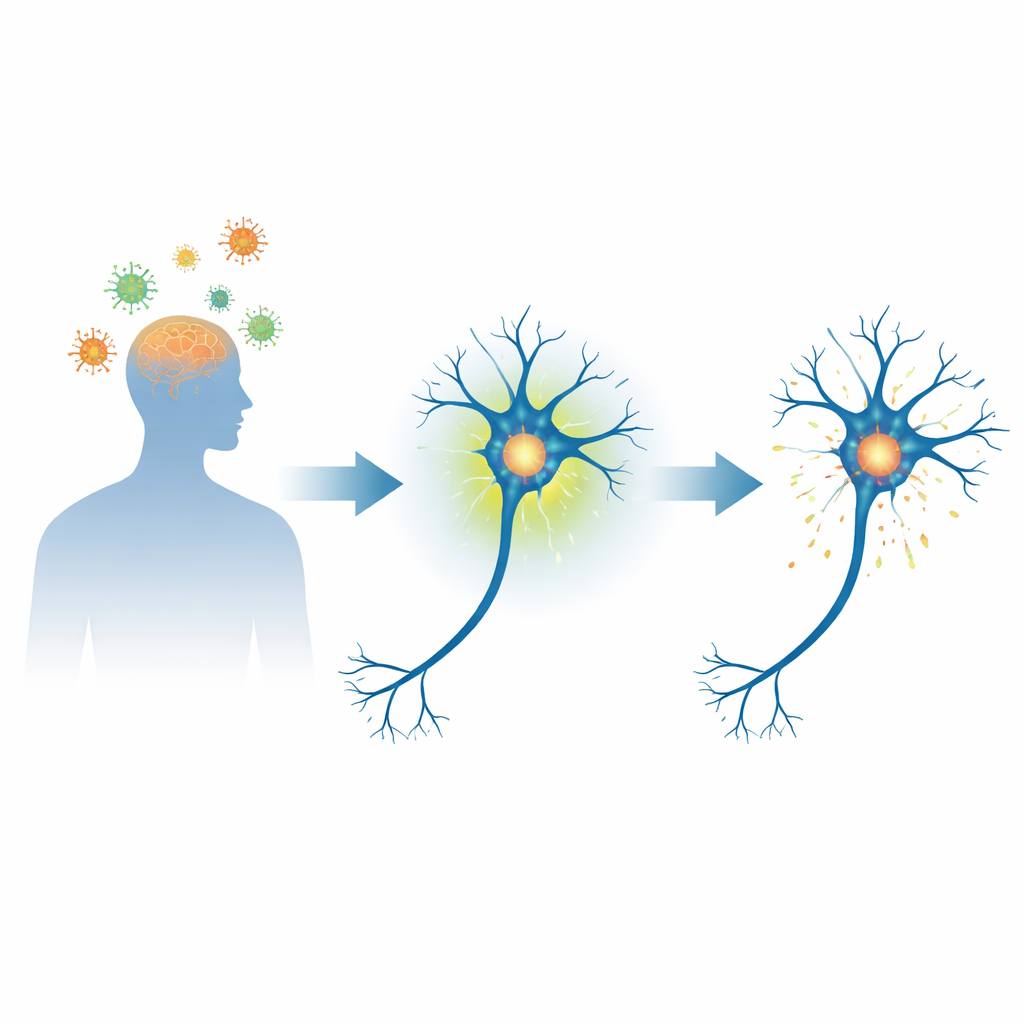
Une protéine neuronale au centre des maladies cérébrales
L’alpha‑synucléine est une petite protéine souple, abondante dans les neurones, qui contribue à réguler la transmission des signaux entre eux. Dans la maladie de Parkinson et les affections apparentées, cette protéine peut se déplier de façon anormale et s’accumuler en dépôts denses appelés corps de Lewy, étroitement associés à la mort neuronale. Un marqueur chimique clé sur cette protéine, la phosphorylation à un site spécifique (la sérine 129), se retrouve sur la plupart de l’alpha‑synucléine contenue dans ces dépôts. Cela a amené les scientifiques à se demander si ce marqueur n’est que le témoin d’un dommage ou bien une étape précoce sur la voie de la maladie.
Indices tirés d’humains et d’animaux atteints d’infections cérébrales
Les chercheurs ont d’abord examiné des tissus cérébraux de personnes décédées d’une infection cérébrale sévère à virus West Nile. Par rapport aux cerveaux témoins, les cerveaux infectés présentaient davantage d’alpha‑synucléine portant la marque sur la sérine‑129 à l’intérieur des neurones, en particulier dans des zones importantes pour le mouvement, et ces mêmes cellules montraient des signes d’activation de la signalisation antivirale. Pour tester la causalité, l’équipe a ensuite développé un modèle murin dans lequel le virus West Nile remonte du nez vers le cerveau le long des voies olfactives. À mesure que le virus se propageait, les animaux perdaient du poids, activaient de puissants gènes antiviraux et — crucialement — manifestaient une flambée d’alpha‑synucléine marquée dans les bulbes olfactifs, alors même que la protéine n’avait pas encore formé de dépôts insolubles.
Déclencheurs viraux sans agrégats durables
Pour savoir si cette réaction était générale, les scientifiques ont étudié d’autres virus. Un virus à ADN provoquant une maladie similaire au zona chez les singes, et le virus de l’herpès simplex chez la souris, augmentaient également l’alpha‑synucléine marquée dans des amas neuronaux desservant la peau et le visage. En culture de cellules cérébrales de souris, l’infection par le virus West Nile augmentait rapidement les niveaux d’alpha‑synucléine marquée en quelques heures, mais ces niveaux retombaient ensuite, et des tests sensibles n’ont détecté aucun nouvel agrégat. Mêmetr l’imitation du matériel génétique viral par une molécule synthétique, sans utiliser de virus réel, suffisait à accroître temporairement la forme marquée de la protéine dans les neurones, encore une fois sans création de dépôts.
Interféron : le messager qui active la marque
Ce qui reliait toutes ces observations, c’était le système d’alarme de première ligne du cerveau : l’interféron de type I, une famille de protéines libérées par les neurones lorsqu’ils détectent du matériel génétique viral. En neurones en culture, l’infection réelle comme l’imitateur viral faisaient sécréter ce type d’interféron, et un traitement direct avec l’interféron à lui seul doublait rapidement les niveaux d’alpha‑synucléine marquée en 30 minutes. Ce pic était de courte durée et n’était toujours pas accompagné d’agrégats. Fait marquant, lorsque l’équipe a répété les expériences sur des neurones dépourvus génétiquement du récepteur de l’interféron, ni le virus ni l’imitateur d’ARN n’ont pu élever l’alpha‑synucléine marquée. Cela montre que l’ajout de la marque a lieu en aval de la signalisation de l’interféron, et non pas directement par le virus.
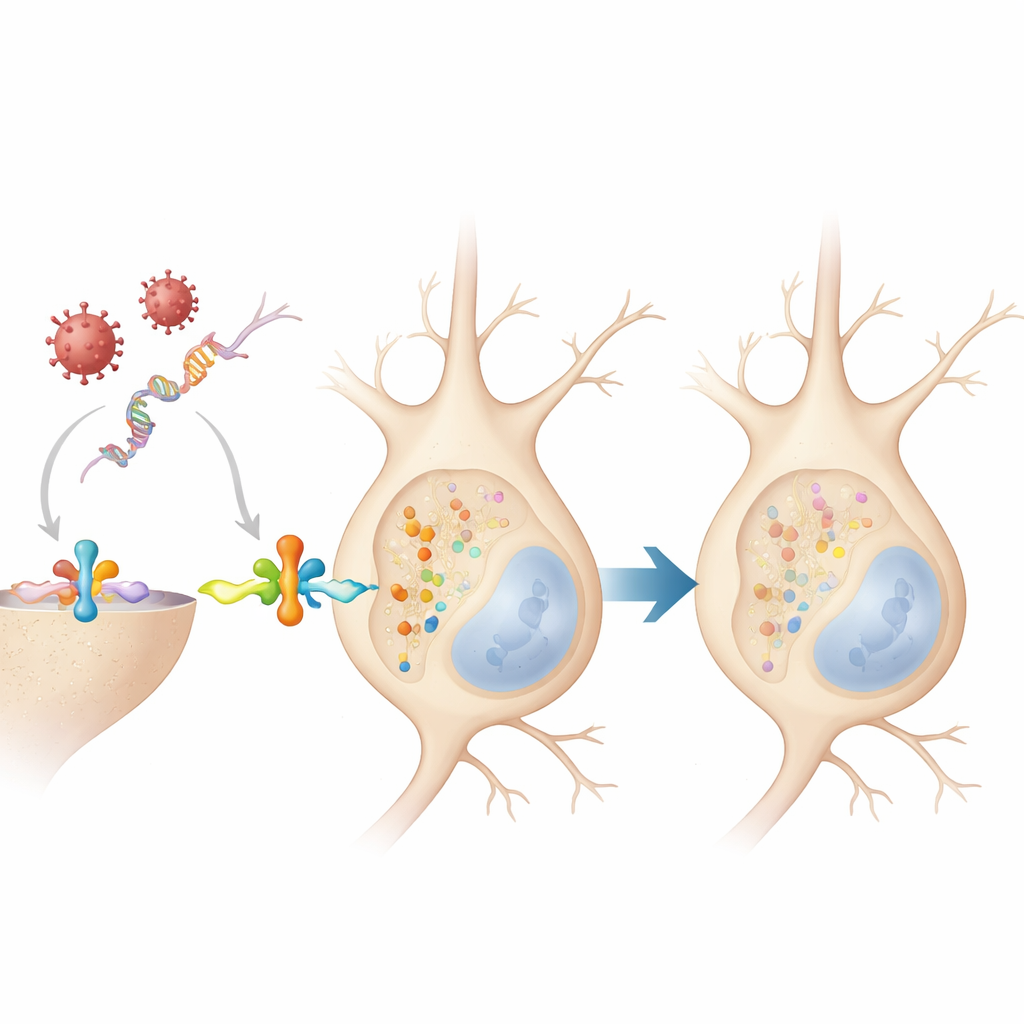
Ce que cela signifie pour la santé cérébrale à long terme
Pris ensemble, ces travaux suggèrent que lorsque les neurones déclenchent une défense antivirale, ils modifient brièvement l’alpha‑synucléine d’une manière normalement réversible et qui ne crée pas immédiatement de dépôts toxiques. Cependant, parce que cette réponse apparaît chez différentes espèces et face à divers virus, des infections répétées ou une inflammation chronique au cours de la vie pourraient activer à plusieurs reprises cet interrupteur moléculaire. Si les systèmes qui éliminent habituellement l’alpha‑synucléine marquée deviennent surchargés ou défaillants avec l’âge, ces modifications bénignes et fugitives pourraient commencer à s’accumuler, poussant la protéine vers les agrégats observés dans la maladie de Parkinson et les affections apparentées. Dans cette optique, le marquage de l’alpha‑synucléine n’est pas seulement un signe de dommage mais fait partie de la réponse précoce du cerveau à l’infection — une réponse qui, dans de mauvaises conditions, peut lentement basculer du protecteur au nocif.
Citation: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Mots-clés: Maladie de Parkinson, alpha-synucléine, infection virale, interféron, neuroinflammation