Clear Sky Science · es
La inmunidad innata antiviral induce la fosforilación de alfa-sinucleína en serina129 en neuronas independiente de la agregación
Por qué los virus y el Parkinson podrían estar relacionados
Muchas personas que se recuperan de infecciones virales graves desarrollan más tarde problemas de memoria, de movimiento o del estado de ánimo. Al mismo tiempo, enfermedades cerebrales como el Parkinson se caracterizan por acúmulos anormales de una proteína llamada alfa-sinucleína dentro de las neuronas. Este estudio plantea una pregunta urgente para pacientes y familias: cuando el cerebro combate un virus, ¿esa misma respuesta inmune empuja a la alfa-sinucleína hacia cambios que, con el tiempo, pueden preparar el terreno para trastornos similares al Parkinson?
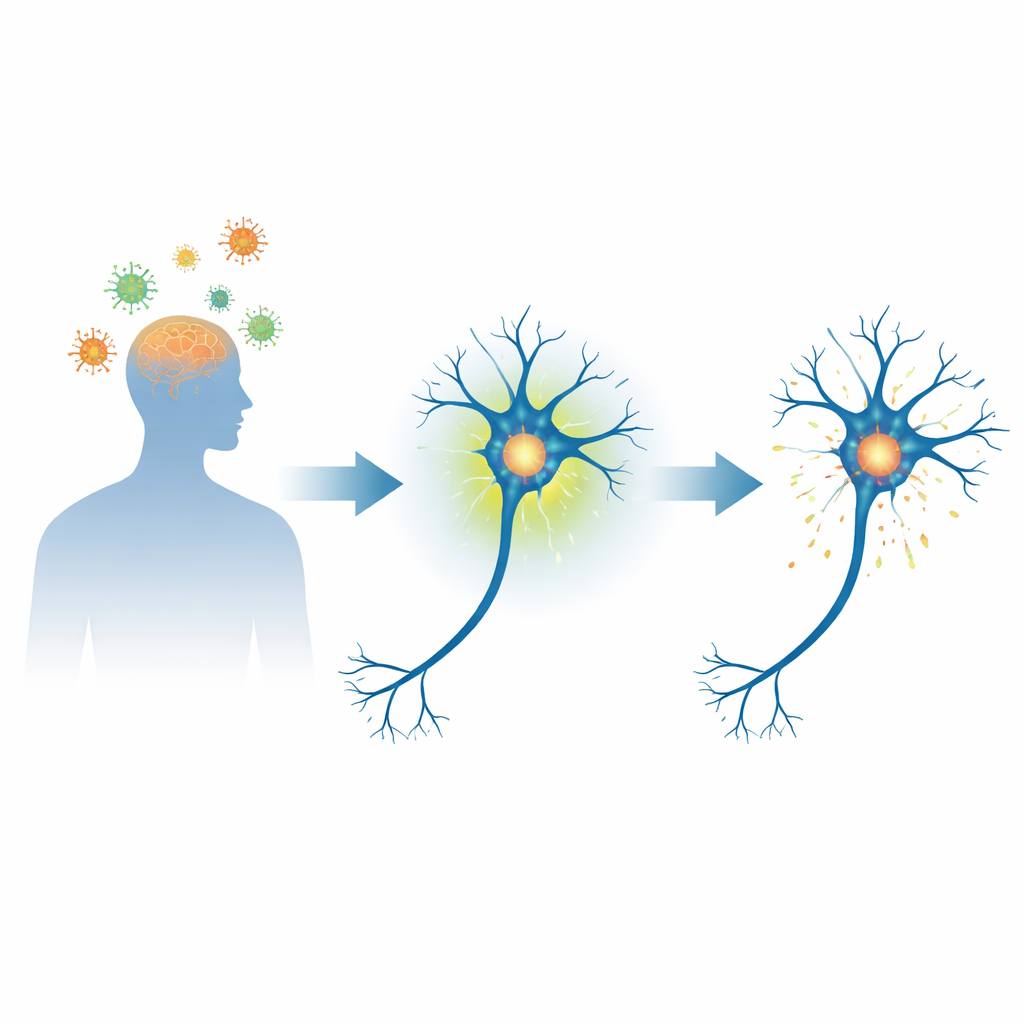
Una proteína neuronal en el centro de la enfermedad cerebral
La alfa-sinucleína es una proteína pequeña y flexible, abundante en las neuronas, que ayuda a regular cómo se transmiten las señales entre ellas. En la enfermedad de Parkinson y afecciones relacionadas, esta proteína puede plegarse mal y acumularse en depósitos densos conocidos como cuerpos de Lewy, que se asocian estrechamente con la muerte neuronal. Una etiqueta química clave en esta proteína, denominada fosforilación en un sitio específico (serina 129), se encuentra en la mayor parte de la alfa-sinucleína dentro de estos depósitos. Eso ha llevado a los científicos a preguntarse si esta etiqueta es simplemente un marcador de daño o un paso temprano en la progresión hacia la enfermedad.
Pistas de personas y animales con infecciones cerebrales
Los investigadores examinaron primero tejido cerebral de personas que murieron con una infección cerebral severa por el virus del Nilo Occidental. En comparación con cerebros de control, los cerebros infectados mostraron más alfa-sinucleína con la etiqueta en serina 129 dentro de las neuronas, especialmente en áreas importantes para el movimiento, y esas mismas células mostraban signos de señalización antiviral activa. Para probar causa y efecto, el equipo desarrolló luego un modelo de ratón en el que el virus del Nilo Occidental viaja desde la nariz hacia el cerebro a lo largo de las vías olfatorias. A medida que el virus se propagaba, los animales perdieron peso, activaron genes antivirales fuertes y —crucialmente— mostraron un aumento de alfa-sinucleína etiquetada en los bulbos olfatorios, aunque la proteína aún no había formado agregados insolubles.
Desencadenantes virales sin acúmulos duraderos
Para ver si esto era una respuesta general, los científicos estudiaron otros virus. Un virus de ADN que causa una enfermedad similar a la culebrilla en monos, y el virus del herpes simple en ratones, también aumentaron la alfa-sinucleína etiquetada en grupos neuronales que sirven la piel y la cara. En cultivos de células cerebrales de ratón, la infección por el virus del Nilo Occidental elevó rápidamente los niveles de alfa-sinucleína etiquetada en cuestión de horas, pero esos niveles luego descendieron, y pruebas sensibles no detectaron nuevos agregados. Incluso imitar el material genético viral con una molécula sintética, sin usar virus real, fue suficiente para aumentar temporalmente la forma etiquetada de la proteína en neuronas, nuevamente sin crear acúmulos.
Interferón: el mensajero que activa la etiqueta
Lo que unificó todas estas observaciones fue el sistema de alarma de primera línea del cerebro: el interferón de tipo I, una familia de proteínas que las neuronas liberan cuando detectan material genético viral. En neuronas cultivadas, tanto la infección real como el análogo viral provocaron que las células secretaran este tipo de interferón, y el tratamiento directo solo con interferón duplicó rápidamente los niveles de alfa-sinucleína etiquetada en 30 minutos. Este pico fue de corta duración y aun así no se acompañó de agregados. De forma llamativa, cuando el equipo repitió los experimentos en neuronas genéticamente desprovistas del receptor de interferón, ni el virus ni el análogo de ARN pudieron aumentar la alfa-sinucleína etiquetada. Eso muestra que la etiqueta se añade aguas abajo de la señalización por interferón, no por acción directa del virus.
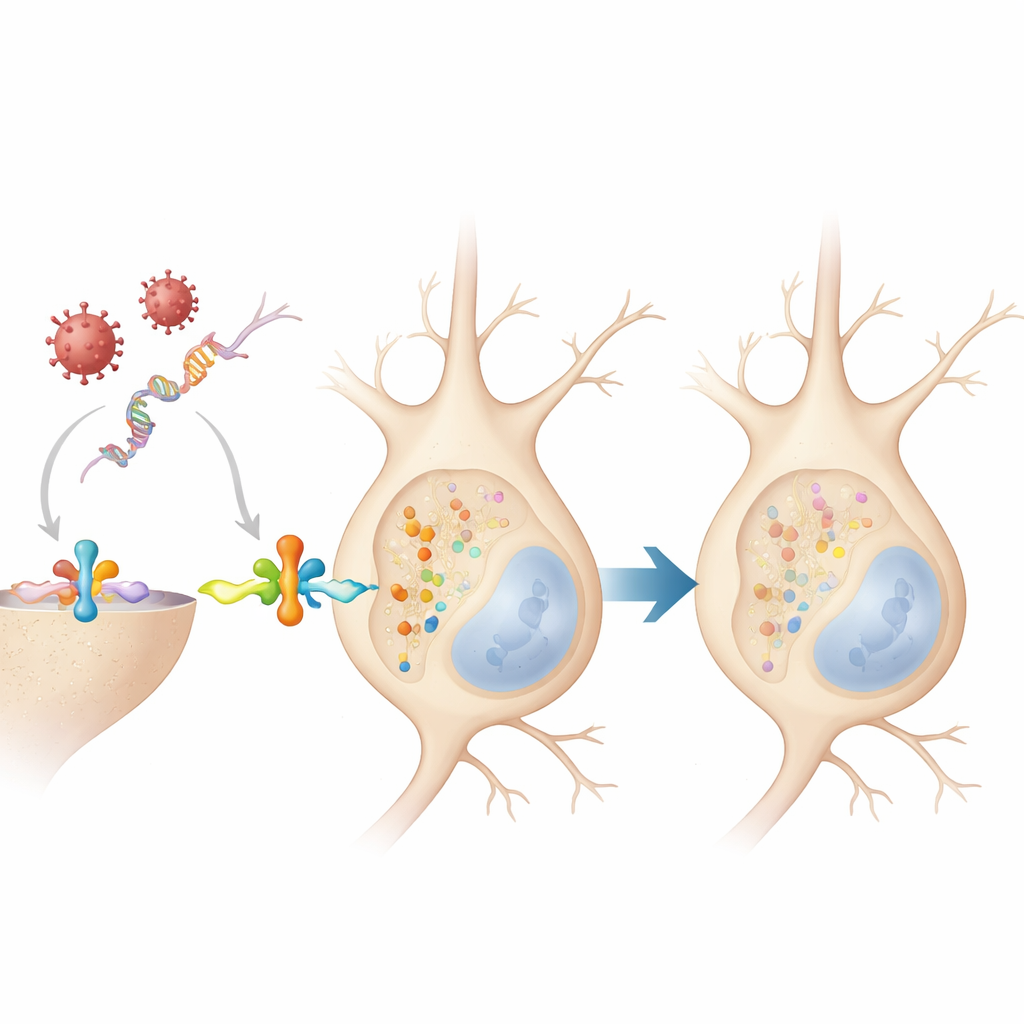
Qué significa esto para la salud cerebral a largo plazo
En conjunto, el trabajo sugiere que cuando las neuronas montan una defensa antiviral, modifican brevemente la alfa-sinucleína de una manera que normalmente es reversible y no crea de inmediato agregados tóxicos. Sin embargo, dado que esta respuesta aparece en distintas especies y con virus diversos, infecciones repetidas o inflamación crónica a lo largo de la vida podrían activar este interruptor molecular de forma recurrente. Si los sistemas que normalmente eliminan la alfa-sinucleína etiquetada se sobrecargan o fallan con la edad, estos cambios fugaces e inofensivos podrían empezar a acumularse, impulsando a la proteína hacia los agregados observados en el Parkinson y enfermedades relacionadas. En esta perspectiva, el etiquetado de la alfa-sinucleína no es solo un signo de daño, sino parte de la respuesta temprana del cerebro a la infección —una respuesta que, en condiciones adversas, puede lentamente pasar de protectora a perjudicial.
Cita: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Palabras clave: Enfermedad de Parkinson, alfa-sinucleína, infección viral, interferón, neuroinflamación