Clear Sky Science · de
Antivirale angeborene Immunität induziert die Phosphorylierung von Alpha‑Synuclein an Serin129 in Neuronen unabhängig von Aggregation
Warum Viren und Parkinson miteinander verknüpft sein könnten
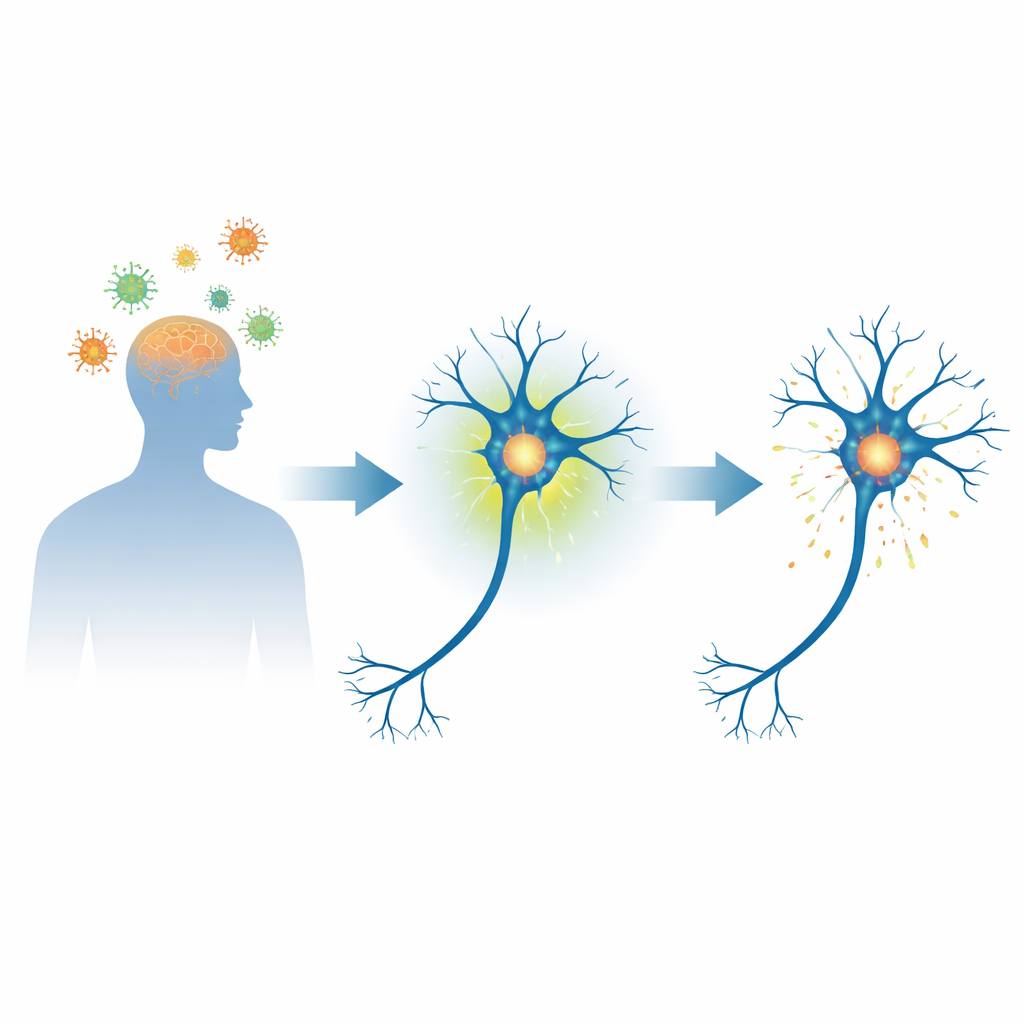
Viele Menschen, die sich von schweren Virusinfektionen erholen, entwickeln später Probleme mit Gedächtnis, Bewegung oder Stimmung. Gleichzeitig zeichnen sich Erkrankungen wie Parkinson durch abnorme Ablagerungen des Proteins Alpha‑Synuclein in Nervenzellen aus. Diese Studie stellt eine dringliche Frage für Patientinnen, Patienten und Angehörige: Bewirkt die Immunantwort des Gehirns gegen ein Virus, dass Alpha‑Synuclein in eine Richtung verändert wird, die über Jahre hinweg die Grundlage für Parkinson‑ähnliche Erkrankungen legen kann?
Ein Nervenzellprotein im Zentrum neurologischer Erkrankungen
Alpha‑Synuclein ist ein kleines, flexibles Protein, das in Nervenzellen reichlich vorkommt und die Übertragung von Signalen zwischen ihnen mitregelt. Bei Morbus Parkinson und verwandten Erkrankungen kann dieses Protein fehlfalten und sich zu dichten Ablagerungen, den sogenannten Lewy‑Körpern, anreichern, die eng mit dem Untergang von Nervenzellen verbunden sind. Eine wichtige chemische Markierung an diesem Protein — die Phosphorylierung an einer bestimmten Stelle (Serin 129) — findet sich an den meisten Alpha‑Synuclein‑Molekülen in diesen Ablagerungen. Das hat Wissenschaftlerinnen und Wissenschaftler darüber nachdenken lassen, ob diese Markierung nur ein Schadenanzeiger ist oder ein früher Schritt auf dem Weg zur Krankheit.
Anhaltspunkte aus Menschen und Tieren mit Gehirninfektionen
Die Forschenden untersuchten zunächst Hirngewebe von Personen, die an einer schweren West-Nil‑Virus‑Enzephalitis gestorben waren. Im Vergleich zu Kontrollhäuten zeigten die infizierten Gehirne mehr Alpha‑Synuclein mit der Serin‑129‑Markierung innerhalb von Neuronen, insbesondere in für die Bewegung wichtigen Bereichen, und dieselben Zellen wiesen Anzeichen aktiver antiviraler Signalgebung auf. Um Ursache und Wirkung zu prüfen, entwickelte das Team anschließend ein Mausmodell, in dem sich das West‑Nil‑Virus über die Riechbahn von der Nase ins Gehirn ausbreitet. Während das Virus sich ausbreitete, verloren die Tiere an Gewicht, schalteten starke antivirale Gene ein und zeigten — entscheidend — einen Anstieg des markierten Alpha‑Synucleins in den Riechkolben, obwohl das Protein noch keine unlöslichen Aggregate gebildet hatte.
Virale Auslöser ohne dauerhafte Aggregate
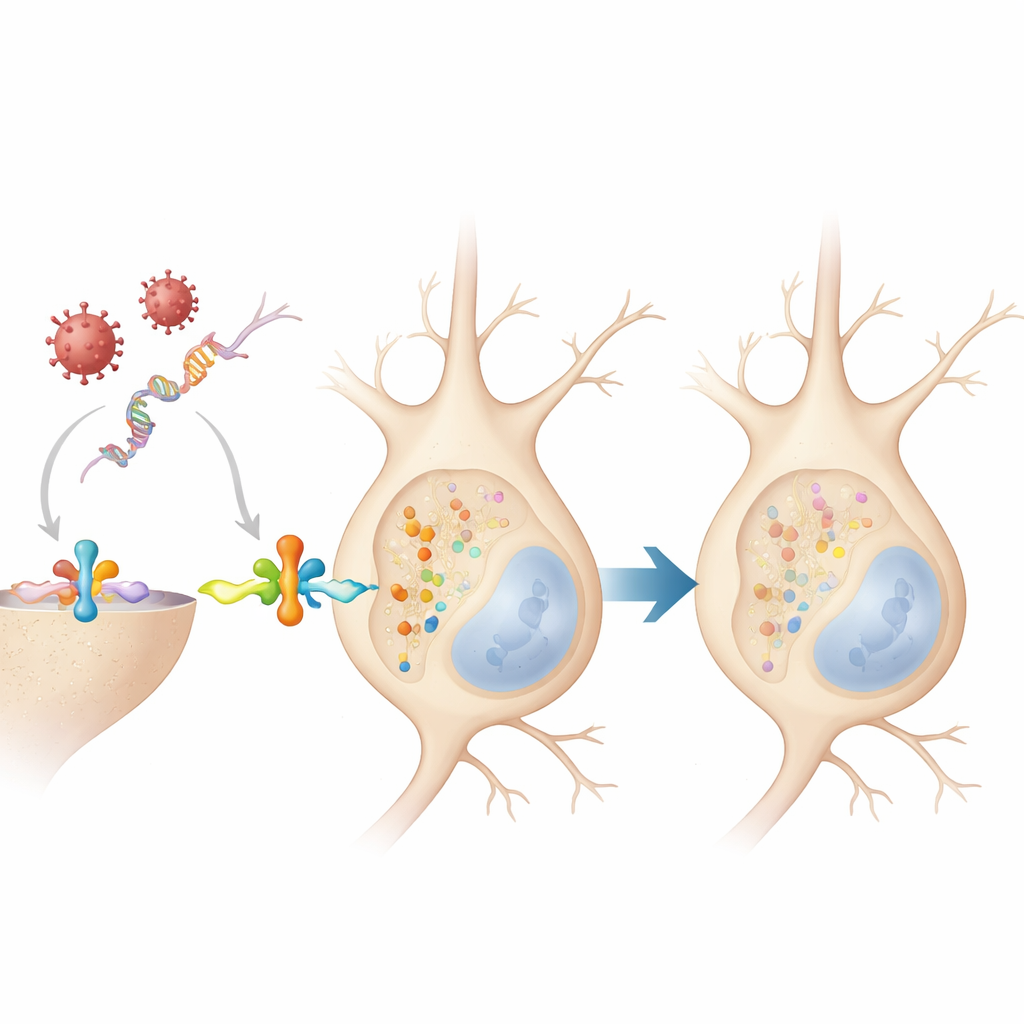
Um zu prüfen, ob es sich um eine allgemeine Reaktion handelt, betrachteten die Forschenden weitere Viren. Ein DNA‑Virus, das bei Affen eine Gürtelrose‑ähnliche Erkrankung verursacht, und das Herpes‑simplex‑Virus in Mäusen erhöhten ebenfalls das markierte Alpha‑Synuclein in Nervenknoten, die Haut und Gesicht versorgen. In Zellkulturen muriner Gehirnzellen führte eine West‑Nil‑Virus‑Infektion innerhalb weniger Stunden zu einem raschen Anstieg markierten Alpha‑Synucleins, doch fielen diese Werte anschließend wieder ab, und empfindliche Tests detektierten keine neuen Aggregate. Selbst das Nachahmen viraler Genmaterialien mit einem synthetischen Molekül, ohne echten Erreger, genügte, um die markierte Form des Proteins in Neuronen vorübergehend zu erhöhen — wiederum ohne Bildung von Klumpen.
Interferon: Der Botenstoff, der die Markierung einschaltet
Was all diese Beobachtungen verband, war das Alarm‑System des Gehirns: Typ‑I‑Interferon, eine Proteinfamilie, die Nervenzellen freisetzen, wenn sie virales Genmaterial wahrnehmen. In kultivierten Neuronen führten sowohl echte Infektionen als auch der virale Nachahmer dazu, dass die Zellen diese Art von Interferon abgaben, und eine direkte Behandlung mit Interferon allein verdoppelte innerhalb von 30 Minuten rasch die Menge an markiertem Alpha‑Synuclein. Dieser Spitzenwert war kurzlebig und ging ebenfalls nicht mit Aggregatbildung einher. Auffällig war, dass weder das Virus noch der RNA‑Mimik in Neuronen ohne Interferonrezeptor den Anstieg des markierten Alpha‑Synucleins hervorrufen konnten. Das zeigt, dass die chemische Markierung downstream der Interferon‑Signalgebung hinzugefügt wird, nicht direkt durch den Virus.
Was das für die langfristige Gehirngesundheit bedeutet
Zusammengefasst legen die Ergebnisse nahe, dass Neuronen bei einer antiviralen Abwehr Alpha‑Synuclein kurzzeitig so modifizieren, dass die Veränderung normalerweise reversibel ist und nicht sofort toxische Aggregate erzeugt. Weil diese Reaktion jedoch bei verschiedenen Arten und unterschiedlichen Viren auftritt, könnten wiederholte Infektionen oder chronische Entzündungen im Laufe des Lebens diesen molekularen Schalter wiederholt umlegen. Wenn die Systeme, die markiertes Alpha‑Synuclein normalerweise entfernen, im Alter überfordert sind oder versagen, könnten sich diese harmlosen, flüchtigen Veränderungen anhäufen und das Protein in Richtung der bei Parkinson beobachteten Aggregate drängen. Nach dieser Sichtweise ist die Alpha‑Synuclein‑Markierung nicht nur ein Schadenmarker, sondern Teil der frühen Infektionsantwort des Gehirns — eine Reaktion, die unter ungünstigen Bedingungen langsam vom Schützenden ins Schädliche umschlagen kann.
Zitation: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Schlüsselwörter: Morbus Parkinson, Alpha‑Synuclein, Virusinfektion, Interferon, Neuroinflammation