Clear Sky Science · pt
Imunidade inata antiviral induz fosforilação da alfa-sinucleína na serina129 em neurônios independentemente da agregação
Por que vírus e Parkinson podem estar relacionados
Muitas pessoas que se recuperam de infecções virais graves desenvolvem mais tarde problemas de memória, movimento ou humor. Ao mesmo tempo, doenças cerebrais como o Parkinson são caracterizadas por aglomerados anormais de uma proteína chamada alfa‑sinucleína dentro dos neurônios. Este estudo aborda uma pergunta urgente para pacientes e famílias: quando o cérebro combate um vírus, essa própria resposta imune empurra a alfa‑sinucleína para alterações que, ao longo dos anos, podem preparar o terreno para transtornos semelhantes ao Parkinson?
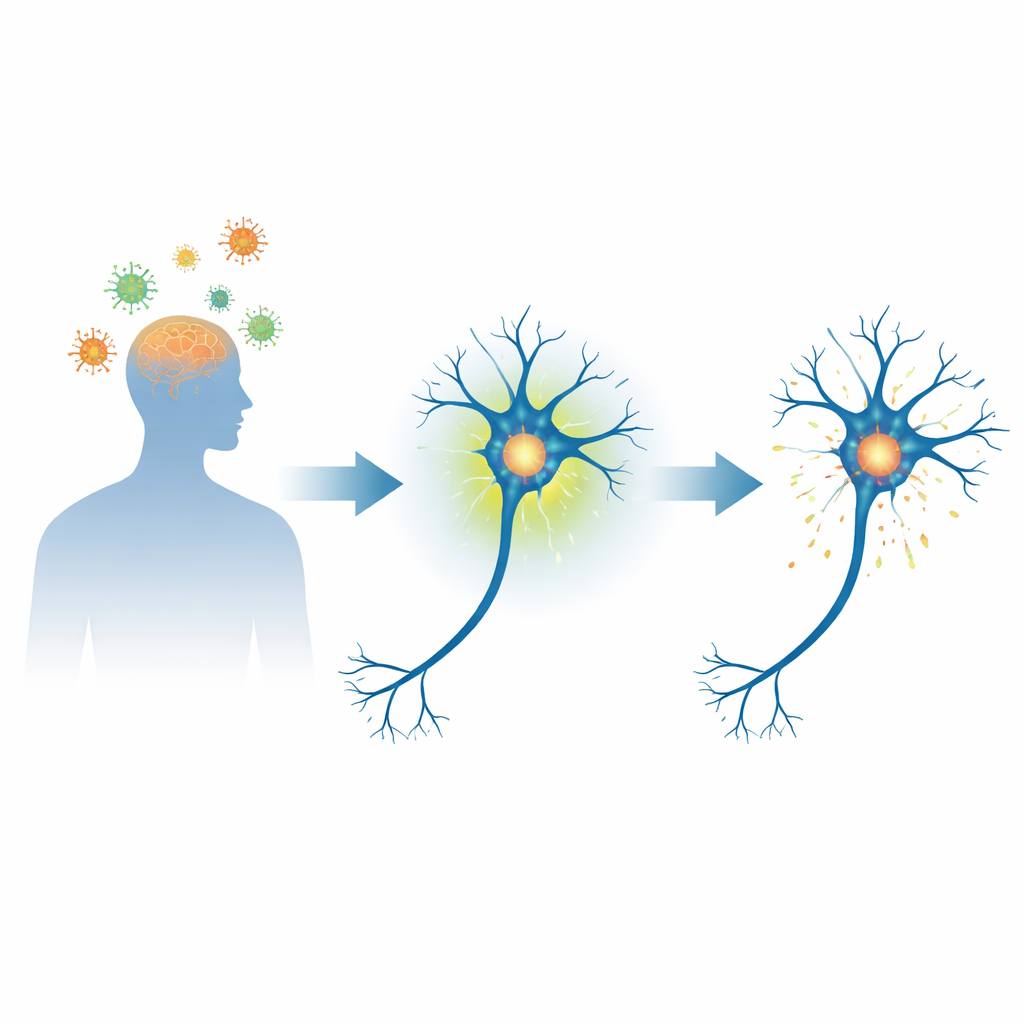
Uma proteína neuronal no centro da doença cerebral
A alfa‑sinucleína é uma proteína pequena e flexível, abundante nos neurônios, que ajuda a regular a transmissão de sinais entre eles. Na doença de Parkinson e em condições relacionadas, essa proteína pode se dobrar de forma incorreta e acumular‑se em depósitos densos conhecidos como corpos de Lewy, que estão intimamente ligados à morte neuronal. Uma marca química chave nessa proteína, chamada fosforilação em um sítio específico (serina 129), é encontrada na maior parte da alfa‑sinucleína dentro desses depósitos. Isso levou os cientistas a questionar se essa marca é meramente um marcador de dano ou um passo inicial no caminho para a doença.
Pistas de pessoas e animais com infecções cerebrais
Os pesquisadores começaram examinando tecido cerebral de pessoas que morreram com infecção cerebral severa pelo vírus West Nile. Em comparação com cérebros de controle, os cérebros infectados mostraram mais alfa‑sinucleína portando a marca na serina‑129 dentro dos neurônios, especialmente em áreas importantes para o movimento, e essas mesmas células exibiram sinais de sinalização antiviral ativa. Para testar causa e efeito, a equipe desenvolveu um modelo de camundongo em que o vírus West Nile viaja do nariz para o cérebro ao longo das vias olfativas. À medida que o vírus se espalhava, os animais perderam peso, ativaram genes antivirais fortes e — crucialmente — apresentaram um aumento da alfa‑sinucleína marcada nos bulbos olfatórios, embora a proteína ainda não tivesse formado agregados insolúveis.
Gatilhos virais sem aglomerados duradouros
Para ver se essa era uma resposta geral, os cientistas examinaram outros vírus. Um vírus de DNA que causa uma doença semelhante a cobreiro em macacos, e o vírus herpes simplex em camundongos, também aumentaram a alfa‑sinucleína marcada em aglomerados nervosos que atendem à pele e ao rosto. Em culturas de células cerebrais de camundongo, a infecção por West Nile aumentou rapidamente os níveis de alfa‑sinucleína marcada em poucas horas, mas esses níveis depois diminuíram, e testes sensíveis não detectaram novos agregados. Até mesmo mimetizar material genético viral com uma molécula sintética, sem usar vírus real, foi suficiente para aumentar temporariamente a forma marcada da proteína em neurônios, novamente sem criar aglomerados.
Interferon: o mensageiro que liga a marca
O que uniu todas essas observações foi o sistema de alarme de primeira linha do cérebro: o interferon tipo I, uma família de proteínas que os neurônios liberam quando detectam material genético viral. Em neurônios cultivados, tanto a infecção real quanto o mimético viral fizeram as células secretarem esse tipo de interferon, e o tratamento direto apenas com interferon dobrou rapidamente os níveis de alfa‑sinucleína marcada em 30 minutos. Esse pico foi de curta duração e ainda não veio acompanhado de agregados. Notavelmente, quando a equipe repetiu os experimentos em neurônios geneticamente desprovidos do receptor de interferon, nem o vírus nem o mimético de RNA conseguiram aumentar a alfa‑sinucleína marcada. Isso mostra que a marca química é adicionada a jusante da sinalização por interferon, não pelo vírus em si.
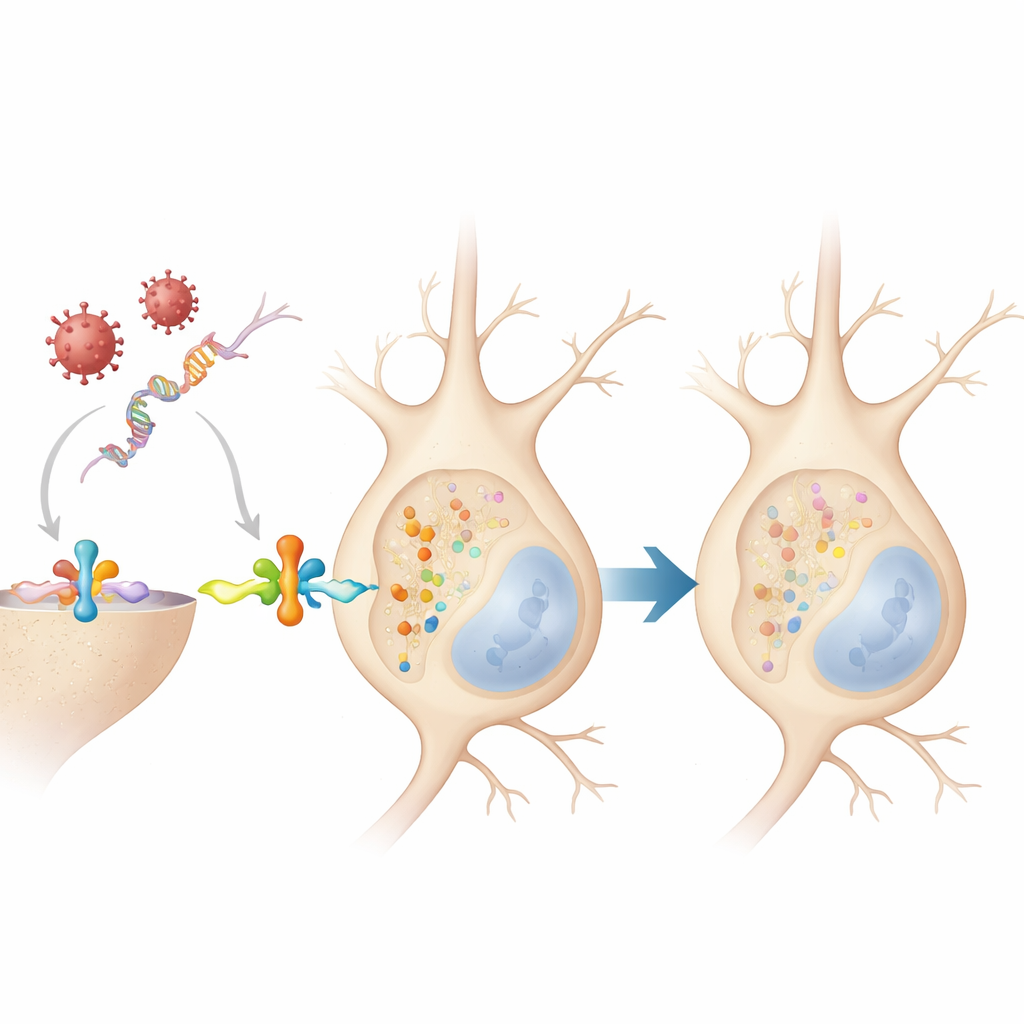
O que isso significa para a saúde cerebral a longo prazo
Em conjunto, o trabalho sugere que quando os neurônios montam uma defesa antiviral, eles modificam brevemente a alfa‑sinucleína de uma forma que normalmente é reversível e não cria imediatamente aglomerados tóxicos. No entanto, porque essa resposta aparece em diferentes espécies e com vírus diversos, infecções repetidas ou inflamação crônica ao longo da vida podem ligar esse interruptor molecular repetidamente. Se os sistemas que normalmente removem a alfa‑sinucleína marcada ficarem sobrecarregados ou falharem com a idade, essas mudanças inofensivas e transitórias podem começar a se acumular, empurrando a proteína na direção dos agregados vistos no Parkinson e em doenças relacionadas. Nessa visão, a marcação da alfa‑sinucleína não é apenas um sinal de dano, mas parte da resposta inicial do cérebro à infecção — uma resposta que, em condições inadequadas, pode lentamente passar de protetora a prejudicial.
Citação: Heiden, D.L., Merrick, C., Evans, R.C. et al. Antiviral innate immunity induces alpha synuclein phosphorylation at serine129 in neurons independent of aggregation. npj Parkinsons Dis. 12, 80 (2026). https://doi.org/10.1038/s41531-026-01297-9
Palavras-chave: Doença de Parkinson, alfa-sinucleína, infecção viral, interferon, neuroinflamação