Clear Sky Science · zh
变体 U1 snRNA 参与人类诱导多能干细胞的细胞周期与分化调控
为什么微小的 RNA 片段对干细胞很重要
干细胞之所以吸引临床与工程领域的关注,是因为它们可以分化为机体中的几乎任何细胞。这一潜能依赖于非常严格的内部控制。本研究考察了人类诱导多能干细胞中一类长期被忽视的微小 RNA 分子,并显示它们在悄然决定干细胞分裂速率以及准备好分化为专门细胞的程度方面发挥作用。
细胞“信息加工厂”中的小帮手
在每个细胞内部,基因首先被转录为 RNA 信息,这些信息随后被修剪和拼接后才作为制造蛋白质的指令被解读。这个修剪机制的关键成分之一是称为 U1 的小 RNA。多年来,类似 U1 的额外拷贝被认为是无用的残留物。作者将注意力集中在其中两个长得很像的变体 U1 上,这些变体在早期人类组织和干细胞中尤其活跃。由于它们的序列与主要 U1 略有不同,它们可能识别不同的切割位点,从而微妙改变细胞可以产生的蛋白质版本。
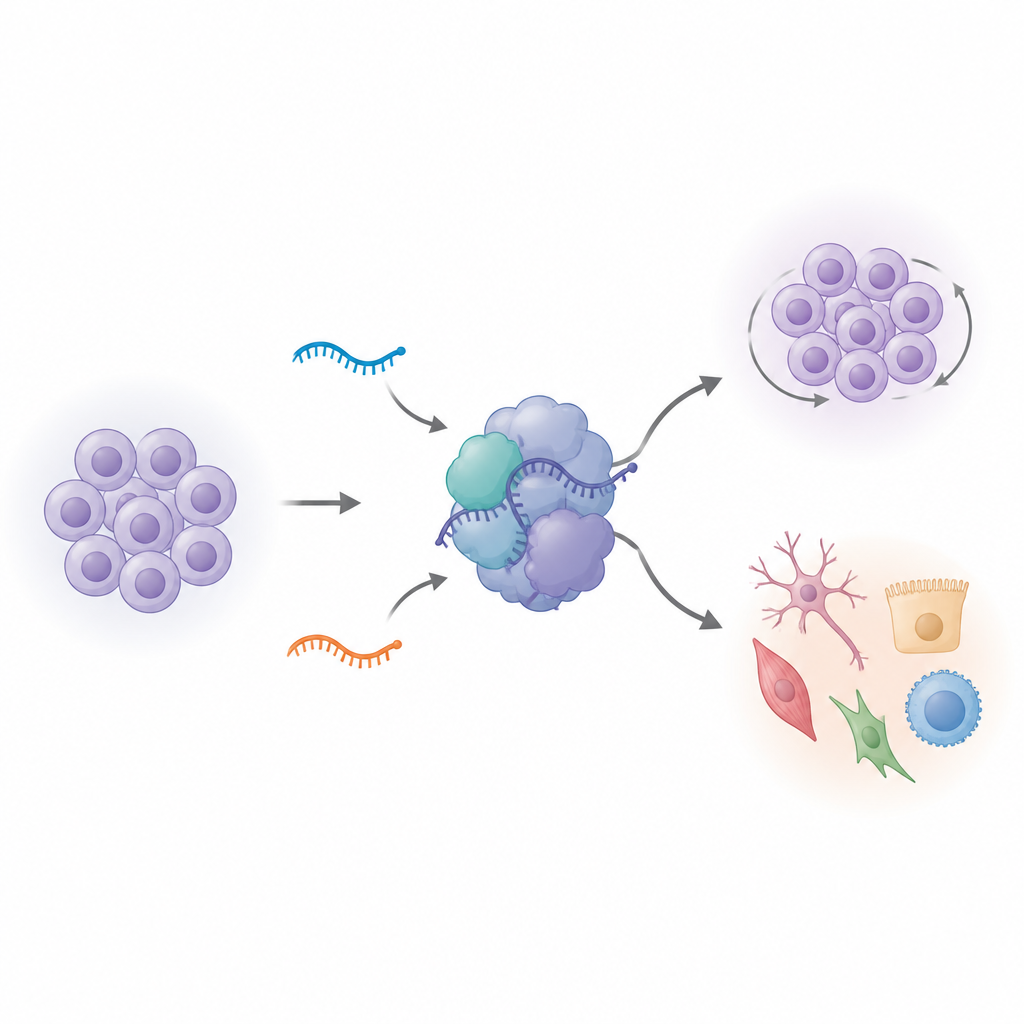
关闭变体 RNA 重塑干细胞行为
为了弄清这些变体 U1 究竟有什么作用,研究团队使用基因组编辑在人体诱导多能干细胞中删除了任一变体。乍看之下,被编辑的细胞外观正常。但当研究人员测量哪些基因被开启或关闭时,他们发现了大范围的变化,尤其是在删除了一个变体 vU1.8 时。数百个参与细胞分裂与干细胞身份的基因活性发生了改变。细胞的内部时钟也随之改变:更多细胞在细胞周期的后期积累,当细胞被推动开始分化时整体生长速率增加。那些通常标记干性与早期脑发育的基因不再遵循正常模式,这表明这些小型 RNA 有助于将干细胞维持在自我更新与专门化之间的精细调节状态。
通过切割与重接编辑信息
研究随后聚焦于变体 U1 如何影响 RNA 信息的精细编辑。许多人体基因可以以不同方式被切割和重接,产生在稳定性、定位或活性方面有所不同的蛋白质变体。通过比较正常与被编辑的干细胞,作者发现了数千处 RNA 剪接方式的变化。一些信息失去了重要的蛋白编码片段,而转而产生缩短或非编码的版本。某一变体偏向于在信息的起始与末端发生变化,修剪那些可控制 RNA 寿命和使用时机的尾部区域。与细胞分裂和神经发育相关的基因受到的影响尤其明显,将这些微小 RNA 与健康生长和大脑形成的关键过程联系起来。
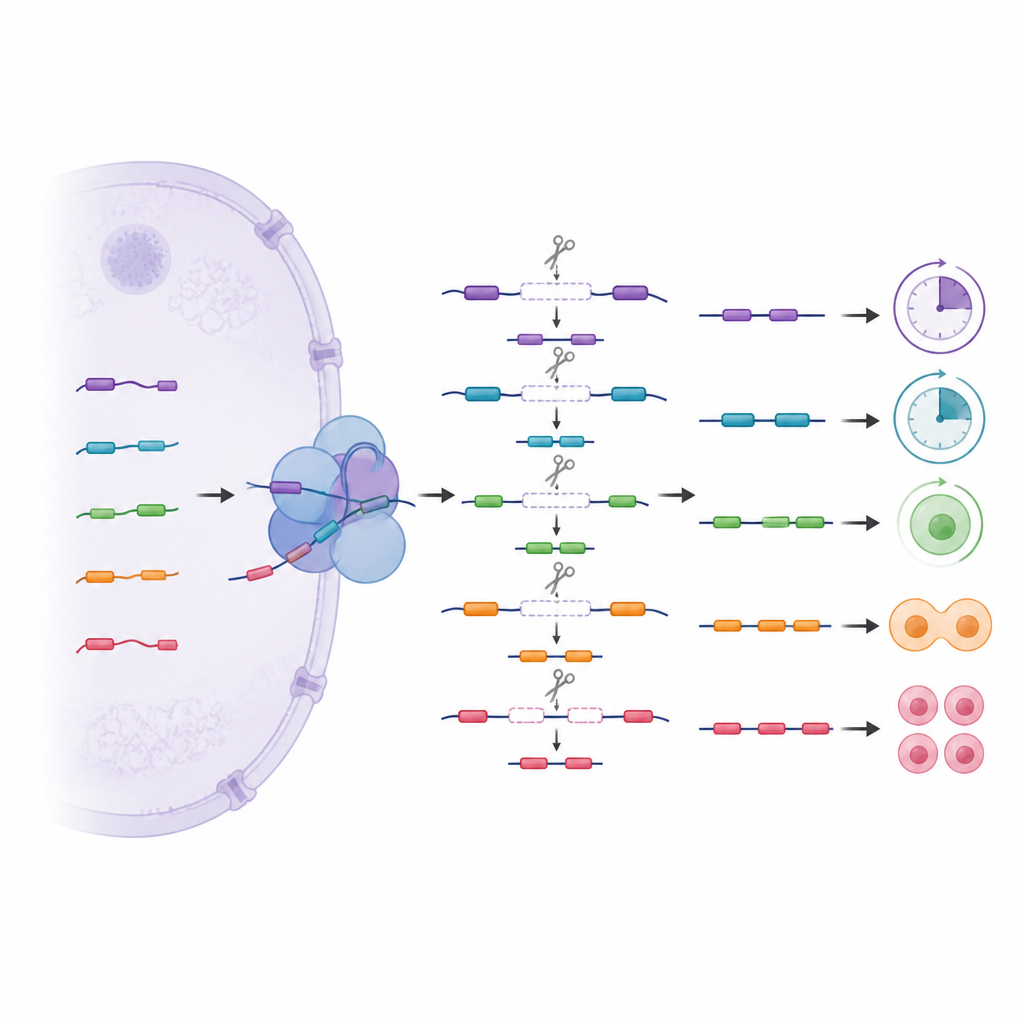
一种被隐藏的分步骤剪切层次
除了常规剪接,团队还探究了一种更复杂的模式,称为递归剪接,其中长的基因片段通过使用隐藏的内部切割位点分几步移除。这种分步骤的切割在早期发育的细胞以及那些管理 DNA、RNA 与细胞信号的基因中最为常见。通过追踪在正常与被编辑的干细胞中某些位点的使用频率,作者发现变体 U1 帮助选择哪些隐藏切割位点被识别。丢失某一变体会导致某些位点被跳过而其他位点使用增多,进而改变附近的信息片段。其中一些隐藏段表现得像通常被排除在最终信息之外的隐匿小外显子,但在控制失衡时可能被插入,潜在导致 RNA 不稳定或被降解。
对干细胞科学与疾病的意义
总体而言,这项工作揭示了这些变体 U1 RNA 并非沉默的旁观者。它们影响干细胞是否分裂、可以产生哪些蛋白版本以及 RNA 信息能存留多久。通过调节常规与分步骤剪接,它们为维持人类多能干细胞并引导其早期向神经元等细胞类型分化的基因控制网络增添了一道精细调节层。因为含有这些特殊剪接位点的基因也携带与人类疾病相关的遗传变异,理解变体 U1 的工作机制或有助于最终解释为何某些非编码 DNA 的改变会导致发育或神经系统疾病。
引用: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
关键词: 干细胞, RNA 剪接, 细胞周期, 多能性, 神经发育