Clear Sky Science · sv
Variant U1-snRNA bidrar till cellcykel- och differentieringskontroll i humana iPS-celler
Varför små RNA-bitar spelar roll för stamceller
Stamceller fascinerar läkare och ingenjörer eftersom de kan bli nästan vilken cell i kroppen som helst. Det löftet bygger på mycket strikt intern kontroll. Denna studie undersöker en förbisedd grupp små RNA-molekyler i humana inducerade pluripotenta stamceller och visar att de diskret hjälper till att bestämma hur snabbt stamceller delar sig och hur beredda de är att bli specialiserade celler.
Små hjälpande molekyler i cellens budskapsfabrik
I varje cell kopieras gener först till RNA-budskap, som sedan trimmas och sys ihop innan de läses som instruktioner för att göra proteiner. En viktig del av denna trimningsapparat använder små RNA kallade U1. Under lång tid antogs extra kopior av U1-liknande RNA vara oanvändbara restprodukter. Författarna fokuserar på två av dessa look-alikes, kallade variant U1, som är särskilt aktiva i tidiga mänskliga vävnader och stamceller. Eftersom deras sekvenser skiljer sig något från huvud-U1 kan de känna igen andra klippställen i RNA och subtilt ändra vilka proteinalternativ en cell kan göra.
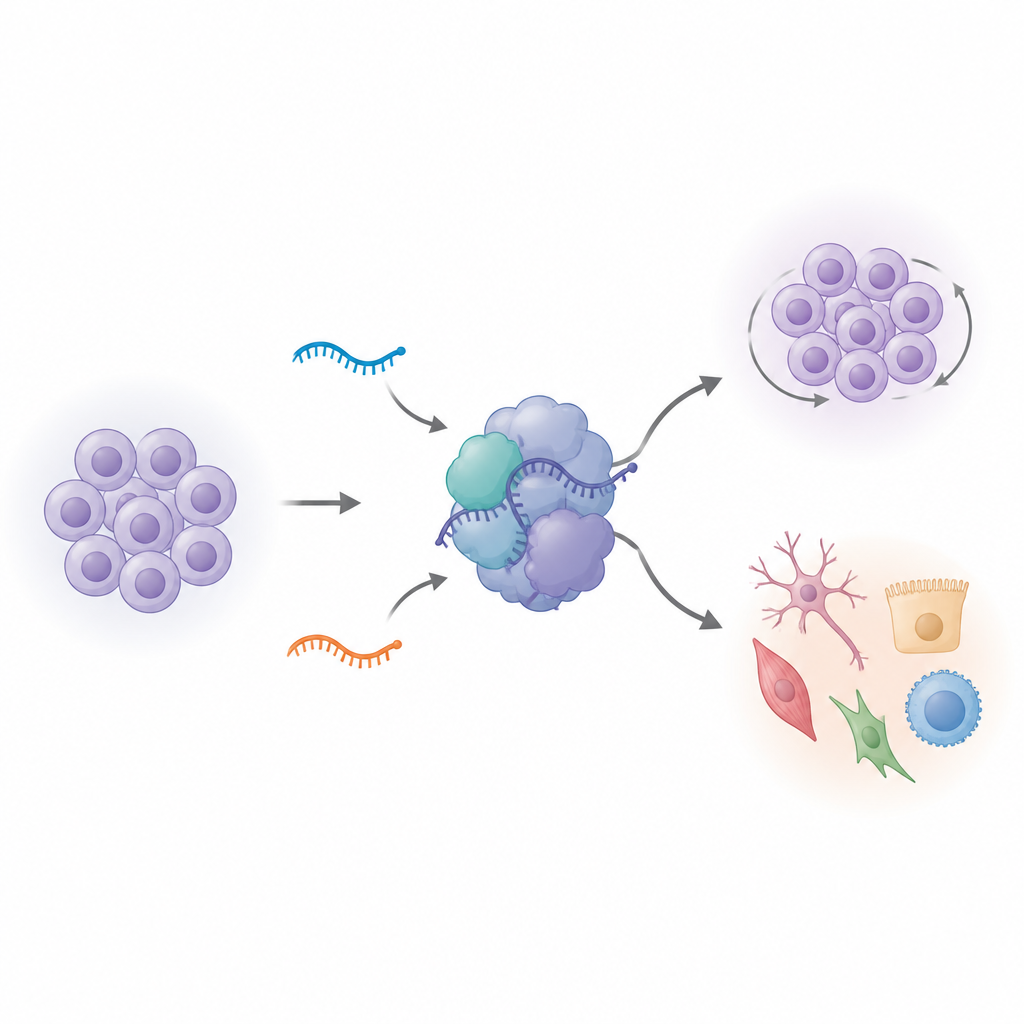
Att stänga av variant-RNA omformar stamcellsbeteende
För att se vad dessa variant U1 faktiskt gör använde teamet genredigering för att ta bort antingen av de två varianterna i humana inducerade pluripotenta stamceller. Vid första anblick såg de redigerade cellerna normala ut. Men när forskarna mätte vilka gener som var påslagna eller avstängda fann de omfattande förändringar, särskilt när en variant, vU1.8, togs bort. Hundratals gener involverade i celldelning och stamcellsidentitet ändrade sin aktivitet. Cellernas interna klockor förändrades också: fler celler samlades i en senare fas av cellcykeln, och den övergripande tillväxthastigheten ökade när cellerna knuffades mot att börja differentiera. Gener som normalt markerar stamstil och tidig hjärnutveckling följde inte längre sina vanliga mönster, vilket tyder på att dessa små RNA hjälper till att hålla stamceller i ett välavvägt tillstånd mellan självförnyelse och specialisering.
Redigerar budskap genom klippning och hopfogning
Studien granskade sedan hur variant U1 påverkar detaljerad bearbetning av RNA-budskap. Många mänskliga gener kan klippas och fogas på olika sätt och ge proteinalternativ som skiljer sig i stabilitet, lokalisation eller aktivitet. Genom att jämföra normala och redigerade stamceller upptäckte författarna tusentals förändringar i hur RNA splitsades. Vissa budskap förlorade viktiga proteinkodande sektioner och producerade istället förkortade eller icke-kodande versioner. En variant gynnade förändringar i början och slutet av budskapen, och trimmade de svansregioner som kan styra hur länge ett RNA överlever och när det används. Gener kopplade till celldelning och neural utveckling påverkades särskilt, vilket kopplar dessa små RNA till processer som är centrala både för hälsosam tillväxt och hjärnbildning.
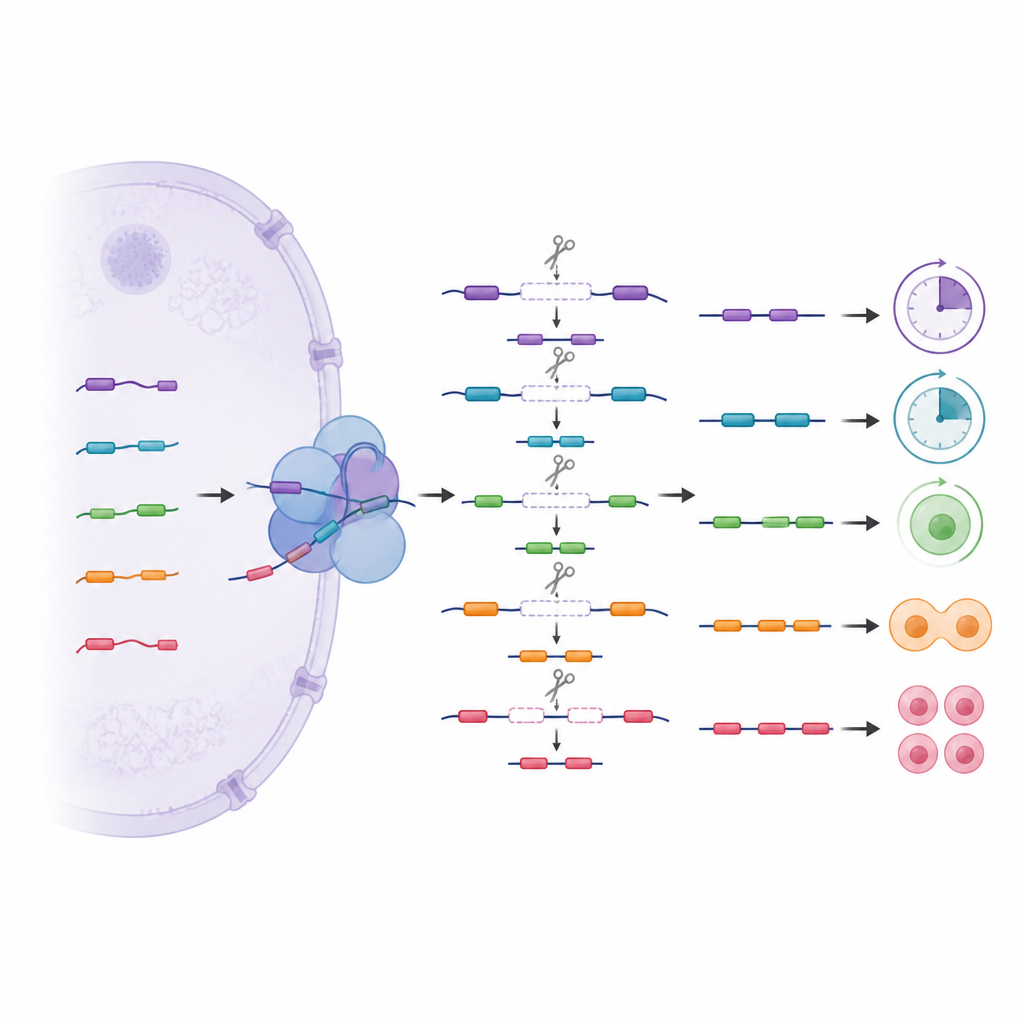
En dold nivå av stegvis klippning
Bortom vanlig splitsning undersökte teamet ett mer komplext mönster kallat rekursiv splitsning, där långa gensegment tas bort i flera steg med hjälp av dolda interna klippställen. Dessa stegvisa klipp var vanligast i celler från tidig utveckling och i gener som hanterar DNA, RNA och cellsignalering. Genom att följa hur ofta specifika platser användes i normala kontra redigerade stamceller fann författarna att variant U1 hjälper till att välja vilka dolda klippställen som känns igen. Förlust av en variant fick vissa ställen att hoppas över och andra att användas oftare, vilket i sin tur ändrade intilliggande budskapsdelar. Några av dessa dolda segment beter sig som kryptiska mini-exon som normalt hålls ute ur slutliga budskap men kan smyga in när kontrollen sviktar, vilket potentiellt leder till instabila eller degraderade RNA.
Vad detta betyder för stamcellsforskning och sjukdom
Sammantaget visar arbetet att dessa variant U1-RNA inte är tysta åskådare. De påverkar om stamceller delar sig, vilka proteinalternativ de kan producera och hur länge deras RNA-budskap varar. Genom att styra både vanlig och stegvis splitsning lägger de till ett finjusteringslager i de genregleringsnätverk som upprätthåller humana pluripotenta stamceller och styr deras tidiga steg mot att bli neuroner och andra celltyper. Eftersom gener som innehåller dessa speciella splitsningsställen också rymmer genetiska varianter kopplade till mänskliga sjukdomar, kan förståelsen för hur variant U1 fungerar så småningom hjälpa till att förklara varför vissa förändringar i icke-kodande DNA bidrar till utvecklings- och neurologiska sjukdomar.
Citering: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Nyckelord: stamceller, RNA-splitsning, cellcykel, pluripotens, neuroutveckling