Clear Sky Science · de
Variante U1-snRNAs tragen zur Kontrolle von Zellzyklus und Differenzierung humaner iPS-Zellen bei
Warum winzige RNA‑Stücke für Stammzellen wichtig sind
Stammzellen faszinieren Ärztinnen und Ingenieure, weil sie sich in nahezu jede Körperzelle verwandeln können. Dieses Potenzial beruht auf strengem inneren Steuerung. Diese Studie untersucht eine bislang wenig beachtete Gruppe winziger RNA‑Moleküle in humanen induzierten pluripotenten Stammzellen und zeigt, dass sie stillschweigend mitentscheiden, wie schnell Stammzellen sich teilen und wie bereit sie sind, zu spezialisierten Zellen zu werden.
Kleine Helfer in der Nachrichtenfabrik der Zelle
In jeder Zelle werden Gene zunächst in RNA‑Botschaften kopiert, die dann zugeschnitten und zusammengesetzt werden, bevor sie als Bauanleitung für Proteine gelesen werden. Ein zentraler Teil dieser Zuschneidemaschinerie nutzt kleine RNAs namens U1. Lange galten zusätzliche Kopien U1‑ähnlicher RNAs als nutzlose Überbleibsel. Die Autoren konzentrieren sich auf zwei dieser Doppelgänger, sogenannte Variante U1s, die in frühen menschlichen Geweben und Stammzellen besonders aktiv sind. Weil sich ihre Sequenzen leicht vom Haupt‑U1 unterscheiden, könnten sie unterschiedliche Schnittstellen in RNAs erkennen und so dezent verändern, welche Proteinvarianten eine Zelle herstellen kann.
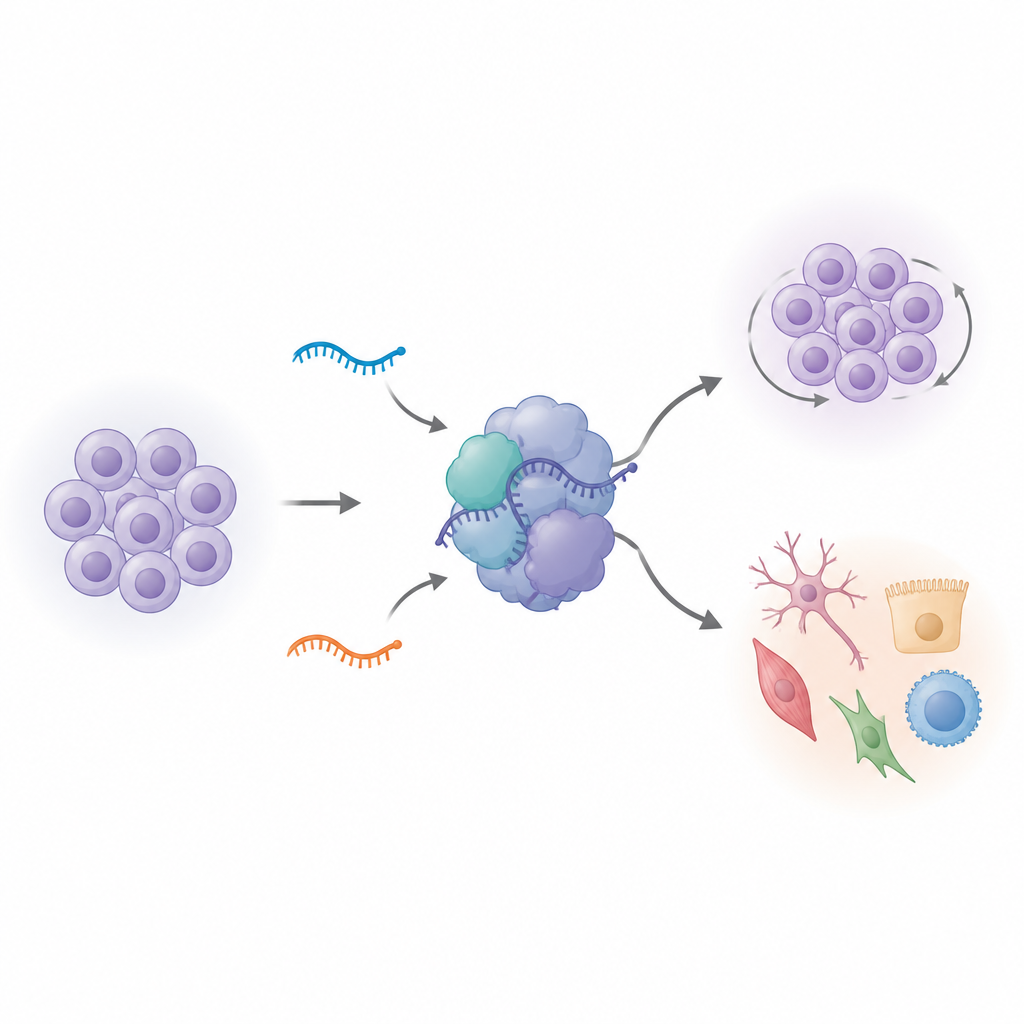
Das Abschalten der Varianten‑RNAs verändert das Verhalten von Stammzellen
Um herauszufinden, was diese Variante U1s tatsächlich bewirken, verwendete das Team Genom‑Editing, um jeweils eine der beiden Varianten in humanen induzierten pluripotenten Stammzellen zu entfernen. Auf den ersten Blick wirkten die editieren Zellen normal. Als die Forschenden jedoch maßen, welche Gene ein‑ oder abgeschaltet waren, fanden sie weitreichende Veränderungen, besonders nach Deletion einer Variante, vU1.8. Hunderte Gene, die an Zellteilung und Stammzellidentität beteiligt sind, veränderten ihre Aktivität. Auch die inneren Uhren der Zellen verschoben sich: Mehr Zellen sammelten sich in einer späteren Phase des Zellzyklus, und die Gesamtwachstumsraten stiegen, wenn die Zellen zum Differenzieren angeregt wurden. Gene, die normalerweise Stammhaftigkeit und frühe Gehirnentwicklung markieren, folgten nicht länger ihren üblichen Mustern, was darauf hindeutet, dass diese kleinen RNAs helfen, Stammzellen in einem fein abgestimmten Zustand zwischen Selbst‑Erneuerung und Spezialisierung zu halten.
Nachrichten bearbeiten durch Schneiden und Wiederverbinden
Die Studie zoomte anschließend darauf, wie Variante U1s das detaillierte Bearbeiten von RNA‑Botschaften beeinflussen. Viele menschliche Gene können auf verschiedene Weisen geschnitten und wieder zusammengefügt werden, wodurch Proteinvarianten mit unterschiedlicher Stabilität, Lokalisation oder Aktivität entstehen. Durch den Vergleich normaler und editierter Stammzellen entdeckten die Autorinnen und Autoren Tausende von Änderungen im Spleißverhalten. Manche Botschaften verloren wichtige protein‑kodierende Abschnitte und produzierten stattdessen verkürzte oder nicht‑kodierende Varianten. Eine Variante begünstigte Veränderungen am Anfang und Ende von Botschaften, indem sie die Schwanzregionen kürzte, die kontrollieren können, wie lange eine RNA überlebt und wann sie benutzt wird. Besonders betroffen waren Gene, die mit Zellteilung und neuronaler Entwicklung verknüpft sind, wodurch diese winzigen RNAs mit Prozessen verbunden werden, die sowohl für gesundes Wachstum als auch für Gehirnbildung zentral sind.
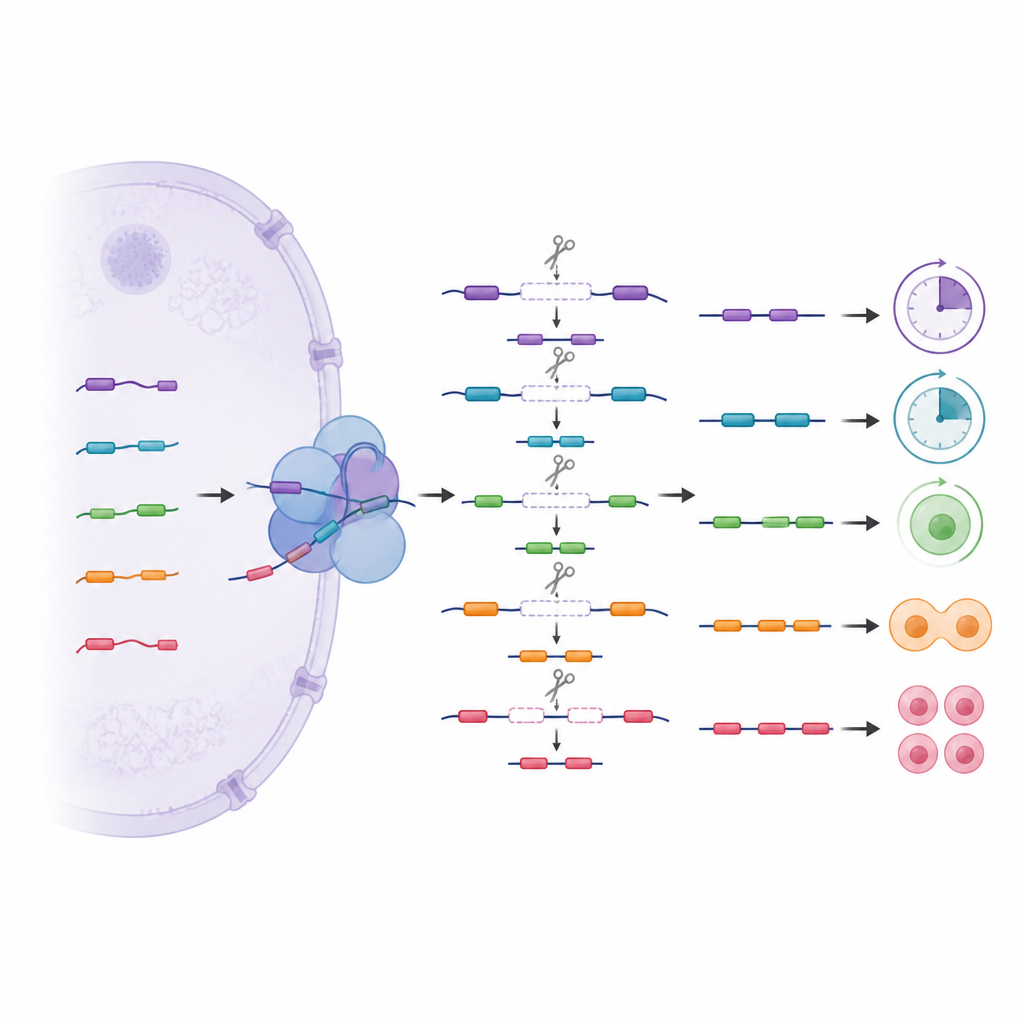
Eine verborgene Ebene schrittweiser Schnitte
Über das gewöhnliche Spleißen hinaus untersuchte das Team ein komplexeres Muster, das rekursive Spleißen genannt wird, bei dem lange Genabschnitte in mehreren Schritten unter Verwendung verborgener interner Schnittstellen entfernt werden. Diese schrittweisen Schnitte traten am häufigsten in Zellen früher Entwicklung und in Genen auf, die DNA, RNA und Signalwege steuern. Indem sie verfolgten, wie oft bestimmte Stellen in normalen und editierten Stammzellen genutzt wurden, fanden die Autoren heraus, dass Variante U1s dabei helfen, auszuwählen, welche verborgenen Schnittstellen erkannt werden. Der Verlust einer Variante führte dazu, dass einige Stellen übersprungen und andere häufiger genutzt wurden, was wiederum benachbarte Nachrichtenabschnitte veränderte. Einige dieser verborgenen Segmente verhalten sich wie kryptische Mini‑Exons, die normalerweise aus der finalen Botschaft ausgeschlossen sind, aber bei Kontrollverlust hineingeraten können und potenziell zu instabilen oder abgebauten RNAs führen.
Was das für Stammzellforschung und Krankheit bedeutet
Insgesamt zeigt die Arbeit, dass diese Variante U1‑RNAs keine stummen Nebencharaktere sind. Sie beeinflussen, ob Stammzellen sich teilen, welche Proteinvarianten sie produzieren können und wie lange ihre RNA‑Botschaften überdauern. Indem sie sowohl gewöhnliches als auch schrittweises Spleißen steuern, fügen sie eine feinabgestimmte Ebene zu den Genkontrollnetzwerken hinzu, die humane pluripotente Stammzellen erhalten und ihre frühen Schritte in Richtung Neuronen und anderer Zelltypen lenken. Da Gene mit diesen speziellen Spleißstellen auch genetische Varianten tragen, die mit menschlichen Erkrankungen verknüpft sind, könnte das Verständnis der Funktionsweise der Variante U1s letztlich erklären helfen, warum bestimmte Veränderungen in nichtkodierender DNA zu Entwicklungs‑ und neurologischen Krankheiten beitragen.
Zitation: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Schlüsselwörter: Stammzellen, RNA‑Spleißen, Zellzyklus, Pluripotenz, Neuroentwicklung