Clear Sky Science · ru
Вариантные U1 snRNA влияют на контроль клеточного цикла и дифференцировки человеческих iPS-клеток
Почему важны крошечные фрагменты РНК для стволовых клеток
Стволовые клетки привлекают внимание врачей и инженеров тем, что могут превращаться почти в любую клетку организма. Это обещание требует очень строгого внутреннего контроля. В этом исследовании рассматривается малоизученная группа крошечных молекул РНК в человеческих индуцированных плюрипотентных стволовых клетках и показано, что они молчаливо помогают решать, как быстро стволовые клетки делятся и насколько они готовы становиться специализированными клетками.
Маленькие помощники в фабрике клеточных сообщений
В каждой клетке гены сначала копируются в РНК‑сообщения, которые затем подрезаются и сшиваются прежде, чем будут использованы как инструкции для синтеза белков. Ключевую роль в этом механизме обработки играют небольшие РНК, называемые U1. Годы считали дополнительные копии U1‑подобных РНК бесполезными остатками. Авторы сосредоточились на двух таких «двойниках», названных вариантными U1, которые особенно активны в ранних человеческих тканях и стволовых клетках. Поскольку их последовательности немного отличаются от основной U1, они могут распознавать иные сайты разреза в РНК и тонко менять, какие варианты белков клетка может производить.
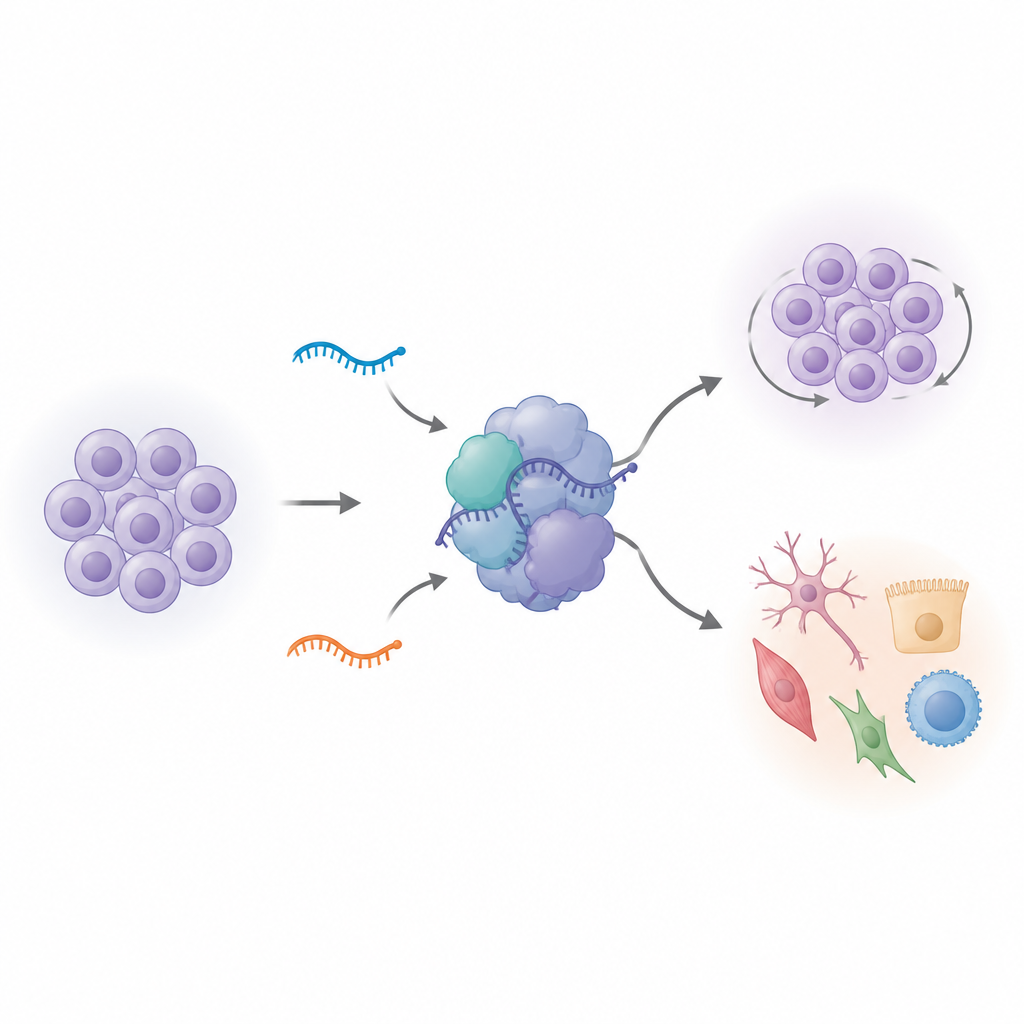
Отключение вариантных РНК меняет поведение стволовых клеток
Чтобы выяснить, что конкретно делают эти вариантные U1, команда использовала редактирование генома для удаления одного из двух вариантов в человеческих индуцированных плюрипотентных стволовых клетках. На первый взгляд отредактированные клетки выглядели нормально. Но когда исследователи измерили, какие гены включены или выключены, они обнаружили масштабные изменения, особенно при удалении варианта vU1.8. Сотни генов, связанных с делением клеток и идентичностью стволовых клеток, изменили активность. Внутренние часы клеток тоже сместились: больше клеток накопилось в более поздней фазе клеточного цикла, а общие темпы роста увеличились, когда клетки стимулировали начать дифференцировку. Гены, обычно отмечающие «стволовость» и раннее развитие мозга, перестали следовать обычным схемам, что указывает на то, что эти маленькие РНК помогают удерживать стволовые клетки в точно настроенном состоянии между самовозобновлением и специализацией.
Редактирование сообщений посредством разрезания и сшивания
Затем исследование углубилось в то, как вариантные U1 влияют на детальную обработку РНК‑сообщений. Многие человеческие гены могут быть разрезаны и сшиты по-разному, давая варианты белков, которые отличаются стабильностью, локализацией или активностью. Сравнивая нормальные и отредактированные стволовые клетки, авторы обнаружили тысячи изменений в сплайсинге РНК. Некоторые сообщения потеряли важные кодирующие фрагменты и вместо этого образовали укороченные или некодирующие версии. Один из вариантов влиял преимущественно на изменения в начале и конце сообщений, укорачивая хвостовые регионы, которые контролируют, как долго РНК сохраняется и когда она используется. Гены, связанные с делением клеток и нейрональным развитием, были особенно затронуты, что связывает эти крошечные РНК с процессами, центральными для здорового роста и формирования мозга.
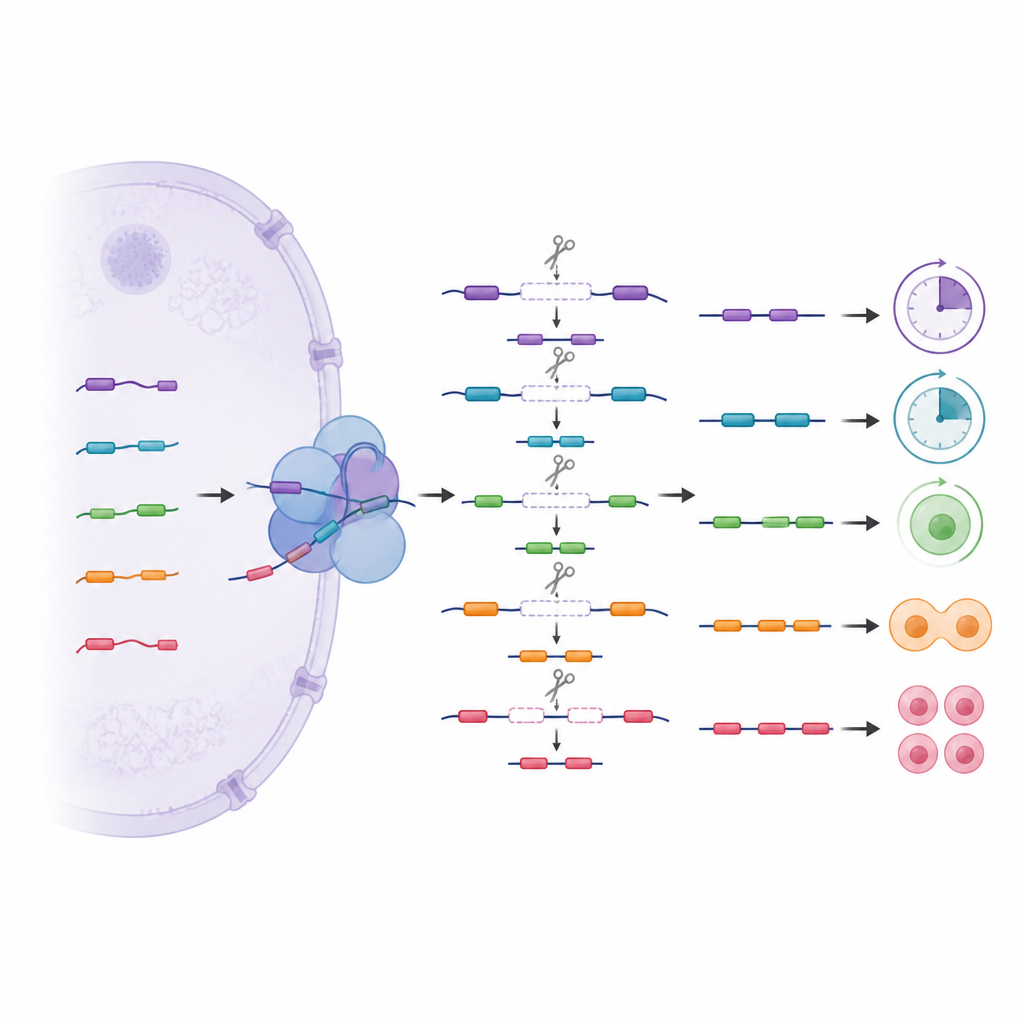
Скрытый уровень пошагового разрезания
Помимо обычного сплайсинга, команда исследовала более сложный паттерн, называемый рекурсивным сплайсингом, при котором длинные участки гена удаляются в несколько шагов с использованием скрытых внутренних сайтов разреза. Эти пошаговые разрезы были наиболее распространены в клетках раннего развития и в генах, регулирующих ДНК, РНК и сигнальные пути. Отслеживая, как часто использовались конкретные сайты в нормальных и отредактированных стволовых клетках, авторы обнаружили, что вариантные U1 помогают выбирать, какие скрытые сайты распознаются. Потеря варианта приводила к тому, что некоторые сайты пропускались, а другие использовались чаще, что, в свою очередь, изменяло соседние участки сообщений. Некоторые из этих скрытых сегментов ведут себя как криптические мини‑экзоны, которые обычно исключаются из финального сообщения, но могут включаться при нарушении контроля, что потенциально ведёт к нестабильным или деградируемым РНК.
Что это значит для науки о стволовых клетках и заболеваний
В целом работа показывает, что эти вариантные U1 РНК не являются молчаливыми наблюдателями. Они влияют на то, делятся ли стволовые клетки, какие варианты белков они могут производить и как долго живут их РНК‑сообщения. Направляя как обычный, так и пошаговый сплайсинг, они добавляют тонкую настройку в сети генетического контроля, которые поддерживают человеческие плюрипотентные стволовые клетки и управляют их ранними шагами к превращению в нейроны и другие типы клеток. Поскольку гены, содержащие эти особые сайты сплайсинга, также несут генетические варианты, связанные с человеческими расстройствами, понимание работы вариантных U1 может в конечном счёте помочь объяснить, почему некоторые изменения в некодирующей ДНК способствуют развитию и неврологическим заболеваниям.
Цитирование: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Ключевые слова: стволовые клетки, сплайсинг РНК, клеточный цикл, плюрипотентность, нейроразвитие