Clear Sky Science · fr
Les snRNAs variante U1 contribuent au contrôle du cycle cellulaire et de la différenciation des cellules iPS humaines
Pourquoi de minuscules fragments d’ARN importent pour les cellules souches
Les cellules souches fascinent médecins et ingénieurs car elles peuvent se transformer en presque n’importe quelle cellule du corps. Cette promesse repose sur un contrôle interne très strict. Cette étude examine un groupe jusque-là négligé de petits ARN présents dans les cellules souches pluripotentes induites humaines et montre qu’ils contribuent discrètement à décider la vitesse de division des cellules souches et leur propension à se spécialiser.
Petits auxiliaires dans l’usine à messages de la cellule
Dans chaque cellule, les gènes sont d’abord copiés en messages ARN, qui sont ensuite raccourcis et recousus avant d’être lus comme instructions pour fabriquer des protéines. Une part essentielle de ce mécanisme de maturation utilise de petits ARN appelés U1. Pendant des années, des copies supplémentaires d’ARN de type U1 ont été considérées comme des restes sans utilité. Les auteurs se concentrent sur deux de ces sosies, appelés U1 variants, particulièrement actifs dans les tissus précoces humains et les cellules souches. Parce que leurs séquences diffèrent légèrement de l’U1 principal, ils pourraient reconnaître des sites de coupure différents dans l’ARN et modifier subtilement les versions de protéines qu’une cellule peut produire.
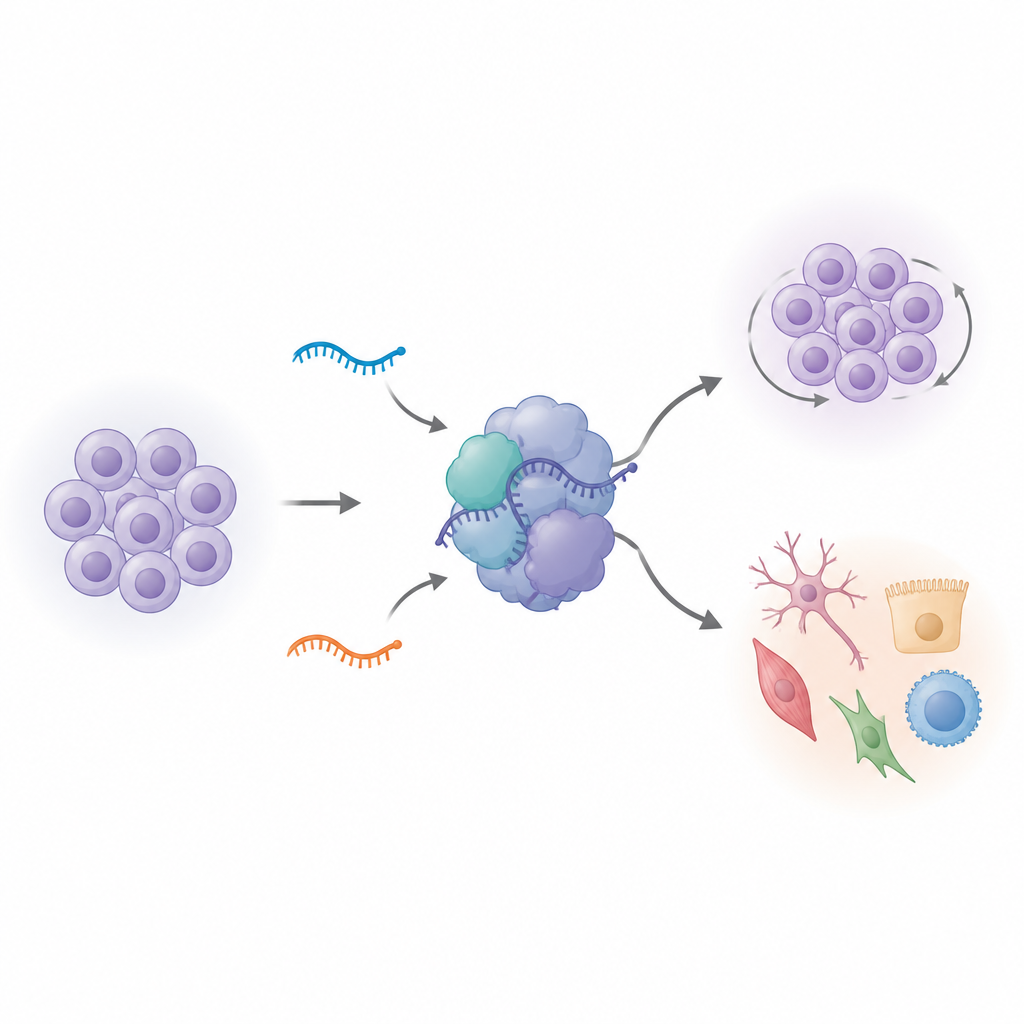
Éteindre les ARN variants reconfigure le comportement des cellules souches
Pour déterminer ce que font réellement ces U1 variants, l’équipe a utilisé l’édition du génome pour supprimer l’un ou l’autre de ces deux variants dans des cellules iPS humaines. À première vue, les cellules éditées semblaient normales. Mais lorsque les chercheurs ont mesuré quels gènes étaient activés ou réprimés, ils ont observé des changements profonds, surtout lorsque l’un des variants, vU1.8, était supprimé. Des centaines de gènes impliqués dans la division cellulaire et l’identité des cellules souches ont vu leur activité modifiée. Les rythmes internes des cellules ont également changé : davantage de cellules s’accumulaient dans une phase tardive du cycle cellulaire, et les taux de croissance globaux augmentaient lorsque les cellules étaient poussées à initier la différenciation. Des gènes marquant habituellement la « stemness » et le développement cérébral précoce n’observaient plus leurs schémas normaux, suggérant que ces petits ARN aident à maintenir les cellules souches dans un état finement réglé entre auto-renouvellement et spécialisation.
Éditer les messages en coupant et recousant
L’étude s’est ensuite penchée sur la manière dont les U1 variants influencent l’édition détaillée des messages ARN. De nombreux gènes humains peuvent être découpés et recousus de différentes manières, produisant des variantes protéiques qui diffèrent par leur stabilité, leur localisation ou leur activité. En comparant cellules souches normales et éditées, les auteurs ont découvert des milliers de changements dans la façon dont les ARN étaient épissés. Certains messages perdaient des sections codantes importantes et produisaient à la place des versions tronquées ou non codantes. Un des variants favorisait des changements au niveau des débuts et des fins des messages, élaguant les régions terminales qui contrôlent la durée de vie et l’utilisation d’un ARN. Les gènes liés à la division cellulaire et au développement neural ont été particulièrement affectés, liant ces petits ARN à des processus essentiels pour la croissance saine et la formation du cerveau.
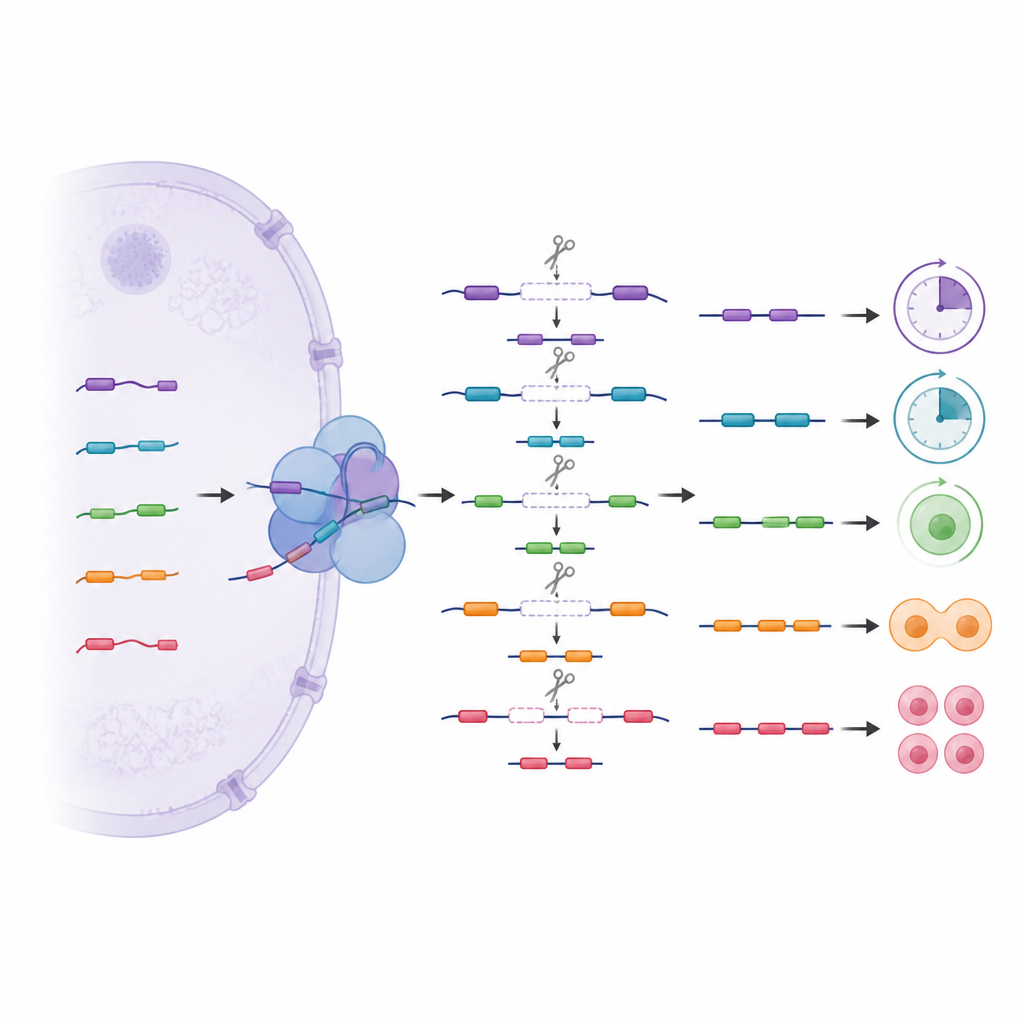
Une couche cachée de découpe par étapes
Au-delà de l’épissage ordinaire, l’équipe a exploré un schéma plus complexe appelé épissage récursif, dans lequel de longs segments géniques sont retirés en plusieurs étapes en utilisant des sites de coupure internes cachés. Ces découpes par étapes étaient les plus fréquentes dans les cellules du début du développement et dans les gènes qui gèrent l’ADN, l’ARN et la signalisation cellulaire. En suivant la fréquence d’utilisation de sites spécifiques dans les cellules normales et éditées, les auteurs ont montré que les U1 variants aident à choisir quels sites internes sont reconnus. La perte d’un variant entraînait l’ignorance de certains sites et l’utilisation accrue d’autres, ce qui modifiait à son tour les segments de message voisins. Certains de ces segments masqués se comportent comme des mini-exons cryptiques qui sont normalement exclus des messages finaux mais peuvent s’y glisser lorsque le contrôle est perdu, conduisant potentiellement à des ARN instables ou dégradés.
Ce que cela signifie pour la science des cellules souches et la maladie
Globalement, ce travail révèle que ces ARN U1 variants ne sont pas de simples spectateurs. Ils influencent la division des cellules souches, les versions de protéines qu’elles peuvent produire et la durée de vie de leurs messages ARN. En orientant à la fois l’épissage ordinaire et l’épissage par étapes, ils ajoutent une couche de réglage fin aux réseaux de contrôle génique qui soutiennent les cellules souches pluripotentes humaines et guident leurs premiers pas vers des neurones et d’autres types cellulaires. Comme les gènes contenant ces sites d’épissage particuliers hébergent aussi des variants génétiques associés à des pathologies humaines, comprendre le fonctionnement des U1 variants pourrait à terme aider à expliquer pourquoi certaines altérations de l’ADN non codant contribuent aux troubles développementaux et neurologiques.
Citation: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Mots-clés: cellules souches, épissage de l’ARN, cycle cellulaire, pluripotence, neurodéveloppement